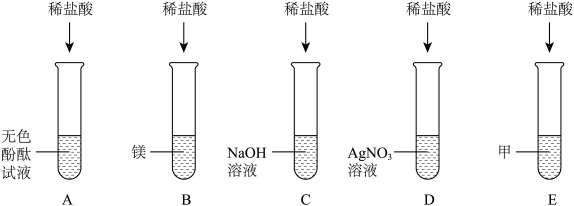
氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。探究小组的同学把定量的CaH2加入Na2CO3溶液,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中Na2CO3的成分是什么?
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
【实验验证】
【反思与拓展】
(1)写出氢化钙(CaH2)与水反应的化学方程式___________ 。
(2)若向NH4C1的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和___________ 。
(3)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是___________ (写一条即可)
【提出问题】滤液中Na2CO3的成分是什么?
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
【实验验证】
| 实验 | 现象 | 结论 |
| (1)取少量滤液,向其中滴入少量碳酸钠溶液 | 猜想二不成立 | |
| (2)另取少量滤液,向其中加入足量 | 猜想三成立,发生反应的化 学方程式 |
【反思与拓展】
(1)写出氢化钙(CaH2)与水反应的化学方程式
(2)若向NH4C1的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和
(3)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是
更新时间:2020-08-04 10:15:47
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
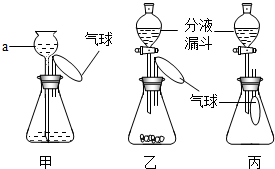
【推荐1】某化学兴趣小组设计了一组“吹气球”实验,三套装置如下图:
(1)甲装置:
①仪器a 的名称为______________
②向a 中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性________________ 。
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是__________________
②若生成H2使气球胀大,则反应的化学方程式为_______________ 。
③若锥形瓶中装有CaO 固体,分液漏斗中加入少量水,则气球胀大的主要原因是______________ ,反应的化学方程式是 ______________ 。
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大, 则分液漏斗中的液体可以是___________ 。锥形瓶中发生的化学方程式是 ___________ 。

(1)甲装置:
①仪器a 的名称为
②向a 中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是
②若生成H2使气球胀大,则反应的化学方程式为
③若锥形瓶中装有CaO 固体,分液漏斗中加入少量水,则气球胀大的主要原因是
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大, 则分液漏斗中的液体可以是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】我国制碱工业先驱侯德榜以NaCl、NH3、CO2等为原料制得NaHCO3,生产出纯碱(Na2CO3),“侯氏制碱法”为世界制碱工业做出了突出贡献。如图C至E为实验室模拟制碱工艺的装置图。回答下列问题:
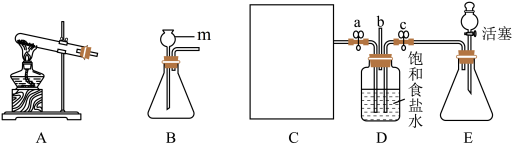
(1)实验仪器m的名称是______ ,实验室制取二氧化碳发生装置选择E,其优点是______ ,该反应的化学方程式为______ 。检查E装置的气密性,可先关闭弹簧夹c,向分液漏斗中注水,立即打开活塞,观察到______ ,则气密性良好。
(2)实验室若用加热氯化铵固体和氢氧化钙固体制取氨气,C处制取氨气应选择的发生装置是______ (填“A”或“B”),该反应的化学方程式为:______ 。
(3)已知NH3极易溶于水,实验时应先打开弹簧夹______ (填a或c),后打开另一个弹簧夹才能保证二氧化碳更容易被吸收。
(4)已知NH3有刺激性气味,D装置中的b导管应最好连接______ 装置(填字母)。


(1)实验仪器m的名称是
(2)实验室若用加热氯化铵固体和氢氧化钙固体制取氨气,C处制取氨气应选择的发生装置是
(3)已知NH3极易溶于水,实验时应先打开弹簧夹
(4)已知NH3有刺激性气味,D装置中的b导管应最好连接

您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】下图是实验室制取气体的部分装置,请回答下列问题:

(1)写出仪器a的名称___________ 。
(2)氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。欣悦同学用锌粒与盐酸反应制取氢气,选择的装置组合是_________ (填字母)。若用F装置排空气法收集氢气,气体应从______ 端进入(填b或c)。
【提出问题】①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
【设计实验方案】欣悦同学按下图装置进行实验(假设每个装置中气体都完全反应或吸收)。

【实验现象和结论】
【交流总结】
根据丁装置中实验现象,说明氢气具有____________ 性。
②丁装置加热前通入H2的目的是_______________________________________ 。

(1)写出仪器a的名称
(2)氢气是最理想的燃料。通常状况下,氢气密度比空气小,难溶于水。欣悦同学用锌粒与盐酸反应制取氢气,选择的装置组合是
【提出问题】①导出的气体除H2外,还有哪些气体?
②氢气具有可燃性外,还具有什么化学性质?
【设计实验方案】欣悦同学按下图装置进行实验(假设每个装置中气体都完全反应或吸收)。

【实验现象和结论】
| 实验现象 | 实验结论 |
| 甲装置中的白色固体变成蓝色 | 气体中有 |
| 乙装置中产生 | 气体中有HCl |
| 丁装置中玻璃管内红色粉末变成黑色、戊装置中白色固体变成蓝色 | H2能与Fe2O3反应 丁装置中玻璃管内反应的化学方程式 为 |
根据丁装置中实验现象,说明氢气具有
②丁装置加热前通入H2的目的是
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】为测定某碳酸钠样品中氯化钠的含量(无其他杂质),进行如下实验:
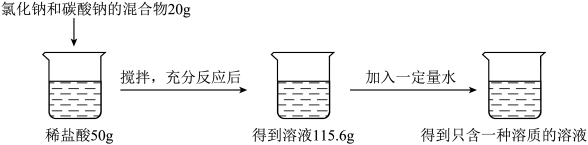
(1)上述实验过程中发生反应的化学方程式为___________ 。
(2)样品中氯化钠的质量分数是___________ 。
(3)向反应后所得溶液中加入___________ g水,最终所得溶液的溶质质量分数为10%;
(4)现质量分数为36.5%的浓盐酸配制上述实验用稀盐酸需要加水___________ mL。(水的密度1g/mL)
(5)上述配制过程中,需用仪器有烧杯、量筒、玻璃棒和___________ 。

(1)上述实验过程中发生反应的化学方程式为
(2)样品中氯化钠的质量分数是
(3)向反应后所得溶液中加入
(4)现质量分数为36.5%的浓盐酸配制上述实验用稀盐酸需要加水
(5)上述配制过程中,需用仪器有烧杯、量筒、玻璃棒和
您最近一年使用:0次