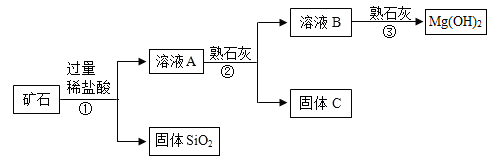
某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图所示:
回答下列问题:
(1)步骤①和步骤②均用到的操作是_________________ ,该操作中用到的玻璃棒的作用是 _______ 。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和_________ (填离子符号)。步骤①中发生反应的化学方程式是(只要求写出一个)_______________ 。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
步骤②加入熟石灰,调节溶液的pH范围为_______________ ,固体C中所含成分的化学式为 ___________ 。
(4)步骤③中制得Mg(OH)2的化学方程式为_____ 。在医药上,氢氧化镁可用来____ 。

回答下列问题:
(1)步骤①和步骤②均用到的操作是
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
| 对应离子 | Fe3+ | Cu2+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
(4)步骤③中制得Mg(OH)2的化学方程式为
更新时间:2020-08-17 10:07:06
|
相似题推荐
填空与简答-简答题
|
较难
(0.4)
解题方法
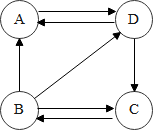
【推荐1】A、B、C、D均为初中化学常见的物质,它们的组成中都含有一种相同的元素,其中A为单质。B、D属于同一种物质类别,且B中金属元素的质量分数为40%。C为蓝色沉淀。它们之间转化关系如图所示(“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。A的化学式为______ ;B的一种用途是______ ;D→C反应的化学方程式为______ 。

您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】某同学在构建碳及其化合物化学性质知识网络时,得到如图的反应关系图,已知A~L均为初中化学常见物质,其中物质J常在农业上用来配制波尔多液,物质C和H是由相同元素组成的两种气体(部分反应条件已省略)。
(1)E的化学式为_______ 。
(2)反应①的基本反应类型为_______ 。
(3)反应③的化学方程式为_______ 。
(4)反应②中F物质表现出_______ 性。

(1)E的化学式为
(2)反应①的基本反应类型为
(3)反应③的化学方程式为
(4)反应②中F物质表现出
您最近一年使用:0次
【推荐3】终身学习是贯穿一生的好习惯。出生于1922年的John Goodenough人称“足够好”先生,因在锂离子电池及钴酸锂(LiCoO2)、磷酸铁翅(LiFePO4)等正极材料研究方面的卓越贡献于97岁高龄获得2019年诺贝尔化学奖。回答下列问题:
(1)新能源电动车使用的磷酸铁锂电池反应原理为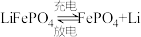 该反应放电时,发生的化学反应属于
该反应放电时,发生的化学反应属于___________ (填基本反应类型)。
(2)磷酸铁可以按 。(填编号)分类
(3)依据各类物质之间的反应规律,设计两种制各磷酸铁(FePO4)的方案(要求依据两种不同的反应规律)。
已知:①磷酸铁(FePO4)的铁元素显正三价,是一种几乎不溶于水的白色固体:
②磷酸(H3PO4)为可溶性酸。完成下表:
(1)新能源电动车使用的磷酸铁锂电池反应原理为
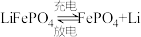 该反应放电时,发生的化学反应属于
该反应放电时,发生的化学反应属于(2)磷酸铁可以按 。(填编号)分类
| A.纯净物 | B.化合物 | C.盐 | D.铁盐 |
已知:①磷酸铁(FePO4)的铁元素显正三价,是一种几乎不溶于水的白色固体:
②磷酸(H3PO4)为可溶性酸。完成下表:
| 方案 | 原料 | 预期反应的化学方程式 | 依据的反应规律 |
| ① | 金属氧化物与酸反应生成盐和水 | ||
| ② |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】下面五环图种的每个环代表初中化学中常见的一种物质,它们分别属于单质、氧化物、酸、碱、盐中的一种。相邻两环相绕表示两种物质之间在常温下能相互反应。
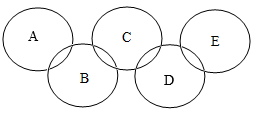
(1)请写出五环图中A、B、C、D、E五种物质的化学式:_____ ,_____ ,_____ ,_____ ,_____ 。
(2)写出C和D反应的化学方程式:_____ ;

(1)请写出五环图中A、B、C、D、E五种物质的化学式:
(2)写出C和D反应的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】如图所示,甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钡、硫酸铜、碳酸钠五种物质中的一种。相邻物质能够发生反应,甲是胃酸的主要成分。请回答下列问题:

(1)上述五种物质中,可用于配制波尔多液的是____ (填化学式);能相互反应生成气体的两种物质可能是____ 。
(2)若丙为氢氧化钡,则乙为___ ;戊为____ 。丙和丁发生反应的化学方程式为__ ,该反应属于____ (填基本反应类型)。

(1)上述五种物质中,可用于配制波尔多液的是
(2)若丙为氢氧化钡,则乙为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】“天问一号”环绕器是一座通信“中继站”,为火星表面巡视器与地球之间的通讯搭建起桥梁。硫酸铜、碳、二氧化碳、氧化铜、盐酸、氢氧化钙、碳酸钠七种物质组合出如图所示的“化学号”环绕器,图中相邻的两种物质能发生反应(所涉及的反应均为初中常见的化学反应)。已知常温下D为气体,G的溶液显蓝色。请回答下列问题:
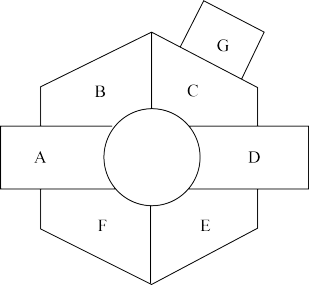
(1)D的化学式为______ 。
(2)图中不涉及的基本反应类型为______ 。
(3)A与F反应的化学方程式为______ 。
(4)下列选项中可以替换E、F的物质分别是______(填序号,双选)。

(1)D的化学式为
(2)图中不涉及的基本反应类型为
(3)A与F反应的化学方程式为
(4)下列选项中可以替换E、F的物质分别是______(填序号,双选)。
| A.H2O、CaO | B.O2、Fe | C.MgCl2、Fe2O3 | D.Ba(OH)2、K2CO3 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
【推荐1】实验室有一固体混合物,可能含有Fe2O3、Cu、C、NH4HCO3、NH4Cl、(NH4)2SO4等物质中的一种或几种,某实验小组通过以下两个实验进行检验,请回答相关问题:
已知:
实验一:
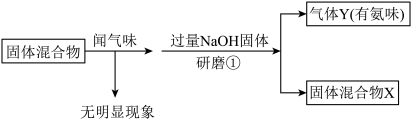
(1)由实验一可知:固体混合物中一定没有_______ (填名称)。
实验二:
取实验一所得固体混合物X继续实验,流程如下:
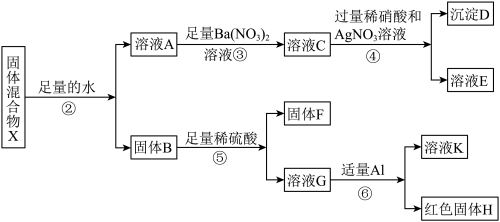
(2)结合实验现象分析,写出步骤①中产生气体Y的化学方程式___________ ;
(3)写出溶液E中一定含有的溶质_______________ (填化学式);
(4)由步骤⑤⑥可知,固体B中一定含有___________ (填化学式);
(5)固体F的组成有________ 种情况(填数字)。
已知:

实验一:

(1)由实验一可知:固体混合物中一定没有
实验二:
取实验一所得固体混合物X继续实验,流程如下:

(2)结合实验现象分析,写出步骤①中产生气体Y的化学方程式
(3)写出溶液E中一定含有的溶质
(4)由步骤⑤⑥可知,固体B中一定含有
(5)固体F的组成有
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,将其任意编号为:A、B、C、D、E,然后两两混合进行实验,其部分实验现象如下表(说明:硫酸钙视为可溶物):
(1)写出溶液A中溶质的化学式:A_____ 。
(2)写出溶液A与B反应的化学方程式:_____ 。
(3)写出溶液C和D反应的化学方程式:_____ 。
| 实验 | A+B | B+C | B+D | C+D |
| 现象 | 产生沉淀 | 产生气体 | 产生沉淀 | 产生沉淀 |
(2)写出溶液A与B反应的化学方程式:
(3)写出溶液C和D反应的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】现有一包固体粉末,可能是CaCO3、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验。请根据实验现象判断:
(1)取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有_______ 、_______ 。
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡。则此固体粉末中一定有_________ 、________ 。
(3)取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确______ 填“是”或“否”)。
(4)对于是否含有NaCl,你认为应对步骤(2)作如何改进__________ (若步骤(3)填“是”,此空不作答)。
(1)取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有
(2)取上述溶液适量,滴加过量的BaCl2溶液,出现白色沉淀,再加入过量的稀硝酸,沉淀部分消失并产生气泡。则此固体粉末中一定有
(3)取步骤(2)实验后的上层清液,加入稀硝酸、硝酸银溶液,出现白色沉淀,由此该同学得出此固体粉末中一定含有NaCl,你认为此结论是否正确
(4)对于是否含有NaCl,你认为应对步骤(2)作如何改进
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】氧化锌( ZnO)可作为紫外线吸收剂应用于化妆品中,其一种生产工艺如下图所示:

据图分析并回答下列问题:
(1)推测草酸的化学式是_____________________ 。
(2)“沉锌”过程中发生复分解反应,反应的化学方程式为_____________________ 。
(3)“操作A”的名称是_____________________ 。
(4)“高温灼烧”时草酸锌分解,写出该反应的化学方程式_____________________ 。

据图分析并回答下列问题:
(1)推测草酸的化学式是
(2)“沉锌”过程中发生复分解反应,反应的化学方程式为
(3)“操作A”的名称是
(4)“高温灼烧”时草酸锌分解,写出该反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
【推荐2】二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
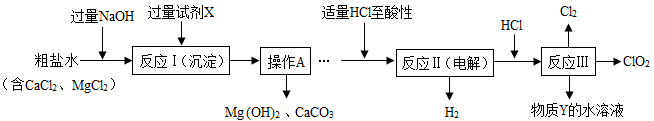
(1)试剂X是________ (填化学式);操作A的名称是_________ ;加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,请写出其中所发生的中和反应的化学方程式:________________________________ 。
(2)分析完成反应Ⅱ的化学方程式:______________ 。
(3)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是_________ 。

(1)试剂X是
(2)分析完成反应Ⅱ的化学方程式:
(3)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下:
 回答下列问题:
回答下列问题:
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,错误的是________ 。
(2)操作②的名称是____________ 。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),能否将BaCl2溶液改用硝酸钡溶液?说明原因。_________________________________ 。有同学提出用___________ 溶液代替BaCl2溶液和NaOH溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是_________________ 。
(5)该流程中可以循环利用的物质是________ 。
(6)加入过量Na2CO3溶液的理由是___________________________________ 。为什么先过滤而后加盐酸,其理由是_______________________________________________________ 。
(7)请再写出一种粗盐提纯的试验方案,添加试剂的顺序为:_____________________________ 。
 回答下列问题:
回答下列问题:(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,错误的是
A.能去除油污,可做厨房清洁剂 B.易溶于水,溶解时放出大量的热
C.水溶液能使石蕊溶液变红 D.可用作某些气体的干燥剂
(2)操作②的名称是
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),能否将BaCl2溶液改用硝酸钡溶液?说明原因。
(4)电解饱和NaCl溶液的化学方程式是
(5)该流程中可以循环利用的物质是
(6)加入过量Na2CO3溶液的理由是
(7)请再写出一种粗盐提纯的试验方案,添加试剂的顺序为:
您最近一年使用:0次



