学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究。
【探究一】影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
(1)对比③④两组实验,可得出过氧化氢分解速率与温度的关系:当过氧化氢溶液的体积和浓度等其它条件相同时,_____ 。
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是______ 填实验序号)。
【探究二】其他金属氧化物能否起到类似 MnO2 的催化作用?
兴趣小组同学用天平称量 0.2 g CuO,用量筒量取 5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。
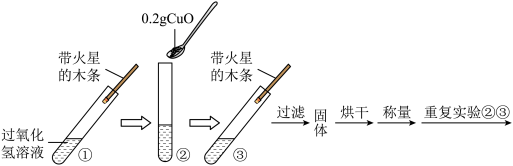
(3)小组同学通过上述实验得出结论:CuO 可作过氧化氢分解的催化剂,支持该结论的实验证据是_____ 。
(4)欲比较不同催化剂 CuO 和 MnO2对H2O2 分解速率的影响,实验时需要控制的变量有_____ 。
(5)过氧化氢能被MnO2 催化分解放出氧气的文字(或符号)表达式为_____ 。
【探究一】影响过氧化氢分解速率的因素有哪些? 兴趣小组同学做了四个实验,实验数据如下表:
| 实验 序号 | H2O2 溶液的溶质质量分数% | H2O2 溶液的体积/mL | 温 度 /℃ | MnO2的用量/g | 收集O2的体积/mL | 反应 时间 |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16 s |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6 s |
| ③ | 30 | 5 | 35 | 0 | 4 | 98 min |
| ④ | 30 | 5 | 55 | 0 | 4 | 2 0min |
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是
【探究二】其他金属氧化物能否起到类似 MnO2 的催化作用?
兴趣小组同学用天平称量 0.2 g CuO,用量筒量取 5 mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤)。

(3)小组同学通过上述实验得出结论:CuO 可作过氧化氢分解的催化剂,支持该结论的实验证据是
(4)欲比较不同催化剂 CuO 和 MnO2对H2O2 分解速率的影响,实验时需要控制的变量有
(5)过氧化氢能被MnO2 催化分解放出氧气的文字(或符号)表达式为
更新时间:2020-10-11 10:25:10
|
相似题推荐
【推荐1】先进的催化技术已成为当今化工技术开发和进步的动力,大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是___________ 。
(2)某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢的分解速率加快。对于此现象,小组同学进行如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
写出淀粉催化过氧化氢分解的文字(或符号)表达式:___________ 。
【实验拓展】小组同学设计了如图装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,相关数据见表:

表中划线处应填___________ ,表中的“待测数据”是指___________ ;若a>b,则可得出___________ 的催化效果较好。
(1)化工生产使用催化剂的目的是
(2)某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢的分解速率加快。对于此现象,小组同学进行如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
| 取A、B两支试管,各加入5mL5%的过氧化氢溶液,仅向B试管中加入0.2g淀粉,分别伸入带火星的木条 | A中无明显现象;B中产生大量气泡,带火星的木条复燃 | B中产生的气体是 |
| 向B试管中重新加入5%的过氧化氢溶液,伸入带火星的木条,反应停止后过滤、洗涤、干燥、称量固体 | B中又产生大量气泡,带火星的木条复燃;固体质量为 | 反应前后淀粉的质量和 |
【实验拓展】小组同学设计了如图装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,相关数据见表:

| 实验 | 5%的H2O2溶液的体积 | 催化剂 | 待测数据 |
| 1 | 20mL | 淀粉0.5g | a |
| 2 | 20mL | __________ | b |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验小组研究不同催化剂对过氧化氢分解速率的影响。
【查阅资料】①MnO2、FeCl3均可作为加快过氧化氢分解速率的催化剂。
②锥形瓶内氧气浓度达到最大值时,表明过氧化氢已完全分解。
【实验准备】组装图1所示装置(夹持仪器已略),经检验,装置的气密性良好。

(1)此装置中注射器替代长颈漏斗的优点是_______________ 。
实验1:比较催化剂种类对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入催化剂,用注射器推入过氧化氢溶液,记录实验数据。
【解释与结论】
(2)用MnO2催化过氧化氢分解的符号或文字表达式为_______________ 。
(3)为达成实验1的目的,需要被控制成相同的变量有过氧化氢溶液的浓度、_______ 和________ 。
(4)依据实验1的数据可推知MnO2催化过氧化氢分解的速率大于FeCl3,其证据是_______________ 。
实验2:继续探究FeCl3质量对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入FeCl3,用注射器推入5%过氧化氢溶液,记录实验数据。
【解释与结论】
(5)由实验2可得结论:FeCl3质量在0.03~0.05g范围内,_______________ 。
【反思与评价】
(6)实验小组用1-2的方案制备氧气,发现反应速率偏慢。根据上述实验结论,你认为可采取的改进措施有①_______________ ,②_______________ 写出两条。
【查阅资料】①MnO2、FeCl3均可作为加快过氧化氢分解速率的催化剂。
②锥形瓶内氧气浓度达到最大值时,表明过氧化氢已完全分解。
【实验准备】组装图1所示装置(夹持仪器已略),经检验,装置的气密性良好。

(1)此装置中注射器替代长颈漏斗的优点是
实验1:比较催化剂种类对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入催化剂,用注射器推入过氧化氢溶液,记录实验数据。
| 序号 | 药品 | 氧气浓度传感器的数据 | |
| 1-1 | 3mL、5%过氧化氢溶液 | 0.03gMnO2固体 |  |
| 1-2 | 3mL、5%过氧化氢溶液 | 0.03 g FeCl3固体 |  |
(2)用MnO2催化过氧化氢分解的符号或文字表达式为
(3)为达成实验1的目的,需要被控制成相同的变量有过氧化氢溶液的浓度、
(4)依据实验1的数据可推知MnO2催化过氧化氢分解的速率大于FeCl3,其证据是
实验2:继续探究FeCl3质量对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入FeCl3,用注射器推入5%过氧化氢溶液,记录实验数据。
| 序号 | FeCl3质量 | 过氧化氢溶液体积 | 过氧化氢完全分解所用时间 |
| 2-1 | 0.03g | 3 mL | 61s |
| 2-2 | 0.04g | 3 mL | 56s |
| 2-3 | 0.05g | 3 mL | 49s |
(5)由实验2可得结论:FeCl3质量在0.03~0.05g范围内,
【反思与评价】
(6)实验小组用1-2的方案制备氧气,发现反应速率偏慢。根据上述实验结论,你认为可采取的改进措施有①
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】实验室常用加热氯酸钾和少量二氧化锰的混合物的方法制取氧气,写出该反应的符号表达式______________ 。
小明发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是他进行了如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表完成实验并记录数据:分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)通过实验__________ 与实验④对比,证明小明的猜想是合理的。
(2)实验所用的三种物质,催化效果由好到差的顺序是____________________ 。
【反思】
(1)如果要证明氧化铁是该反应的催化剂,还要验证氧化铁的______ 和____________ 在反应前后不变。
(2)当使用同种催化剂时,可能影响催化效果的因素有____________________________ 。
小明发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是他进行了如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表完成实验并记录数据:分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(1)通过实验
(2)实验所用的三种物质,催化效果由好到差的顺序是
【反思】
(1)如果要证明氧化铁是该反应的催化剂,还要验证氧化铁的
(2)当使用同种催化剂时,可能影响催化效果的因素有
您最近一年使用:0次
【推荐1】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
【实验验证】
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催剂。
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三的目的是探究____________________________________ 。
【实验步骤】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、________ ;④对比反应前后Al2O3的质量。
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四,实验四的目的是探究_________________________________ 。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢。 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中。 | 产生大量的气泡 木条复燃 |
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三的目的是探究
【实验步骤】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四,实验四的目的是探究
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】如图是实验室制取气体的常用装置。
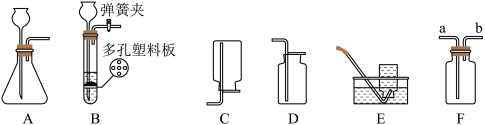

| I.氧气的制取 | Ⅱ.二氧化碳的制取 |
| (1)用A装置制取氧气的化学方程式是 (2)用E装置比用D装置收集氧气的优点是 | (1)用B装置制备二氧化碳的优点是 (2)若用F装置收集CO2,气体应从 (3)收集二氧化碳不选用C、E装置的原因是 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】催化剂可显著提高反应速率,二氧化锰是常见的催化剂。
(1)探究催化剂的用量对过氧化氢分解速率的影响。每次实验均用3mL10%的 溶液,采用不同质量的
溶液,采用不同质量的 粉末作催化剂,测定收集到500mL氧气所用的时间,结果如下:
粉末作催化剂,测定收集到500mL氧气所用的时间,结果如下:
由实验结果可得出的结论是______ 。
(2) 对
对 分解也有催化作用。为比较
分解也有催化作用。为比较 和
和 对
对 分解快慢的不同影响,用如图甲装置进行实验:启动传感器,注入
分解快慢的不同影响,用如图甲装置进行实验:启动传感器,注入 溶液,氧气体积分数随时间变化情况如图乙、丙。
溶液,氧气体积分数随时间变化情况如图乙、丙。
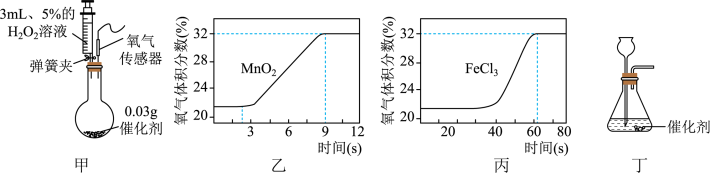
i、初始时氧气的体积分数不为0,原因是______ 。
ii、使 分解较快的催化剂是
分解较快的催化剂是______ ,判断依据是______ 。
iii、用 溶液制取氧气,若采用如图丁所示装置进行实验,上述两种催化剂中较为合适的是
溶液制取氧气,若采用如图丁所示装置进行实验,上述两种催化剂中较为合适的是______ ,原因是______ 。
(1)探究催化剂的用量对过氧化氢分解速率的影响。每次实验均用3mL10%的
 溶液,采用不同质量的
溶液,采用不同质量的 粉末作催化剂,测定收集到500mL氧气所用的时间,结果如下:
粉末作催化剂,测定收集到500mL氧气所用的时间,结果如下:| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 粉末用量/g 粉末用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间/s | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 |
(2)
 对
对 分解也有催化作用。为比较
分解也有催化作用。为比较 和
和 对
对 分解快慢的不同影响,用如图甲装置进行实验:启动传感器,注入
分解快慢的不同影响,用如图甲装置进行实验:启动传感器,注入 溶液,氧气体积分数随时间变化情况如图乙、丙。
溶液,氧气体积分数随时间变化情况如图乙、丙。
i、初始时氧气的体积分数不为0,原因是
ii、使
 分解较快的催化剂是
分解较快的催化剂是iii、用
 溶液制取氧气,若采用如图丁所示装置进行实验,上述两种催化剂中较为合适的是
溶液制取氧气,若采用如图丁所示装置进行实验,上述两种催化剂中较为合适的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐1】化学小组围绕“铁丝在氧气中燃烧现象及产物”进行了相应的探究活动。
活动 1:“火星四射”的现象与铁丝含碳量的关系?
活动 2:生成的黑色固体中是否含有铁?
查阅资料:①铁粉是黑色或灰黑色粉末,四氧化三铁为黑色固体,具有磁性。
②铁、四氧化三铁均能溶于稀盐酸。(即:铁+盐酸→氯化亚铁+氢气;四氧化三铁+盐酸→氯化铁+氯化亚铁+水)
③氯化亚铁溶液为浅绿色,氯化铁溶液为黄色。
小明质疑小刚用磁铁来检验黑色固体是否含有铁的方案,其理由是____________ ; 同学们都认可了下列实验方案:
活动 1:“火星四射”的现象与铁丝含碳量的关系?
| 实验操作 | 实验现象 | 实验结论 |
| 实验 1:取直径 0.20mm,含碳 0.1%的铁丝在氧气中燃烧。 | 零星火星 | “火星四射”与铁丝含碳量的关系是 |
| 实验 2:取直径 | 较明显的火星四射 |
活动 2:生成的黑色固体中是否含有铁?
查阅资料:①铁粉是黑色或灰黑色粉末,四氧化三铁为黑色固体,具有磁性。
②铁、四氧化三铁均能溶于稀盐酸。(即:铁+盐酸→氯化亚铁+氢气;四氧化三铁+盐酸→氯化铁+氯化亚铁+水)
③氯化亚铁溶液为浅绿色,氯化铁溶液为黄色。
小明质疑小刚用磁铁来检验黑色固体是否含有铁的方案,其理由是
| 实验操作 | 实验现象 | 实验结论 |
| 取少量黑色固体于试管中,加入一定量 | 黑色固体中含有铁 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】二氧化锰可作过氧化氢分解的催化剂,兴趣小组想探究过氧化氢分解有没有其他催化剂。影响过氧化氢分解的因素,除催化剂外,还有什么?
Ⅰ.【提出问题】氧化铜是否也能作过氧化氢分解的催化剂?与二氧化锰相比效果怎样?
【设计实验】以生成等体积的氧气为标准,设计如下实验(其他影响因素均忽略)。
(1)上述实验应测量的“待测数据“是_______ 。
(2)若y比x的数值_______ ,则说明氧化铜能加快过氧化氢的分解速率。
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中,向试管中加入适量的过氧化氢溶液,观察到_______ 。
【预期结论】氧化铜也能作过氧化氢分解的催化剂。
【评价设计】你认为设计实验③和实验②对比的目的是_______ 。
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
【交流讨论】可以通过测定相同条件下不同浓度过氧化氢溶液_______ 来探究。
A.产生相同体积氧气的时间 B.产生氧气的质量
C.产生氧气的总体积 D.单位时间内产生氧气的体积
【实验探究】按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、3。

【实验结论】图2说明过氧化氢溶液浓度与反应速率关系是_______ 。
图3说明从温度看,过氧化氢溶液浓度越高,反应越_______ (填“剧烈”或“平稳”)。
Ⅰ.【提出问题】氧化铜是否也能作过氧化氢分解的催化剂?与二氧化锰相比效果怎样?
【设计实验】以生成等体积的氧气为标准,设计如下实验(其他影响因素均忽略)。
| 实验序号 | 3%的过氧化氢溶液体积/mL | 其他物质质量/g | 待测数据 |
| ① | 20 | x | |
| ② | 20 | 氧化铜 0.5 | y |
| ③ | 20 | 二氧化锰 0.5 | z |
(2)若y比x的数值
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中,向试管中加入适量的过氧化氢溶液,观察到
【预期结论】氧化铜也能作过氧化氢分解的催化剂。
【评价设计】你认为设计实验③和实验②对比的目的是
Ⅱ.探究过氧化氢溶液浓度对过氧化氢分解速率的影响。
【交流讨论】可以通过测定相同条件下不同浓度过氧化氢溶液
A.产生相同体积氧气的时间 B.产生氧气的质量
C.产生氧气的总体积 D.单位时间内产生氧气的体积
【实验探究】按图1装置进行实验:水浴温度控制在21℃,二氧化锰均为0.5g,过氧化氢溶液均为5mL,三颈瓶容积为250mL,恒压漏斗(漏斗的支管与三颈瓶相连)的作用是使过氧化氢溶液自行下滴。数字传感器数据绘制图像如图2、3。

【实验结论】图2说明过氧化氢溶液浓度与反应速率关系是
图3说明从温度看,过氧化氢溶液浓度越高,反应越
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】柿饼是深受人们喜欢的大众食品,出霜效果是柿饼质量的重要标准。小组同学实验探究柿饼出霜的影响因素。
【查阅资料】
1 柿饼出霜期间易生霉菌导致变质,熏硫处理是控制霉变的方法之一。国家出口标准要求柿饼含硫量应小于0.5mg/100g。
2 评分越高、“霜量级别”值越小,柿饼出霜效果越好。评分标准如下:
【进行实验】
实验1:探究温度对柿饼出霜效果的影响
实验2:探究熏硫时间对柿饼出霜过程中霉变的影响
在4℃下,按试样与柿皮(含水量2.6%)质量比为4:1进行实验,50天后,记录如下:
实验3:探究柿皮对柿饼出霜效果的影响
试样经熏硫2h处理,在4℃下进行实验,50天后,记录如下:
【解释与结论】
(1)实验1中,______ ℃时,柿饼出霜效果最好。
(2)实验2中,熏硫的作用是______ 。
(3)实验3中,得出“柿皮含水量低能促进柿饼出霜”的结论,需要对比______ (填序号)。
(4)进行实验①~⑤的目的是______ 。
【反思与评价】
(5)实验1中,需要控制的实验条件是:试样与柿皮(含水量2.6%)质量比为4:1、熏硫时间2h和______ 。
(6)某同学认为“在制作柿饼时,熏硫时间越长,控制霉变效果越好”,你是否同意此观点,并说明理由______ 。
【查阅资料】
1 柿饼出霜期间易生霉菌导致变质,熏硫处理是控制霉变的方法之一。国家出口标准要求柿饼含硫量应小于0.5mg/100g。
2 评分越高、“霜量级别”值越小,柿饼出霜效果越好。评分标准如下:
| 柿霜分布量占柿饼表面积的百分数/% | 0~40 | 41~60 | 61~80 | 81~100 |
| 评分标准/分 | 0~4.0 | 4.1~7.0 | 7.1~8.9 | 9.0~10 |
| 霜量级别/级 | 4 | 3 | 2 | 1 |
实验1:探究温度对柿饼出霜效果的影响
| 温度/℃ | 4 | 13 | 20 |
| 得分 | 9.3 | 3.1 | 0.7 |
在4℃下,按试样与柿皮(含水量2.6%)质量比为4:1进行实验,50天后,记录如下:
| 熏硫时间/h | 0 | 2 | 4 | 6 | 8 |
| 柿饼含硫量/mg/100g) | 0 | 0.27 | 0.43 | 0.67 | 0.98 |
| 霉变情况 | 发生霉变 | 没有霉变 | |||
试样经熏硫2h处理,在4℃下进行实验,50天后,记录如下:
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 柿皮含水量/% | 2.6 | 2.6 | 2.6 | 2.6 | 2.6 | 4.3 | 8.8 | 16.1 |
| 试样与柿皮质量比 | 2:1 | 4:1 | 8:1 | 16:1 | 1:0 | 4:1 | 4:1 | 4:1 |
| 得分 | 9.2 | 9.0 | 2.3 | 0.5 | 0.3 | 8.6 | 1.6 | 0 |
(1)实验1中,
(2)实验2中,熏硫的作用是
(3)实验3中,得出“柿皮含水量低能促进柿饼出霜”的结论,需要对比
(4)进行实验①~⑤的目的是
【反思与评价】
(5)实验1中,需要控制的实验条件是:试样与柿皮(含水量2.6%)质量比为4:1、熏硫时间2h和
(6)某同学认为“在制作柿饼时,熏硫时间越长,控制霉变效果越好”,你是否同意此观点,并说明理由
您最近一年使用:0次



