空气中氧气含量测定的再认识。
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图1),写出红磷燃烧的符号表达式:_____ 。兴趣小组用该方法测出的氧气含量常远远低于 21%。

【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)_____ ,装置内氧气有剩余;……
【实验探究1】小明查阅资料知铁在潮湿的空气中能与氧气和水反应生成铁锈。根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图2),通过7天测得的数据计算空气中氧气的含量为19.13%。
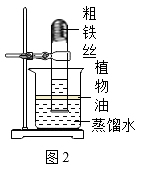
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点有:_____ (答案合理即可)。
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图3),8分钟后测得的数据如表:

请计算出空气中氧气含量_____ (计算结果保留一位小数)。
【结论与反思】通过上述实验探究,选择_____ (填物质名称 )进行实验,可较为快速地完成实验并减小实验误差。
【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图2装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由:_____ (填“能”或“否”);_____ 。
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图1),写出红磷燃烧的符号表达式:

【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)
【实验探究1】小明查阅资料知铁在潮湿的空气中能与氧气和水反应生成铁锈。根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图2),通过7天测得的数据计算空气中氧气的含量为19.13%。

【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点有:
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图3),8分钟后测得的数据如表:
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 131 mL | 90.0 mL | 63.6 mL |

请计算出空气中氧气含量
【结论与反思】通过上述实验探究,选择
【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图2装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由:
更新时间:2020-10-18 18:22:09
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】空气中氧气含量测定的再认识.






(1)【经典赏析】拉瓦锡用定量的方法研究空气的成分(实验装置如图1).
该实验中选择使用汞的优点有____________
A.实验过程中没有污染
B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封的作用
D.生成的化合物加热分解又能得到汞和氧气
(2)【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的符号表达式________________ 。图2中集气瓶底部的水的作用为_________ 。(填字母)
A.吸收有害物质 B.降温,快速冷却 C.保护瓶底
但是用该方法测出的氧气含量常常低于21%。
(3)【提出问题】用该方法测出的氧气含量为什么低于21%?
【进行猜想】①____________ ;②____________ ,装置内氧气有剩余;
(4)【实验与交流】为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是_____ (填“温度”或“氧气的浓度”);
【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是_______________ ;
(5)【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为________________ ,一般不能在空气中燃烧,因此无法用铁丝代替红磷进行该实验。小明根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点____ (填字母)。
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(6)【实验探究2】小明利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:请计算出空气中氧气含量________ (计算结果保留一位小数)。相对于实验探究1,实验探究2改进的目的是_______________________ 。
(7) 【拓展延伸】铜能与空气中氧气、水、二氧化碳反应生成铜绿[其主要成分为:
Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,能否比较准确地测定空气中氧气的含量_____________ ,理由____________ (填字母)
A.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
B.铜丝反应比铁丝快
C.反应更彻底






(1)【经典赏析】拉瓦锡用定量的方法研究空气的成分(实验装置如图1).
该实验中选择使用汞的优点有
A.实验过程中没有污染
B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封的作用
D.生成的化合物加热分解又能得到汞和氧气
(2)【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的符号表达式
A.吸收有害物质 B.降温,快速冷却 C.保护瓶底
但是用该方法测出的氧气含量常常低于21%。
(3)【提出问题】用该方法测出的氧气含量为什么低于21%?
【进行猜想】①
(4)【实验与交流】为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是
【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是
(5)【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(6)【实验探究2】小明利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:请计算出空气中氧气含量
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
131mL | 90.0mL | 63.6mL |
Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,能否比较准确地测定空气中氧气的含量
A.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
B.铜丝反应比铁丝快
C.反应更彻底
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某兴趣小组开展“测定密闭容器中某种气体的体积分数”的探究实验。
【实验1】按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。

(1)实验1中,红磷燃烧的主要现象是_______ 。红磷熄灭后,集气瓶冷却至室温,打开K,水能倒吸入集气瓶的原因是_______ 。
【实验2】利用图2甲装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度随时间的变化趋势如图乙所示。

(2)根据图2乙中所测氧气浓度的变化趋势,下列说法正确的是_______ 。
A 反应结束后容器内的氧气已全部被消耗
B 红磷有剩余的原因是容器内氧气的体积分数小于一定值时,红磷无法继续燃烧
C t2后氧气浓度略微上升的原因之一是因为止水夹右侧导管中的空气进入了集气瓶中
(3)根据图2乙所测的压强变化曲线,解释AB段气体压强变化的原因是_______ 。
(4)若用实验1的装置进行实验,需要寻找红磷的替代物,该替代物应满足的条件___ (写两点)。
【实验1】按图1所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。

(1)实验1中,红磷燃烧的主要现象是
【实验2】利用图2甲装置测定空气中氧气的含量并结合现代传感器技术,测得过程中容器内气体压强、温度、氧气浓度随时间的变化趋势如图乙所示。

(2)根据图2乙中所测氧气浓度的变化趋势,下列说法正确的是
A 反应结束后容器内的氧气已全部被消耗
B 红磷有剩余的原因是容器内氧气的体积分数小于一定值时,红磷无法继续燃烧
C t2后氧气浓度略微上升的原因之一是因为止水夹右侧导管中的空气进入了集气瓶中
(3)根据图2乙所测的压强变化曲线,解释AB段气体压强变化的原因是
(4)若用实验1的装置进行实验,需要寻找红磷的替代物,该替代物应满足的条件
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】建构合理的思维模型,既能促进深度学习,又能提高思维品质。小科建构了“两组分混合物含量测定”的思维模型。

运用该模型对教材中“测定空气中氧气含量”的实验进行了再探究:忽略含量很低的其它物质,空气可以看成由氮气和氧气组成的两组分混合物。
【探究一】根据沸点低的组分先汽化的性质,测定混合物中某组分的含量。
(1)将空气转变为液态空气,液氮先汽化。从建模角度分析,该操作属于上述思维模型中的______ 。
【探究二】根据混合物中某组分发生化学反应,测定混合物中某组分的含量。
(2)按图甲装置测定空气中氧气含量时,止水夹最合理的打开时间是______ (填“反应刚结束时”或“冷却到室温时”)。该实验中,红磷要足量的目的是______ ,红磷燃烧的文字表达式为______ 。

【交流评价】(3)已知:在空气中点燃石蜡,会生成水和二氧化碳等物质。小科用足量石蜡替换红磷,规范操作后,测得的氧气含量将______ (填“偏大”、“偏小”或“不变”)。
【继续探究】(4)运用上述思维模型,小科又设计了图乙的实验装置,简述其“测定空气中氧气含量”的原理______ 。

运用该模型对教材中“测定空气中氧气含量”的实验进行了再探究:忽略含量很低的其它物质,空气可以看成由氮气和氧气组成的两组分混合物。
【探究一】根据沸点低的组分先汽化的性质,测定混合物中某组分的含量。
(1)将空气转变为液态空气,液氮先汽化。从建模角度分析,该操作属于上述思维模型中的
【探究二】根据混合物中某组分发生化学反应,测定混合物中某组分的含量。
(2)按图甲装置测定空气中氧气含量时,止水夹最合理的打开时间是

【交流评价】(3)已知:在空气中点燃石蜡,会生成水和二氧化碳等物质。小科用足量石蜡替换红磷,规范操作后,测得的氧气含量将
【继续探究】(4)运用上述思维模型,小科又设计了图乙的实验装置,简述其“测定空气中氧气含量”的原理
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
【推荐1】金属的性质和应用是化学研究的重要课题。
【知识回顾】
(1)铁丝在潮湿的空气中会慢慢锈蚀,是铁与___________ (填化学式)等物质作用的过程。
【实验探究】(以下实验均在室温和1标准大气压的环境中进行)制作暖宝宝要用到铁粉、活性炭、氯化钠等物质。
【实验1】
(2)如图1所示,称取2.0g铁粉和2.5g活性炭,搅拌均匀,用滤纸包好,再滴入约1mL溶质质量分数为5%的氯化钠溶液,迅速用温度传感器测量,实验进行到450s时搓揉一次滤纸包使表面结块的混合物松散,实验过程中测得混合物温度随时间变化的曲线如图2所示。


图中450s后混合物温度继续升高的原因是___________ 。
无烟食品加热剂(内装有镁粉、铁粉和氯化钠等化学品)常用于野外加热食物,使用时向化学品中加入一定量的水,能迅速反应升温使水沸腾,对食物进行加热。
【实验2】
(3)向加有100mL水的隔热容器中分别加入下表各组物质,连续搅拌,每50s记录一次温度,测得温度变化曲线如图3所示。
①分析上述实验可以发现影响镁和水反应速率的因素是___________ 。
②无烟食品加热剂的成分不能用于制作暖宝宝的理由是___________ 。
③在实验2基础上,要证明温度升高的主要原因是镁参与了反应,请你设计实验方案描述实验现象及结论___________ 。
【实验3】
化学兴趣小组按如图(见图4)所示装置进行实验,瓶中的氧气可以几乎耗尽,测得实验数据如下表所示。

(4)铜能与空气中氧气、水和二氧化碳反应而锈蚀,生成铜绿,若将如图装置中的铁粉换成足量的铜粉进行实验,能否比较准确地测定空气中氧气的含量,你的判断和理由是___________ 。
【知识回顾】
(1)铁丝在潮湿的空气中会慢慢锈蚀,是铁与
【实验探究】(以下实验均在室温和1标准大气压的环境中进行)制作暖宝宝要用到铁粉、活性炭、氯化钠等物质。
【实验1】
(2)如图1所示,称取2.0g铁粉和2.5g活性炭,搅拌均匀,用滤纸包好,再滴入约1mL溶质质量分数为5%的氯化钠溶液,迅速用温度传感器测量,实验进行到450s时搓揉一次滤纸包使表面结块的混合物松散,实验过程中测得混合物温度随时间变化的曲线如图2所示。


图中450s后混合物温度继续升高的原因是
无烟食品加热剂(内装有镁粉、铁粉和氯化钠等化学品)常用于野外加热食物,使用时向化学品中加入一定量的水,能迅速反应升温使水沸腾,对食物进行加热。
【实验2】
(3)向加有100mL水的隔热容器中分别加入下表各组物质,连续搅拌,每50s记录一次温度,测得温度变化曲线如图3所示。
| 组别 | 物质 |
| Ⅰ | 2.4g的整根镁条、2.8g铁粉、5.85gNaCl粉末 |
| Ⅱ | 2.4g镁条剪成100份、2.8g铁粉、5.85gNaCl粉末 |
| Ⅲ | 2.4g镁粉、2.8g铁粉、5.85gNaCl粉末 |
②无烟食品加热剂的成分不能用于制作暖宝宝的理由是
③在实验2基础上,要证明温度升高的主要原因是镁参与了反应,请你设计实验方案描述实验现象及结论
【实验3】
化学兴趣小组按如图(见图4)所示装置进行实验,瓶中的氧气可以几乎耗尽,测得实验数据如下表所示。

| 测量项目 | 实验前 | 实验后 | |
| 集气瓶(扣除内容物)和导管的容积 | 烧杯中水的体积 | 烧杯中水的体积 | |
| 体积/mL | 131.0 | 90.0 | 63.6 |
(4)铜能与空气中氧气、水和二氧化碳反应而锈蚀,生成铜绿,若将如图装置中的铁粉换成足量的铜粉进行实验,能否比较准确地测定空气中氧气的含量,你的判断和理由是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】在“空气中氧气含量的测定”实验探究中,甲同学设计了如下实验方案:

在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温。打开铁夹,水注入集气瓶。(实验装置如图所示)回答下列问题:
(1)实验过程中涉及到的化学反应的符号表达式是______ 通过该实验还能得出氮气的性质有______ 、______ 。
(2)若实验操作规范,该实验得出的结论是______ 。
(3)该方法测定的结果偏小的可能原因是______ (填序号)。
①红磷量不足②装置气密性不好③弹簧夹没有加紧④没有冷却到室温
某学习小组的同学对甲同学的实验方案开展进一步探究:
[提出问题〕
①可用于“空气中氧气含量测定实验”的药品只能是红磷吗?什么样的药品可以作为该实验的反应物?
②可用于“空气中氧气含量测定实验”的装置除了课本中提及的,还有其它装置吗?
③改进装置和药品,能使一些在一般条件下不能用于测定空气含量的物质也能测定氧气的含量吗?
[作出猜想]
猜想1一定还可用其它的物质测定空气中氧气含量,如镁条。
猜想2可用于“空气中氧气含量测定实验”的装置不止这一种,但都须满足一定的条件。
[查阅资料]
刘小源同学查阅资料获知:
(1)“镁在空气中燃烧不仅与氧气反应,还与氮气和二氧化碳反应”;
(2)铁丝在潮湿的空气中会生锈;
(3)“引火铁”(极细的铁粉)是一种准纳米材料,这种铁粉具有很高的反应活性,它在空气中受热很容易燃烧;
(4)白磷与红磷的化学性质有相似之处,白磷在40℃左右便能燃烧,红磷在240℃才能燃烧。
【分析论证】刘小源同学觉得如果用蜡烛、硫粉、木炭在空气中燃烧做此实验将产生很大误差,理由是______ 。李雨欣同学觉得用铁丝也不行,理由是______ 。根据刘小源同学查阅的资料,若用镁条代替红磷,测得的氧气的体积含晕应该______ (填"大于"或"小于”"等于”)空气体积的1/5。
【得出结论】根据刘小源同学查阅的资料及上述分析,请归纳:在测定空气中氧气含量的实验中,应考虑所用药品和生成物应满足以下的条件:
①______ ②______ 。
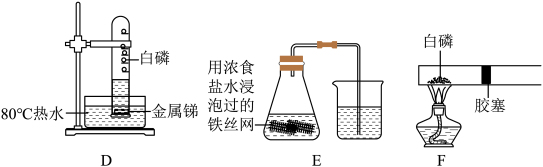
【反思改进】李雨欣同学根据查阅到的不同装置,结合刘小源同学查阅的资料与分析,设计了如下实验方案(包括装置及药品);其中,不适宜在较短时间内测得空气中氧气含量的一种方案是______ (填字母序号),理由______ 。在其余的五种实验方案中,有一个装置可能因为受热不均导致装置损坏或气体外逸,该装置是______ (填字母序号)。其余改进方案共同的优点是:______ 。


在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温。打开铁夹,水注入集气瓶。(实验装置如图所示)回答下列问题:
(1)实验过程中涉及到的化学反应的符号表达式是
(2)若实验操作规范,该实验得出的结论是
(3)该方法测定的结果偏小的可能原因是
①红磷量不足②装置气密性不好③弹簧夹没有加紧④没有冷却到室温
某学习小组的同学对甲同学的实验方案开展进一步探究:
[提出问题〕
①可用于“空气中氧气含量测定实验”的药品只能是红磷吗?什么样的药品可以作为该实验的反应物?
②可用于“空气中氧气含量测定实验”的装置除了课本中提及的,还有其它装置吗?
③改进装置和药品,能使一些在一般条件下不能用于测定空气含量的物质也能测定氧气的含量吗?
[作出猜想]
猜想1一定还可用其它的物质测定空气中氧气含量,如镁条。
猜想2可用于“空气中氧气含量测定实验”的装置不止这一种,但都须满足一定的条件。
[查阅资料]
刘小源同学查阅资料获知:
(1)“镁在空气中燃烧不仅与氧气反应,还与氮气和二氧化碳反应”;
(2)铁丝在潮湿的空气中会生锈;
(3)“引火铁”(极细的铁粉)是一种准纳米材料,这种铁粉具有很高的反应活性,它在空气中受热很容易燃烧;
(4)白磷与红磷的化学性质有相似之处,白磷在40℃左右便能燃烧,红磷在240℃才能燃烧。
【分析论证】刘小源同学觉得如果用蜡烛、硫粉、木炭在空气中燃烧做此实验将产生很大误差,理由是
【得出结论】根据刘小源同学查阅的资料及上述分析,请归纳:在测定空气中氧气含量的实验中,应考虑所用药品和生成物应满足以下的条件:
①
【反思改进】李雨欣同学根据查阅到的不同装置,结合刘小源同学查阅的资料与分析,设计了如下实验方案(包括装置及药品);其中,不适宜在较短时间内测得空气中氧气含量的一种方案是


您最近一年使用:0次
【推荐3】小明利用图1装置探究物质在空气中燃烧后氧气浓度变化(已知:白磷的着火点是40℃,红磷的着火点是240℃),图2是用传感器测量整个实验过程中烧瓶内氧气浓度变化情况的曲线。
步骤1:用激光笔照射燃烧匙中足量的红磷,红磷燃烧,一段时间后熄灭,白磷始终不燃烧。
步骤2:冷却至室温,将装有白磷的燃烧匙提出水面,用激光笔照射引燃白磷,白磷燃烧。

(1)在步骤1中反应的符号表达式为________ ,图2哪一段表示红磷的燃烧_______ (填AB、BC、CD或DE):你认为“测定空气中氧气的含量”,选择________ (填“红磷”或“白磷”)效果会更好,理由是_________ 。
(2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。用图2装置进行测定空气氧气含量的实验。数据如下表:
①脱氧剂发生复杂的化学反应,首先是铁粉与氧气,水反应生成氢氧化亚铁【Fe(OH)2】固体。
②实验过程中量筒中的液面不断下降,水被吸入瓶中,出现该现象的原因是________ 。
③通过脱氧剂实验测得的空气中氧气的体积分数为________ 。
步骤1:用激光笔照射燃烧匙中足量的红磷,红磷燃烧,一段时间后熄灭,白磷始终不燃烧。
步骤2:冷却至室温,将装有白磷的燃烧匙提出水面,用激光笔照射引燃白磷,白磷燃烧。

(1)在步骤1中反应的符号表达式为
(2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。用图2装置进行测定空气氧气含量的实验。数据如下表:
| 所需要的时间/s | 0 | 5 | 10 | 30 | 35 | 45 |
| 量筒中液面的刻度/mL | 50 | 35 | 27.5 | 19.7 | 19.7 | 19.7 |
②实验过程中量筒中的液面不断下降,水被吸入瓶中,出现该现象的原因是
③通过脱氧剂实验测得的空气中氧气的体积分数为
您最近一年使用:0次



