阅读下面科普短文。
氢能是公认的高热值清洁能源。目前,氢气的来源如如图1所示。
化石资源制氢最为成熟。水煤气变换反应: ,是化石资源制氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
,是化石资源制氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国“人造太阳”大科学装置“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题:
(1)目前最清洁的能源是________ 。
(2)如图2中,催化剂为2%Au/a-MoC时,CO转化率和温度的关系是__________ 。
(3)根据下表信息可知氘、氚都属于氢元素,理由是____________ 。
(4)下列说法正确的是___________ (填字母)。
Aa-MoC可使CO转化率接近100%
B水电解制氢的不足是造价高昂
C利用太阳能制氢是未来的发展方向
D“东方超环”利用核聚变提供能量
氢能是公认的高热值清洁能源。目前,氢气的来源如如图1所示。
化石资源制氢最为成熟。水煤气变换反应:
 ,是化石资源制氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
,是化石资源制氢过程中的重要反应之一。北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国“人造太阳”大科学装置“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题:
(1)目前最清洁的能源是
(2)如图2中,催化剂为2%Au/a-MoC时,CO转化率和温度的关系是
(3)根据下表信息可知氘、氚都属于氢元素,理由是
| 原子种类 | 质子数 | 中子数 | 核外电子数 |
| 氘 | 1 | 1 | 1 |
| 氚 | 1 | 2 | 1 |
Aa-MoC可使CO转化率接近100%
B水电解制氢的不足是造价高昂
C利用太阳能制氢是未来的发展方向
D“东方超环”利用核聚变提供能量
更新时间:2020-12-25 15:00:12
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】钠元素和镁元素的本质区别是_____ 不同;H2O和H2O2都是由氢元素和氧元素组成,但是化学性质不同,是因为_____ 不同。一定质量的某化合物完全燃烧,消耗9.6克氧气,生成8.8克二氧化碳和5.4克水,该化合物中氧元素和氢元素的原子个数比为_____ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】铝与铝的化合物有极其重要的用途。
(一)铝的存在
(1)铝是很活泼的金属,但铝制的炊具却耐腐蚀,其原因是___________ (用方程式表示)。
(2)使用铝制炊具会使人体摄入过量的“铝”,导致记忆力减退等不良症状。这里的“铝”是指___________ (填序号)。
A分子 B原子 C元素 D单质
(二)铝的利用:铝粒和生石灰、碳酸钠混合可制成发热包。
(3)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,放出大量的热,写出产生该现象的主要反应方程式___________ 。
(4)小明向使用后的发热包中加入稀盐酸,发现有气泡产生,于是他对产生的气体展开进一步探究。
【猜想与假设】小明认为该气体可能是a.H2;b.___________ ;c.H2和CO2的混合气体。
【实验设计】小明设计如图实验装置,对气体成分进行探究。

【实验验证】甲装置中的实验现象是___________ ,丁装置中黑色的粉末逐渐变为红色,试管口有水珠产生。证明猜想c正确。
若甲、乙装置交换位置,___________ (填“能”或“不能”)确定气体中含有CO2,写出化学方程式并说明理由___________ 。
(三)铝的化合物
硫酸铝铵晶体[NH4Al(SO4)2·xH2O]是一种用途广泛的含铝化合物。为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。

(5)固体甲是T1℃刚好完全失去结晶水的产物,则x=___________ 。(写出计算过程)
(6)T3℃时固体乙的成分是___________ (填字母)。
A Al(OH)3
B Al2(SO4)3
C Al2(SO4)3和Al(OH)3
(一)铝的存在
(1)铝是很活泼的金属,但铝制的炊具却耐腐蚀,其原因是
(2)使用铝制炊具会使人体摄入过量的“铝”,导致记忆力减退等不良症状。这里的“铝”是指
A分子 B原子 C元素 D单质
(二)铝的利用:铝粒和生石灰、碳酸钠混合可制成发热包。
(3)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,放出大量的热,写出产生该现象的主要反应方程式
(4)小明向使用后的发热包中加入稀盐酸,发现有气泡产生,于是他对产生的气体展开进一步探究。
【猜想与假设】小明认为该气体可能是a.H2;b.
【实验设计】小明设计如图实验装置,对气体成分进行探究。

【实验验证】甲装置中的实验现象是
若甲、乙装置交换位置,
(三)铝的化合物
硫酸铝铵晶体[NH4Al(SO4)2·xH2O]是一种用途广泛的含铝化合物。为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。

(5)固体甲是T1℃刚好完全失去结晶水的产物,则x=
(6)T3℃时固体乙的成分是
A Al(OH)3
B Al2(SO4)3
C Al2(SO4)3和Al(OH)3
您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
解题方法
【推荐3】阅读下列短文并回答问题。
安徽是豆腐的发源地。豆腐中含有丰富的蛋白质和钙,容易被人体消化吸收。但过量食用会阻碍人体对铁的吸收,且易出现腹胀、腹泻等症状。以大豆为原料制作豆腐的主要工序:选料、泡料、磨豆、滤
浆、煮浆、点浆、成型等,其中点浆是制作豆腐的关键工序。点浆时需要用到凝固剂,传统工艺制作豆腐用的是石膏(主要成分为硫酸钙)或盐卤(如氯化镁等),制作内酯豆腐用的是葡萄糖酸内酯。凝固剂添加量对豆腐的品质也有影响,将大豆泡发后,与水按1:4的比例磨成豆浆,以MgCl2为例,研究结果如图所示。_______ (填“元素”“原子”或“单质”)。
(2)豆腐的制作工序中主要发生化学变化的是_______ 。
(3)滤浆的过程是利用工具将磨浆产生的豆腐渣分离出去,该操作与化学实验中的_______ 操作作用相同。
(4)据图可知,MgCl2添加量与豆腐保水性的关系是_______ 。
(5)下列说法正确的是_______(填字母序号)。
安徽是豆腐的发源地。豆腐中含有丰富的蛋白质和钙,容易被人体消化吸收。但过量食用会阻碍人体对铁的吸收,且易出现腹胀、腹泻等症状。以大豆为原料制作豆腐的主要工序:选料、泡料、磨豆、滤
浆、煮浆、点浆、成型等,其中点浆是制作豆腐的关键工序。点浆时需要用到凝固剂,传统工艺制作豆腐用的是石膏(主要成分为硫酸钙)或盐卤(如氯化镁等),制作内酯豆腐用的是葡萄糖酸内酯。凝固剂添加量对豆腐的品质也有影响,将大豆泡发后,与水按1:4的比例磨成豆浆,以MgCl2为例,研究结果如图所示。

(2)豆腐的制作工序中主要发生化学变化的是
(3)滤浆的过程是利用工具将磨浆产生的豆腐渣分离出去,该操作与化学实验中的
(4)据图可知,MgCl2添加量与豆腐保水性的关系是
(5)下列说法正确的是_______(填字母序号)。
| A.点浆时用到的石膏属于混合物 |
| B.多吃豆腐对身体无害 |
| C.MgCl2添加得越多,豆腐的产率越高 |
| D.豆腐是人体补充蛋白质的来源之一 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】氢气作为新能源的优点是____ (答出一条即可);甲烷是常用的燃料之一,甲烷完全燃烧的化学方程式为____ ;一定量的乙醇在氧气不充足的情况下,燃烧生成2.7g水、2.2g二氧化碳和一定质量的一氧化碳,则该反应方程式为____ 。
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】A是常见金属单质,B、C是非金属单质,且C是密度最小的气体,甲是磁铁矿的主要成分,乙是无色液体,它们之间有如下的转化关系(部分产物和反应条件未标明).

(1)推断C、甲、乙的化学式为:C__________ ,甲 __________ ,乙 __________ ;
(2)写出反应①的化学方程式_________________________________________ ,C作为能源除了具有放出热量多,原料不受限制的优点外,还有 _____________ 的优点.

(1)推断C、甲、乙的化学式为:C
(2)写出反应①的化学方程式
您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
名校
解题方法
【推荐3】阅读下面科普短文。

氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。化石资源制氢最为成熟。水煤气变换反应:CO+H2O CO2+H2,是化石资源制氢过程中的重要反应之一、北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
CO2+H2,是化石资源制氢过程中的重要反应之一、北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国的“人造太阳”—“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。
除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是_______
(2)图2中,催化剂为2%Au/a-MoC时,CO转化率和温度的关系是_______
(3)根据下表信息可知氘、氚都属于氢元素,理由是_______
(4)下列说法正确的是_______(填序号)。

氢能是公认的高热值清洁能源。目前,氢气的来源如图1所示。化石资源制氢最为成熟。水煤气变换反应:CO+H2O
 CO2+H2,是化石资源制氢过程中的重要反应之一、北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。
CO2+H2,是化石资源制氢过程中的重要反应之一、北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国的“人造太阳”—“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。
除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。
依据文章内容回答下列问题。
(1)目前氢气的主要来源是
(2)图2中,催化剂为2%Au/a-MoC时,CO转化率和温度的关系是
(3)根据下表信息可知氘、氚都属于氢元素,理由是
(4)下列说法正确的是_______(填序号)。
| A.a-MoC可使CO转化率接近100% |
| B.水电解制氢的不足主要是造价高昂 |
| C.利用太阳能制氢是未来发展方向 |
| D.“东方超环”利用核聚变提供能量 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】乙醇汽油是一种新型替代能源,它是由90%的普通汽油与10%的燃料乙醇调和而成的。写出乙醇完全燃烧的化学方程式:______ 。现将一定量乙醇和氧气置于密闭容器中点燃恰好完全反应,产物为二氧化碳、一氧化碳和水,待恢复到室温,测得混合气体中碳元素占30%,则参加反应的氧气与生成的水的质量比为______ 。
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。
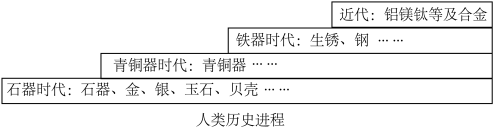
(1)金、银在自然界有单质形式存在,说明他们的化学性质都___________ 。
(2)在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
①)比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是___________ 。
②近代工业上采用电解熔融氧化铝(A12O3)的方法治炼铝,A12O3分解后得到两种单质,该反应的化学方程式为_______ 。
(3)镁铝合金被誉为“21世纪绿色金属结构材料”。一种镁铝合金Mg17A112是特殊的储氢材料,完全吸收氢气后得到MgH2和A1,该反应的化学方程式为______ 。
(4)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其________(填字母序号)非常好。
(5)铁在潮湿的空气中反应生成疏松的铁锈。已知: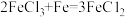 铁锈的主要成分是
铁锈的主要成分是__________ (填化学式):将生锈的铁制品放入一定量的稀盐酸中充分反应,变化过程中最多涉及_______ 种化学反应基本类型。
(6)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有________(填字母序号)。

(1)金、银在自然界有单质形式存在,说明他们的化学性质都
(2)在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
①)比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是
②近代工业上采用电解熔融氧化铝(A12O3)的方法治炼铝,A12O3分解后得到两种单质,该反应的化学方程式为
(3)镁铝合金被誉为“21世纪绿色金属结构材料”。一种镁铝合金Mg17A112是特殊的储氢材料,完全吸收氢气后得到MgH2和A1,该反应的化学方程式为
(4)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其________(填字母序号)非常好。
| A.可塑性 | B.机械性能 | C.抗腐蚀性能 |
(5)铁在潮湿的空气中反应生成疏松的铁锈。已知:
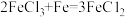 铁锈的主要成分是
铁锈的主要成分是(6)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有________(填字母序号)。
| A.金属原料的成本 |
| B.生成过程中的能耗和污染 |
| C.金属的回收利用 |
您最近一年使用:0次
【推荐3】能源和环境一直受到人们关注。
(1)太阳能和天然气中属于可再生能源的是___________ ;为方便贮存和运输,天然气通常被压缩到容积很小的钢瓶中,而可燃冰却很难被压缩。试从分子的角度分析,其中的原因是____________________ 。
(2)造成大气中CO2含量增加的主要原因是___________ 。(填序号)
a 动植物的呼吸作用 b 实验室逸出CO2 c 化石燃料的大量燃烧
(3)汽车尾气中的CO和NO,在催化剂作用下能转化为CO2和N2,该反应中CO和NO的分子个数比为___________ 。
(4)为减少污染、提高煤的利用率,可在高温条件下将煤转化为可燃性气体,此过程的微观示意图如图所示,该反应的化学方程式为___________________ 。

(5)可燃冰作为新型能源,相比传统化石燃料具有很多优势,主要是_______________ (填序号)。
A 储量丰富
B 燃烧值大
C 清洁、无污染
D 易于开采
(1)太阳能和天然气中属于可再生能源的是
(2)造成大气中CO2含量增加的主要原因是
a 动植物的呼吸作用 b 实验室逸出CO2 c 化石燃料的大量燃烧
(3)汽车尾气中的CO和NO,在催化剂作用下能转化为CO2和N2,该反应中CO和NO的分子个数比为
(4)为减少污染、提高煤的利用率,可在高温条件下将煤转化为可燃性气体,此过程的微观示意图如图所示,该反应的化学方程式为

(5)可燃冰作为新型能源,相比传统化石燃料具有很多优势,主要是
A 储量丰富
B 燃烧值大
C 清洁、无污染
D 易于开采
您最近一年使用:0次
【推荐1】人类在向大自然获取物质和能源的过程中,对物质的循环产生影响。由于人类过度开采使用地下碳(主要是化石燃料),打破了大气中二氧化碳的平衡。2020年9月中国宣布:力争CO2的排放在2030年前实现“碳达峰”。
(1)捕集、利用和封存CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为____________ 。
(2)利用催化剂将废气中的二氧化碳转化为燃料X,是实现碳中和的另一路径。该反应的化学方程式为 ,X的化学式为
,X的化学式为____________ 。
(3)低碳冶金:氢基熔融冶金技术是利用氢作为还原剂代替碳还原剂,从而实现减少CO2排放的目的,实现低碳冶金,氢基熔融还原生产高纯铸造生铁的主要流程如下图:

①燃烧区的作用是______ ,燃烧区发生燃烧反应的物质还有_______ 。(填化学式)
②还原区的反应除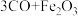

 ,另一主要反应的化学方程式是
,另一主要反应的化学方程式是_______ 。
③从环境保护角度,与高炉炼铁技术相比,氢基熔融冶金技术的优点____________ 。
(4)氢能源的开发:如图是利用ZnO和Fe2O3为催化剂制取氢气的一种方法。“循环制氢体系”涉及的能量转化是由太阳能转化为_______ 能,请写出该体系制取氢气的化学方程式______ 。

(5)超临界CO2是指温度与压强达到一定值时,CO2形成气态与液态交融在一起的流体,超临界CO2流体和水相似,溶解能力强,被誉为“绿色环保溶剂”。超临界CO2流体的说法正确的是 。(填序号)
(1)捕集、利用和封存CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为
(2)利用催化剂将废气中的二氧化碳转化为燃料X,是实现碳中和的另一路径。该反应的化学方程式为
 ,X的化学式为
,X的化学式为(3)低碳冶金:氢基熔融冶金技术是利用氢作为还原剂代替碳还原剂,从而实现减少CO2排放的目的,实现低碳冶金,氢基熔融还原生产高纯铸造生铁的主要流程如下图:

①燃烧区的作用是
②还原区的反应除
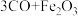

 ,另一主要反应的化学方程式是
,另一主要反应的化学方程式是③从环境保护角度,与高炉炼铁技术相比,氢基熔融冶金技术的优点
(4)氢能源的开发:如图是利用ZnO和Fe2O3为催化剂制取氢气的一种方法。“循环制氢体系”涉及的能量转化是由太阳能转化为

(5)超临界CO2是指温度与压强达到一定值时,CO2形成气态与液态交融在一起的流体,超临界CO2流体和水相似,溶解能力强,被誉为“绿色环保溶剂”。超临界CO2流体的说法正确的是 。(填序号)
| A.它是混合物 | B.它的化学性质与普通二氧化碳相同 |
| C.它的分子不再运动 | D.它可代替许多有害、有毒、易燃的溶剂 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E分别表示初中化学常见的五种物质,它们的部分反应和转化关系如图所示(“﹣”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及条件)。

(1)若图中所示只有两种物质是氧化物,E是黑色粉末,B、D是组成元素相同物质,B物质的化学式为______ :写出D→A的化学方程式是______ 。
(2)若E、B是组成元素相同的物质,且为氧化物,A、D是气体,C可作实验室常见液态燃料,则E的化学式是______ ,C物质燃烧的化学方程式是______ 。

(1)若图中所示只有两种物质是氧化物,E是黑色粉末,B、D是组成元素相同物质,B物质的化学式为
(2)若E、B是组成元素相同的物质,且为氧化物,A、D是气体,C可作实验室常见液态燃料,则E的化学式是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐3】煤是重要的能源,也是生产化工产品的重要原料。随着人类社会的飞速发展,化石能源大量消耗,人类已经面临较严重的能源危机。为此,提高能源的利用率和开发更多的新能源显得相当重要。下图是煤化工产业链的一部分。
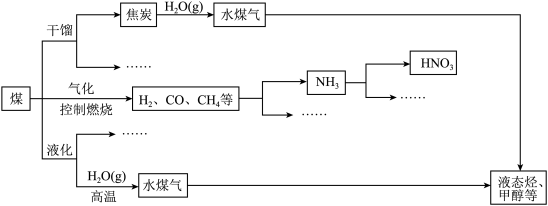
请回答:
(1)任意列举两种新能源______ ;
(2)上述处理煤的过程属于______ (选填“物理”或“化学”)变化。
(3)煤和石油等化石燃料燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通入含有长石(地壳中最常见的矿石,含量高达60)成分的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,则X的名称是______ ;
(4)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
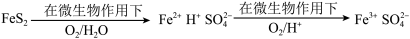
这种脱硫技术称为微生物脱硫技术。该技术的两步反应的化学方程式依次是:______ 。
(5)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ[n(O2)/n(NH3)]=1.25,实际生产要将γ值维护在1.7 ~2.2之间,原因是________ 。
[温馨提示:n(O2)可以认为是表示氧气分子堆积数目的一种物理量,即n(O2)值越大,说明氧分子数目越多]


请回答:
(1)任意列举两种新能源
(2)上述处理煤的过程属于
(3)煤和石油等化石燃料燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通入含有长石(地壳中最常见的矿石,含量高达60)成分的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,则X的名称是
(4)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
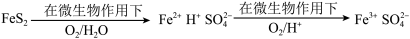
这种脱硫技术称为微生物脱硫技术。该技术的两步反应的化学方程式依次是:
(5)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ[n(O2)/n(NH3)]=1.25,实际生产要将γ值维护在1.7 ~2.2之间,原因是
[温馨提示:n(O2)可以认为是表示氧气分子堆积数目的一种物理量,即n(O2)值越大,说明氧分子数目越多]

您最近一年使用:0次



