人类的日常生活以及工农业生产离不开能源。
(1)煤、石油、天然气是常见的化石燃料,请写出天然气中主要成分(甲烷)燃烧的化学方程式_____ 。化石燃料大量燃烧,会排放出较多温室气体,引起环境问题。
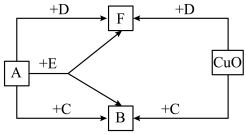
(2)为减少温室气体二氧化碳的排放,可以在催化剂条件下将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题:
①该反应中涉及到的氧化物有_____ (填序号)。
②在反应中C与D质量比为_____ 。
(3)为了解决能源危机,需开发新能源,其中氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图:
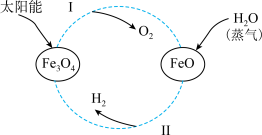
①反应Ⅰ的基本反应类型为_____ 。
②写出在一定条件下发生的反应Ⅱ的化学方程式:_____ 。
③在上述循环过程中,最终得到的产品是_____ 。
(1)煤、石油、天然气是常见的化石燃料,请写出天然气中主要成分(甲烷)燃烧的化学方程式
(2)为减少温室气体二氧化碳的排放,可以在催化剂条件下将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题:
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  | 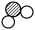 | 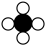 | |
②在反应中C与D质量比为
(3)为了解决能源危机,需开发新能源,其中氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图:

①反应Ⅰ的基本反应类型为
②写出在一定条件下发生的反应Ⅱ的化学方程式:
③在上述循环过程中,最终得到的产品是
20-21九年级上·江苏无锡·阶段练习 查看更多[4]
江苏省无锡市江阴市第一初级中学2020-2021学年九年级上学期12月月考化学试题(A卷)江苏省无锡市江阴市第一初级中学2020-2021学年九年级上学期12月月考化学试题(B卷)2023年河北省秦皇岛市卢龙县中考一模化学试题(已下线)2024年中考风向标-河北-质量守恒定律与微观示意图
更新时间:2021-01-07 13:14:15
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如图(部分产物略去):
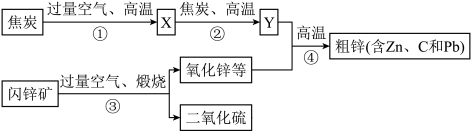
(1)X的化学式是__________ ,Y的名称是_________ ;图中①用过量空气的目的是_______________ ;
(2)①~④中属于化合反应的是________________ ;
(3)Zn_____________ (填“能”或“不能”)与PbC12溶液反应。
(4)写出反应③中生成ZnO的化学方程式__________________ ;
(5)结合下表数据设计,从粗锌中分离出纯锌的方案是:_____________________ ;

(1)X的化学式是
(2)①~④中属于化合反应的是
(3)Zn
(4)写出反应③中生成ZnO的化学方程式
(5)结合下表数据设计,从粗锌中分离出纯锌的方案是:
| 物质 | Zn | Pb | C |
| 沸点℃ | 907 | 1749 | 4827 |
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
【推荐2】推断题:物质之间的转化关系如图所示,部分产物和反应条件已省去.
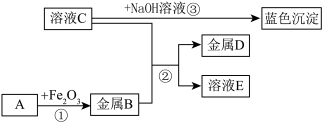
(1)金属B的活动性_____ 金属D的活动性(填“>”、“<”、“=”);
(2)若A是一种气体化合物,写出①的化学方程式:______________________ ;
(3)向C溶液中加入AgNO3溶液,有白色沉淀,加入稀硝酸,沉淀不溶解,写出其化学方程式__________________________________ ;
(4)写出溶液C与NaOH溶液反应的化学方程式:____________________ .

(1)金属B的活动性
(2)若A是一种气体化合物,写出①的化学方程式:
(3)向C溶液中加入AgNO3溶液,有白色沉淀,加入稀硝酸,沉淀不溶解,写出其化学方程式
(4)写出溶液C与NaOH溶液反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】活性氧化锌( )粒径介于1~100nm,是一种面向21世纪的新型高功能精细无机产品。某科研小组利用某废弃的氧化铜锌矿(主要成分为
)粒径介于1~100nm,是一种面向21世纪的新型高功能精细无机产品。某科研小组利用某废弃的氧化铜锌矿(主要成分为 和
和 ,其余成分既不与酸反应,也不溶解于水)回收铜,并制备活性氧化锌。
,其余成分既不与酸反应,也不溶解于水)回收铜,并制备活性氧化锌。
【查阅资料】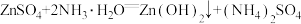 ;
;
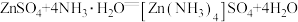 ;
;
常温下氢氧化物沉淀时溶液的pH见下表:
【实验设计】设计的部分实验流程如图所示:

请根据上述资料和实验流程回答下列问题:
(1)操作1的名称是____________ 。
(2)在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为_______________ 。
(3)加过量铁粉后,发生反应的基本反应类型是__________ ,得到滤渣1的成分为__________ 。
(4)加入双氧水的作用是___________ ;不选用高锰酸钾,而选用双氧水的优点是_______ 。
(5)完成操作2的实验步骤①___________ ;②_______ ;③灼烧。
【交流反思】(6)从绿色化学的角度分析上述实验流程,除了能回收金属单质和活性氧化锌外,还可以获取的有用副产品是(写出化学式,并指明其用途)________ 。
 )粒径介于1~100nm,是一种面向21世纪的新型高功能精细无机产品。某科研小组利用某废弃的氧化铜锌矿(主要成分为
)粒径介于1~100nm,是一种面向21世纪的新型高功能精细无机产品。某科研小组利用某废弃的氧化铜锌矿(主要成分为 和
和 ,其余成分既不与酸反应,也不溶解于水)回收铜,并制备活性氧化锌。
,其余成分既不与酸反应,也不溶解于水)回收铜,并制备活性氧化锌。【查阅资料】
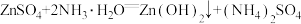 ;
;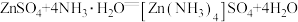 ;
;
常温下氢氧化物沉淀时溶液的pH见下表:
| 氢氧化物 |  |  |  |  |
| 开始沉淀时的pH | 1.9 | 7.0 | 6.0 | 4.7 |
| 沉淀完全时的pH | 3.2 | 9.0 | 8.0 | 6.7 |
【实验设计】设计的部分实验流程如图所示:

请根据上述资料和实验流程回答下列问题:
(1)操作1的名称是
(2)在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为
(3)加过量铁粉后,发生反应的基本反应类型是
(4)加入双氧水的作用是
(5)完成操作2的实验步骤①
【交流反思】(6)从绿色化学的角度分析上述实验流程,除了能回收金属单质和活性氧化锌外,还可以获取的有用副产品是(写出化学式,并指明其用途)
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,写出下列粒子模型所对应的分子名称:
”表示氧原子,写出下列粒子模型所对应的分子名称:
(1)
_____________ (2) 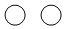
_______________
(3)
________________ (4) 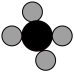
____________
 ”表示氢原子,用“
”表示氢原子,用“ ”表示碳原子,“
”表示碳原子,“ ”表示氧原子,写出下列粒子模型所对应的分子名称:
”表示氧原子,写出下列粒子模型所对应的分子名称:(1)

(3)


您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
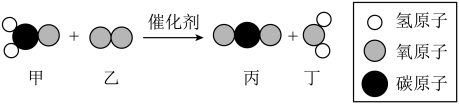
【推荐2】利用催化剂可消除室内装修材料释放的甲醛(CH2O),如图为该反应的微观示意图,则图中单质的化学式为_____ ;现有甲醛和乙醛蒸气( CH3CHO)的混合物共7.4g,完全燃烧后生成5.4gH2O和一定质量的CO2,则反应中一共消耗的氧气的质量为_____ g。

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】(1)①硫酸亚铁溶液中的阳离子符号为______ 。
②某粒子的结构示意图为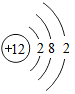 ,该粒子的符号为
,该粒子的符号为______ 。
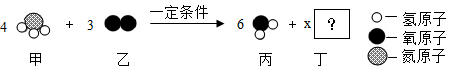
(2)如图所示某反应的微观示意图,则X的数值是______ ;改变反应条件,反应中乙、丙化学计量数之比变为5:6,则丁的化学式为______ 。
(3)向硝酸铜和硝酸镁的混合溶液中加入一定量铝粉和锌粉的混合物,充分反应后过滤,得滤渣A和蓝色滤液B,若向A中滴加稀盐酸,______ (选填“有”“没有”或“可能有”)气泡产生,B中一定含有的金属离子是______ 。
(4)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为______ (填序号)。
a.适量的盐酸 b.稍过量Na2CO3溶液 c.稍过量Ba(OH)2溶液
②某粒子的结构示意图为
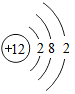 ,该粒子的符号为
,该粒子的符号为(2)如图所示某反应的微观示意图,则X的数值是

(3)向硝酸铜和硝酸镁的混合溶液中加入一定量铝粉和锌粉的混合物,充分反应后过滤,得滤渣A和蓝色滤液B,若向A中滴加稀盐酸,
(4)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为
a.适量的盐酸 b.稍过量Na2CO3溶液 c.稍过量Ba(OH)2溶液
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】能源“非石油化”是战略目标,发展以CH4、CO2等为原料的“C1化学”成为当今化工生产的必然趋势。通常天然气中含有H2S等有毒气体,下图为天然气合成氨的工艺流程。

(1)甲烷----氧气燃料电池是将______ 能转化为 ______ 能的装置。CH4在空气中燃烧时,将
干冷的小烧杯罩在火焰上方,可观察到烧杯内壁有______ 。
(2)CH4可合成多种无机物和有机物。研究CH4和CO2反应生成CO和H2,重大意义在于______ ;我国科研人员首先发现CH4可直接分解获得C6H6和H2,化学方程式为 ____________________________________________ 。
(3)①中CH4与H2O(气)反应生成CO2、H2,化学方程式是______ 。②中一般加入K2CO3溶液吸收CO2,此反应表示为K2CO3+CO2+H2O = 2 _________ ,N2 与H2按照分子数1: ____ 反应生成NH3。
(4)使用Fe2O3·H2O除去H2S,生成物中含硫元素的物质有______ 种。流程中参与循环的物质是 _______ (填化学式)。

(1)甲烷----氧气燃料电池是将
干冷的小烧杯罩在火焰上方,可观察到烧杯内壁有
(2)CH4可合成多种无机物和有机物。研究CH4和CO2反应生成CO和H2,重大意义在于
(3)①中CH4与H2O(气)反应生成CO2、H2,化学方程式是
(4)使用Fe2O3·H2O除去H2S,生成物中含硫元素的物质有
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】随着人类对能源的需求日益增长,开发和利用新能源成为越来越迫切的需求。请回答:
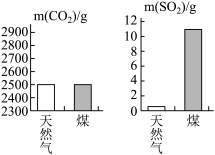
(1)目前,人类使用的燃料大多来自化石能源,如煤、石油、天然气,它们属于___________ (填“可再生”或“不可再生”)能源。
(2)充分燃烧1kg天然气和煤所产生的 和SO2气体的质量如图所示,则燃烧
和SO2气体的质量如图所示,则燃烧___________ 产生的气体更易导致酸雨。
(3)为缓解全球性能源危机,人们正积极开发和利用新能源。请举例一种新能源___________ 。
(4)甲烷是无色无味气体,密度比空气小,难溶于水。若在开采中甲烷气体大量泄漏于大气中,会造成严重的温室效应。除甲烷外,能造成温室效应的气体还有___________ (写一种即可)。
(5)一定甲烷(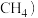 在氧气中不充分燃烧,生成二氧化碳,一氧化碳和水的分子个数之比可能为___________。
在氧气中不充分燃烧,生成二氧化碳,一氧化碳和水的分子个数之比可能为___________。

(1)目前,人类使用的燃料大多来自化石能源,如煤、石油、天然气,它们属于
(2)充分燃烧1kg天然气和煤所产生的
 和SO2气体的质量如图所示,则燃烧
和SO2气体的质量如图所示,则燃烧(3)为缓解全球性能源危机,人们正积极开发和利用新能源。请举例一种新能源
(4)甲烷是无色无味气体,密度比空气小,难溶于水。若在开采中甲烷气体大量泄漏于大气中,会造成严重的温室效应。除甲烷外,能造成温室效应的气体还有
(5)一定甲烷(
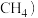 在氧气中不充分燃烧,生成二氧化碳,一氧化碳和水的分子个数之比可能为___________。
在氧气中不充分燃烧,生成二氧化碳,一氧化碳和水的分子个数之比可能为___________。A.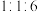 | B.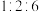 | C.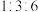 | D. |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐1】页岩气是蕴藏于页岩层可供开采的天然气资源,一种新开发的能源。
(1)页岩气的主要成分甲烷(CH4),则甲烷中碳元素的质量分数为:_____ 。
(2)页岩气做燃料,对于降低空气中SO2含量,解决酸雨污染具有重要作用。酸雨形成过程中,其中部分SO2会在一定条件下转化成SO3,其微观示意图如图
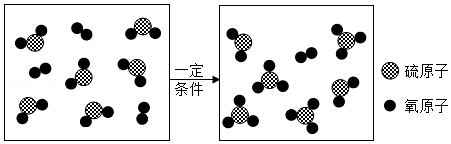
①该反应属于基本反应类型中的_____ 。
②反应消耗的O2与生成的SO3的分子数之比为_____ 。
(1)页岩气的主要成分甲烷(CH4),则甲烷中碳元素的质量分数为:
(2)页岩气做燃料,对于降低空气中SO2含量,解决酸雨污染具有重要作用。酸雨形成过程中,其中部分SO2会在一定条件下转化成SO3,其微观示意图如图

①该反应属于基本反应类型中的
②反应消耗的O2与生成的SO3的分子数之比为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】中国是最早使用天然气的国家,天然气的主要成分是甲烷。写出甲烷在空气中充分燃烧的化学方程式______ 。若甲烷不充分燃烧,可生成CO2、CO和H2O。现有一定质量的甲烷在密闭容器中燃烧后,生成4.4gCO2和5.6gCO,则同时生成H2O的质量为______ g。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】“碳中和”,中国在行动。“碳中和”是指一定时间内二氧化碳的排放量与吸收量基本相当。二氧化碳的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。
(1)2022年北京冬奥会采用二氧化碳制冷技术,实现二氧化碳循环利用,碳排放几乎为零。控制二氧化碳的排放,主要是为了减缓______ 效应。
(2)目前,人们使用的燃料大多来自化石燃料,如煤、______ 和天然气。天然气(主要成分CH4)充分燃烧的化学方程式是______ 。请列举一例可为实现“碳中和”做出贡献的清洁能源:______ 。
(3)工业生产中产生的二氧化碳经吸收剂处理可实现二氧化碳的捕集。
①加压水洗法可捕集二氧化碳,是因为______ 。用足量的石灰乳捕捉二氧化碳,反应的化学反应方程式是______ 。
②氧化钙可在较高温度下捕集二氧化碳,在更高温度下将捕集的二氧化碳释放利用。草酸钙晶体(CaC2O4•H2O)热分解可制备氧化钙,其加热升温过程中固体的质量变化见图。据图分析:第一阶段反应后固体质量减轻的原因是______ 。最终,该反应所得一氧化碳和二氧化碳的分子个数之比为______ 。已知CaCO3 CaO+CO2↑,与碳酸钙分解制备的氧化钙相比,草酸钙分解制备的氧化钙具有更好的二氧化碳捕集性能,其原因是
CaO+CO2↑,与碳酸钙分解制备的氧化钙相比,草酸钙分解制备的氧化钙具有更好的二氧化碳捕集性能,其原因是______ 。

(1)2022年北京冬奥会采用二氧化碳制冷技术,实现二氧化碳循环利用,碳排放几乎为零。控制二氧化碳的排放,主要是为了减缓
(2)目前,人们使用的燃料大多来自化石燃料,如煤、
(3)工业生产中产生的二氧化碳经吸收剂处理可实现二氧化碳的捕集。
①加压水洗法可捕集二氧化碳,是因为
②氧化钙可在较高温度下捕集二氧化碳,在更高温度下将捕集的二氧化碳释放利用。草酸钙晶体(CaC2O4•H2O)热分解可制备氧化钙,其加热升温过程中固体的质量变化见图。据图分析:第一阶段反应后固体质量减轻的原因是
 CaO+CO2↑,与碳酸钙分解制备的氧化钙相比,草酸钙分解制备的氧化钙具有更好的二氧化碳捕集性能,其原因是
CaO+CO2↑,与碳酸钙分解制备的氧化钙相比,草酸钙分解制备的氧化钙具有更好的二氧化碳捕集性能,其原因是
您最近一年使用:0次