某粗盐样品中含有杂质氯化镁、氯化钙。某同学设计了以下提纯方案:

请回答下列问题:
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的___ 。
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是__ 。
(3)滤液B中所含的溶质为__ 。
(4)向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为__ 时,应停止滴加,如果滴加的稀盐酸过量,对最后得到的精盐晶体的成分__ (填“有”或“没有”)影响。
(5)操作C的名称为__ 。
(6)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式_________ 。

请回答下列问题:
(1)方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的
(2)在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是
(3)滤液B中所含的溶质为
(4)向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为
(5)操作C的名称为
(6)工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式
2012·天津·中考真题 查看更多[11]
(已下线)2012年初中毕业升学考试(天津卷)化学(已下线)2013-2014山东省日照市初中学业水平模拟测试一化学试卷2017届天津市宝坻区九年级中考一模冲刺练习化学试卷鲁教版2018届九年级下册化学同步练习:期中测试辽宁省北镇市第一初级中学2019届九年级上学期期末考试化学试题辽宁省锦州市北镇一中2019届九年级上学期期末考试化学试题鲁教版九年级下册第八单元第二节 海水“晒盐”2018年天津市西青区中考二模化学试题山东省泰安市泰山学院附属中学2018届九年级下学期第二次模拟考试化学试题安徽省宣城市宣州区2019-2020学年九年级上学期“狸卫昝水雁裘”第四次六校联考化学试题2019年山东省日照市东港区北京路中学中考一模化学试题
更新时间:2019-01-30 18:14:09
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
【推荐1】(1)我国最大的盐场-------渤海湾长芦盐场,非常适合晒盐,海水晒盐的原理是__ 。
(2)某兴趣小组利用如下仪器进行粗盐提纯实验。
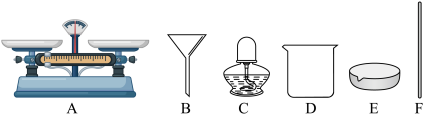
①写出下列仪器的名称: C_______ ,E_______ 。
②其具体操作步骤如下:
步骤一:溶解:用托盘天平称取经研钵研磨过的粗盐2.0g投入烧杯中,要对粗盐进行研磨的原因是__________________ 。
步骤二:过滤:组装一套过滤器,所需要的仪器除需要图中的仪器外还需要的仪器有_____ 。
将粗盐水分几次沿玻璃棒小心倒入漏斗内,玻璃棒所起的作用是_______ 。
观察滤纸上方和滤液情形,发现滤液呈浑浊状态,其原因可能是______ 。
步骤三:蒸发:搭建一套蒸发装置,将滤液倒入蒸发皿中,点燃酒精灯加热,并用玻璃棒轻轻搅拌,当_ ,时,撤去酒精灯。待冷却后,用玻璃棒将精盐拨到滤纸上再称量。
③提纯之后该兴趣小组计算的氯化钠的产率偏低,则可能的原因是_____ (填字母)。
A 溶解含有泥沙的粗盐时,搅拌时间不足
B 过滤时,液面高于滤纸边缘
C 蒸发时,未用玻璃棒搅拌
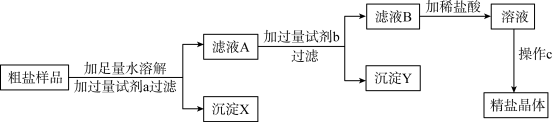
(3)粗盐样品中含有杂质氯化镁、氯化钙。某同学设计了以下提纯方案:
a方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的_____ 。
b滤液B中所含的溶质为______ 。
c向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为___ 时,应停止滴加,如果滴加的稀盐酸过量,对最后得到的精盐晶体的成分_____ (填“有”或“没有”)影响。
d操作C的名称为____ 。
e工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式。_______ 。
(2)某兴趣小组利用如下仪器进行粗盐提纯实验。

①写出下列仪器的名称: C
②其具体操作步骤如下:
步骤一:溶解:用托盘天平称取经研钵研磨过的粗盐2.0g投入烧杯中,要对粗盐进行研磨的原因是
步骤二:过滤:组装一套过滤器,所需要的仪器除需要图中的仪器外还需要的仪器有
将粗盐水分几次沿玻璃棒小心倒入漏斗内,玻璃棒所起的作用是
观察滤纸上方和滤液情形,发现滤液呈浑浊状态,其原因可能是
步骤三:蒸发:搭建一套蒸发装置,将滤液倒入蒸发皿中,点燃酒精灯加热,并用玻璃棒轻轻搅拌,当
③提纯之后该兴趣小组计算的氯化钠的产率偏低,则可能的原因是
A 溶解含有泥沙的粗盐时,搅拌时间不足
B 过滤时,液面高于滤纸边缘
C 蒸发时,未用玻璃棒搅拌

(3)粗盐样品中含有杂质氯化镁、氯化钙。某同学设计了以下提纯方案:
a方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的
b滤液B中所含的溶质为
c向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为
d操作C的名称为
e工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式。
您最近一年使用:0次
【推荐2】海洋是生命的摇篮,浩瀚的海洋是一个巨大的宝库,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
I.海水提取粗盐

(1)氯化钠在海水中的分散微粒是_______ (填微粒符号)。
(2)从贮水池到蒸发池,氯化钠的质量分数_______ (填“变大”“变小”或“不变”)。
II.粗盐提纯
可以采用物理和化学方法除去粗盐中的MgCl2、CaCl2和Na2SO4等可溶性杂质。
(3)物理方法:用NaCl溶液浸洗粗盐,溶解其中的可溶性杂质,则浸洗溶液应选用NaCl的_____ (填“饱和”或“不饱和”)溶液。
(4)化学方法:操作步骤依次为:加水溶解→加过量NaOH溶液→加过量试剂①→加过量Na2CO3→过滤→加适量盐酸,试剂①是_________ (填化学式)溶液,过滤后滤渣主要成分有Mg(OH)2、CaCO3及______ (写出全部成分)。
III.侯氏制碱
我国科学家侯德榜为我国纯碱和氮肥工业技术的发展做出了杰出的贡献。如图是侯氏联合制碱法和西方索尔维制碱法的工艺流程。(已知.NH4Cl NH3↑+HCl↑
NH3↑+HCl↑
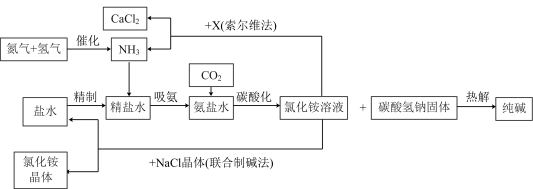
(5)利用碳酸氢钠热解生产纯碱反应的基本类型是________ 。
(6)精盐水中先通入NH3,后通入CO2发生“碳酸化”反应的化学方式是_____ 。
(7)我国化学家侯德榜创立的联合制碱法的优点有________ 。
a.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
b.大大提高了食盐的利用率,节约了成本
c.析出的晶体可用作复合肥,提高了原料的利用率
(8)用“侯氏联合制碱法”制得碳酸钠常含有少量氯化钠。为测定某样品中碳酸钠含量,小明称取该碳酸钠样品11g溶解于水中,加入足量氯化钙溶液,经过滤、洗涤、干燥后得沉淀质量为10g。求:该样品中碳酸钠的质量分数。(写出具体计算过程,结果精确到0.1%)。
I.海水提取粗盐

(1)氯化钠在海水中的分散微粒是
(2)从贮水池到蒸发池,氯化钠的质量分数
II.粗盐提纯
可以采用物理和化学方法除去粗盐中的MgCl2、CaCl2和Na2SO4等可溶性杂质。
(3)物理方法:用NaCl溶液浸洗粗盐,溶解其中的可溶性杂质,则浸洗溶液应选用NaCl的
(4)化学方法:操作步骤依次为:加水溶解→加过量NaOH溶液→加过量试剂①→加过量Na2CO3→过滤→加适量盐酸,试剂①是
III.侯氏制碱
我国科学家侯德榜为我国纯碱和氮肥工业技术的发展做出了杰出的贡献。如图是侯氏联合制碱法和西方索尔维制碱法的工艺流程。(已知.NH4Cl
 NH3↑+HCl↑
NH3↑+HCl↑
(5)利用碳酸氢钠热解生产纯碱反应的基本类型是
(6)精盐水中先通入NH3,后通入CO2发生“碳酸化”反应的化学方式是
(7)我国化学家侯德榜创立的联合制碱法的优点有
a.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
b.大大提高了食盐的利用率,节约了成本
c.析出的晶体可用作复合肥,提高了原料的利用率
(8)用“侯氏联合制碱法”制得碳酸钠常含有少量氯化钠。为测定某样品中碳酸钠含量,小明称取该碳酸钠样品11g溶解于水中,加入足量氯化钙溶液,经过滤、洗涤、干燥后得沉淀质量为10g。求:该样品中碳酸钠的质量分数。(写出具体计算过程,结果精确到0.1%)。
您最近一年使用:0次




