某化学兴趣小组设计如下表所示的对比实验来比较MnO2、CuO对过氧化氢的催化效果,所用实验装置如图所示。
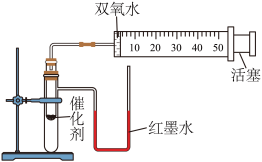
(1)实验2中制取氧气的文字表达式为__________ 。
(2)实验需要测量并记录的数据有:氧气体积和__________ 。
(3)实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U型管内右侧液面上升,原因是_________ 。
(4)结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是_______ 。
| 实验序号 | 过氧化氢溶液 | 催化剂 |
| 实验1 | 5ml 4% | 粉末状MnO20.2g |
| 实验2 | 5ml 4% | 粉末状CuO0.2g |

(1)实验2中制取氧气的文字表达式为
(2)实验需要测量并记录的数据有:氧气体积和
(3)实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U型管内右侧液面上升,原因是
(4)结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是
更新时间:2021-03-05 01:48:49
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
(1)通过实验①和②对比可知,化学反应快慢与______________ 有关;
(2)通过对比实验____________ 和___________ 可知,化学反应快慢与温度的关系是____________ .
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是______________ .
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)_____
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(1)通过实验①和②对比可知,化学反应快慢与
(2)通过对比实验
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)
您最近一年使用:0次
【推荐2】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢分解的催化剂以后,想再探究其他一些物质如三氧化二铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白:
(1)〔问题〕Al2O3能不能作过氧化氢分解的催化剂呢?
(2)〔猜想〕Al2O3能作过氧化氢分解的催化剂。
(3)〔实验验证〕
(4)〔结论〕Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
(5)〔讨论与反思〕经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验(实验三):
〔实验目的〕 探究________ 。
〔实验步骤〕①准确称量少量Al2O3 的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、烘干、________ ;④反应前后进行对比。
〔讨论〕如果Al2O3在反应前后_______ 不变,也不能说明Al2O3可以作过氧化氢分解的催化剂。理由是还应设计实验:探究Al2O3的_______ 性质是否发生变化。
(1)〔问题〕Al2O3能不能作过氧化氢分解的催化剂呢?
(2)〔猜想〕Al2O3能作过氧化氢分解的催化剂。
(3)〔实验验证〕
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 木条不复燃 | 常温下过氧化氢溶液的分解速率很慢 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,将带火星的木条伸入试管中 | 木条复燃 | Al2O3能加快过氧化氢的分解速率 |
(4)〔结论〕Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
(5)〔讨论与反思〕经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验(实验三):
〔实验目的〕 探究
〔实验步骤〕①准确称量少量Al2O3 的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、烘干、
〔讨论〕如果Al2O3在反应前后
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。

(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为_____________ 。
(2)实验1得到的结论是___________ 。实验2的目的是 __________ 。欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比 __________ 。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、 ),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是___________ 。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是_________ 、 ________ 。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_______ 。理由是 ________ 。
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。

(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为
(2)实验1得到的结论是
(3)小组同学通过互联网得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、
 ),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
),稀硫酸中含有三种粒子(H2O、H+、SO42-)为了进一步探究CuSO4溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。①小组同学认为最不可能的是H2O,他们的理由是
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
| 实验步骤 | 实验现象 | 结论 |
| A.取一支试管加入5 mL 5%过氧化氢溶液,然后加入2~3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 |
| B.另取一支试管加入5 mL 5%过氧化氢溶液,然后加入2~3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?
您最近一年使用:0次
【推荐1】小李将实验剩余的FeCl3溶液倒入含有H2O2的废液缸,产生大量的无色气泡。
(1)小李根据组成的元素猜测,无色气体可能是H2、O2、HCl、Cl2中的一种或多种。
【查阅资料】
I.Cl2是黄绿色、有刺激性气味的气体;
II.FeCl3在水中解离出Fe3+、Cl-
根据资料,小李可排除的气体为________ 。
【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察到木条燃得更旺,则该气体一定含_________ (填气体名称)。
(2)小李认为上述过程中FeCl3溶液作了H2O2分解的催化剂。
【实验二】为了进一步探究哪种离子起催化作用,他做了下图所示的对比实验。若要证明FeCl3溶液中的Fe3+对H2O2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为_________ 。
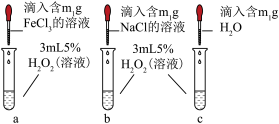
(3)小王同学认为由此得出“FeCl3溶液作H2O2分解的催化剂”的结论不严谨,还需要补充实验来进一步探究,他们又设计了如下实验。
【实验三】

X溶液中溶质的化学式为________ 。
【得出结论】要证明FeCl3溶液作H2O2分解的催化剂,须满足以下两个方面的条件:
①从定性角度需观察到______ (填序号)的现象。
A.实验一 B.实验二 C.实验三
②从定量角度需得到的关系式为m1=______ (用m2和m3表示)。
(1)小李根据组成的元素猜测,无色气体可能是H2、O2、HCl、Cl2中的一种或多种。
【查阅资料】
I.Cl2是黄绿色、有刺激性气味的气体;
II.FeCl3在水中解离出Fe3+、Cl-
根据资料,小李可排除的气体为
【实验一】为进一步验证该气体成分,他用燃着的木条伸入收集满该气体的小试管中,只观察到木条燃得更旺,则该气体一定含
(2)小李认为上述过程中FeCl3溶液作了H2O2分解的催化剂。
【实验二】为了进一步探究哪种离子起催化作用,他做了下图所示的对比实验。若要证明FeCl3溶液中的Fe3+对H2O2分解起催化作用,除观察到试管c中无明显现象外,还需观察到的现象为

(3)小王同学认为由此得出“FeCl3溶液作H2O2分解的催化剂”的结论不严谨,还需要补充实验来进一步探究,他们又设计了如下实验。
【实验三】

X溶液中溶质的化学式为
【得出结论】要证明FeCl3溶液作H2O2分解的催化剂,须满足以下两个方面的条件:
①从定性角度需观察到
A.实验一 B.实验二 C.实验三
②从定量角度需得到的关系式为m1=
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】化学废渣的回收可以变废为宝,还能提高学生的环保意识。在一次整理初中化学实验室时,同学们发现了一包黑色固体粉末,它到底是什么物质,能否回收利用呢?老师带领大家一起展开了探究。
【实验目的】探究黑色物质的组成成分。
【实验猜想】黑色固体可能是碳粉、铁粉、二氧化锰粉末、氧化铜粉末中的一种或者几种。
【查阅资料】氧化铜可以和稀硫酸反应生成硫酸铜和水。
【实验步骤】
【实验结论】该黑色固体中含有_____ (写出化学式)。
【反思评价】1请指出步骤4的不足之处:_____ 。
2小丽同学设计实验回收固体,如图,滤液的主要成分是硫酸铜,请写出①的化学方程式:_____ 。
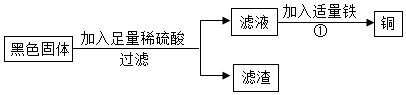
【实验目的】探究黑色物质的组成成分。
【实验猜想】黑色固体可能是碳粉、铁粉、二氧化锰粉末、氧化铜粉末中的一种或者几种。
【查阅资料】氧化铜可以和稀硫酸反应生成硫酸铜和水。
【实验步骤】
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:用磁铁吸引黑色粉末。 | 黑色粉末没有被吸引。 | 说明 |
| 步骤2:在试管中加入5mL 5%的过氧化氢溶液,再向其中加入少量黑色粉末,把带火星的木条伸入试管。 | 说明没有二氧化锰粉末。 | |
| 步骤3:取黑色粉末于燃烧匙中,在酒精灯上加热到红热,将其伸入盛满氧气的集气瓶中,反应后向集气瓶中加入澄清石灰水。 | 黑色粉末剧烈燃烧,发出白光; | 说明有碳粉。 |
步骤4:设计如下实验: | 双通玻璃管中 试管中石灰水变浑浊。 | 说明 |
【反思评价】1请指出步骤4的不足之处:
2小丽同学设计实验回收固体,如图,滤液的主要成分是硫酸铜,请写出①的化学方程式:

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组对过氧化氢分解反应进行探究:
【探究一】探究影响过氧化氢分解速率的因素:
分别取5 mL 溶液进行实验,测定产生4 mL
溶液进行实验,测定产生4 mL  所需时间,实验结果记录如下表:
所需时间,实验结果记录如下表:
(1)欲使①②构成对比,应使x=______ ,对比①②两个实验,若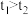 ,则可得出的结论是:
,则可得出的结论是:______ 。
(2)能证明过氧化氢分解速率与其浓度有关的实验组合是______ (填实验序号)。
(3)定量比较反应速率的方法还可以是______ 。
(4)请你再写出一种影响过氧化氢分解速率的因素______ 。
【探究二】探究氧化铁( )能否用作过氧化氢分解的催化剂
)能否用作过氧化氢分解的催化剂
实验步骤及现象如下:
实验结论:
(5)上面表格中两空格的实验现象补充完整:①______ ,②______ 。
(6)实验Ⅱ的目的是______ ,实验Ⅲ的目的是______ 。
(7)写出氧化铁催化作用下,过氧化氢分解的化学方程式______ 。
【探究一】探究影响过氧化氢分解速率的因素:
分别取5 mL
 溶液进行实验,测定产生4 mL
溶液进行实验,测定产生4 mL  所需时间,实验结果记录如下表:
所需时间,实验结果记录如下表:| 实验序号 |  溶液的浓度(%) 溶液的浓度(%) | 温度(℃) |  粉末用量(g) 粉末用量(g) | 反应时间(t) |
| ① | x | 35 | 0 |  |
| ② | 30 | 55 | 0 |  |
| ③ | 5 | 20 | 0.1 |  |
| ④ | 15 | 20 | 0.1 |  |
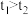 ,则可得出的结论是:
,则可得出的结论是:(2)能证明过氧化氢分解速率与其浓度有关的实验组合是
(3)定量比较反应速率的方法还可以是
(4)请你再写出一种影响过氧化氢分解速率的因素
【探究二】探究氧化铁(
 )能否用作过氧化氢分解的催化剂
)能否用作过氧化氢分解的催化剂实验步骤及现象如下:
| 实验步骤 | 预期实验现象 |
Ⅰ.往A、B两支试管中分别加入5 mL 5%的 溶液,向A试管中加入0.5 g氧化铁粉末,将带火星的木条分别伸入两支试管中。 溶液,向A试管中加入0.5 g氧化铁粉末,将带火星的木条分别伸入两支试管中。 | A试管中产生大量气泡,带火星的木条复燃;B试管中①_________ |
| Ⅱ.待A试管中不再产生气泡时,重新加入过氧化氢溶液,并把带火星的木条伸入试管中。 | 试管中产生大量气泡,带火星的木条复燃。 |
| Ⅲ.待实验Ⅱ中不再产生气泡时,将试管中的固体剩余物过滤,洗涤、干燥、称量。 | 所得固体质量为②______g |
(5)上面表格中两空格的实验现象补充完整:①
(6)实验Ⅱ的目的是
(7)写出氧化铁催化作用下,过氧化氢分解的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】以下是某研究小组探究影响反应速率部分因素的相关实验数据。
(1)通过实验①和②对比可知,化学反应速率与________ 有关;从实验③和④对比可知,化学反应速率与温度的关系是________ ;
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释 “反应物浓度越大,化学反应速率越快”的原因是________ 。
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量________ (填“增多”或“减少”或“不变”)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/mL | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | / | 2 | 49.21 |
| ④ | 30 | 5 | 35 | / | 2 | 10.76 |
(1)通过实验①和②对比可知,化学反应速率与
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释 “反应物浓度越大,化学反应速率越快”的原因是
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组在做完碳还原氧化铜实验后,进行了如下图所示的探究:
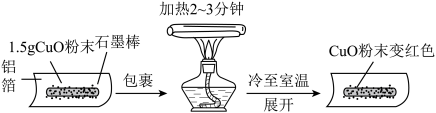
【猜想】把氧化铜还原成铜的物质是:Ⅰ. 石墨棒;Ⅱ. 铝箔。
【实验】用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹。按上述操作步骤实验,黑色粉末__________ ,那么猜想Ⅱ不成立。
【结论】石墨棒能使氧化铜还原成铜,该反应的化学方程式为__________ 。
【改进】把石墨棒换成铝粉,重复上述操作,又获成功。那么,称取等量的铝粉并进行同样的操作,其目的是__________ 。该反应的化学方程式为__________ 。
【拓展】如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好。联想在空气中灼热的铁丝不能燃烧,而铁粉能燃烧,其原因是__________ 。

【猜想】把氧化铜还原成铜的物质是:Ⅰ. 石墨棒;Ⅱ. 铝箔。
【实验】用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹。按上述操作步骤实验,黑色粉末
【结论】石墨棒能使氧化铜还原成铜,该反应的化学方程式为
【改进】把石墨棒换成铝粉,重复上述操作,又获成功。那么,称取等量的铝粉并进行同样的操作,其目的是
【拓展】如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好。联想在空气中灼热的铁丝不能燃烧,而铁粉能燃烧,其原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】催化剂在生产、生活和科研中的地位越来越重要。
探究一:验证MnO2在过氧化氢分解前后的质量没有改变。
(1)某同学用电子天平称取1.0MnO2于试管中,加入适量过氧化氢溶液,写出发生反应的符号表达式____ 。
探究二:红砖粉是否也能作过氧化氢分解的催化剂?效果怎样?
小雨以收集等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
_______ 。
(3)如图可用于此实验收集O2的装置是____ (填字母)。
(4)通过实验2与实验____ 的待测数据对比,可说明红砖粉能改变过氧化氢分解速率。
(5)如需证明红砖粉可作过氧化氢分解的催化剂,还需通过实验证明_____ 。
探究一:验证MnO2在过氧化氢分解前后的质量没有改变。
(1)某同学用电子天平称取1.0MnO2于试管中,加入适量过氧化氢溶液,写出发生反应的符号表达式
探究二:红砖粉是否也能作过氧化氢分解的催化剂?效果怎样?
小雨以收集等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 编号 | 过氧化氢 | 其他物质 | 待测数据 |
| 实验1 | 20mL5%过氧化氢溶液 | 无 | |
| 实验2 | 20mL5%过氧化氢溶液 | 1g红砖粉 | |
| 实验3 | 20mL5%过氧化氢溶液 | 1g二氧化锰 |


(3)如图可用于此实验收集O2的装置是
(4)通过实验2与实验
(5)如需证明红砖粉可作过氧化氢分解的催化剂,还需通过实验证明
您最近一年使用:0次



