某研究性学习小组为证明中和反应的发生进行以下探究,请你参与实验:
【方案一】甲同学按图一进行实验:
(1)观察到溶液由红色变为无色,证明反应发生,化学方程式为_ ;
【方案二】乙同学取一定量稀盐酸,向其中逐滴滴入氢氧化钠溶液,用传感器测溶液的 pH 曲线如图二:
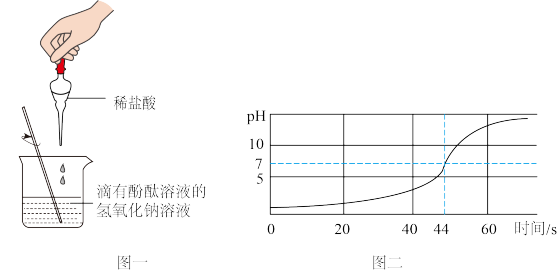
(2)40s 时,烧杯中溶液的溶质为_ (写溶质化学式,不考虑指示剂);
(3)请你根据图二分析稀盐酸和氢氧化钠溶液反应的依据是_ ;
【方案三】丙同学取变色硅胶(吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为无色液体)和氢氧化钠固体进行图三所示的实验:

(4)能证明酸和碱反应的现象是_ ;
【拓展探究】若不加酚酞试液,将稀盐酸与 10mL 稀氢氧化钠溶液混合后,再向其中加入硫酸铜溶液至蓝色沉淀质量不再增加,消耗硫酸铜溶液 5mL,此时还必须做一个对比试验才能证明两者确实反应。
(5)这个对比实验是(简述操作方法和结论)_ 。
【方案一】甲同学按图一进行实验:
(1)观察到溶液由红色变为无色,证明反应发生,化学方程式为
【方案二】乙同学取一定量稀盐酸,向其中逐滴滴入氢氧化钠溶液,用传感器测溶液的 pH 曲线如图二:

(2)40s 时,烧杯中溶液的溶质为
(3)请你根据图二分析稀盐酸和氢氧化钠溶液反应的依据是
【方案三】丙同学取变色硅胶(吸水后由蓝色变为红色)、无水醋酸(一种酸,常温下为无色液体)和氢氧化钠固体进行图三所示的实验:

(4)能证明酸和碱反应的现象是
【拓展探究】若不加酚酞试液,将稀盐酸与 10mL 稀氢氧化钠溶液混合后,再向其中加入硫酸铜溶液至蓝色沉淀质量不再增加,消耗硫酸铜溶液 5mL,此时还必须做一个对比试验才能证明两者确实反应。
(5)这个对比实验是(简述操作方法和结论)
更新时间:2021-06-22 14:55:43
|
相似题推荐
【推荐1】学习酸的性质是一项重要的内容,某化学兴趣小组以“探究硫酸的性质”为主题开展项目式学习
请回答下列问题。

【任务一】观察浓硫酸稀释过程中的能量变化。
(1)图甲实验中,观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水______ (填“放热”或“吸热”)。
【任务二】探究溶液浓度对硫酸化学性质的影响。
(2)图乙实验中,观察到很快变黑的是滤纸B,由此可知______ 不同,腐蚀性不同。
【任务三】探究稀硫酸的化学性质。
小组同学按图丙进行实验,分别将稀硫酸滴加到各试管中。
(3)试管2中可观察到的现象是______ 。
(4)该组同学利用数字化传感器测得试管3中不断加稀硫酸时,pH的变化图象如图4所示,二者恰好完全反应的微观示意图如图5所示。
①图4中a点所示溶液中含有的溶质是______ 。
②该反应中没有发生变化的微粒是______ (写出离子符号)

请回答下列问题。

【任务一】观察浓硫酸稀释过程中的能量变化。
(1)图甲实验中,观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水
【任务二】探究溶液浓度对硫酸化学性质的影响。
(2)图乙实验中,观察到很快变黑的是滤纸B,由此可知
【任务三】探究稀硫酸的化学性质。
小组同学按图丙进行实验,分别将稀硫酸滴加到各试管中。
(3)试管2中可观察到的现象是
(4)该组同学利用数字化传感器测得试管3中不断加稀硫酸时,pH的变化图象如图4所示,二者恰好完全反应的微观示意图如图5所示。
①图4中a点所示溶液中含有的溶质是
②该反应中没有发生变化的微粒是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】在一次实验中,老师将一定量的稀盐酸加入盛有氢氧化钠溶液的小烧杯中反应,未看到明显现象。请你参与学习并帮助填写空格。
【提出问题】反应后溶液中的溶质是什么?
【假设猜想】经分析大家认为,反应后的溶液中一定含有的一种溶质是X。甲组同学的猜想如下:
猜想I,只有X; 猜想Ⅱ:有X和HCI;
猜想Ⅲ:有X和NaOH: 猜想Ⅳ:有X、HCl和NaOH。
X的化学式是______ ;乙组同学认为猜想______ 是不合理的,理由是(用化学方程式表示)_____ 。
【实验探究】
(1)小红同学取烧杯中的溶液少量于斌管中,滴加几滴CuSO4溶液,无明显变化,说明猜想_________ 不成立。
(2)小君同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,认为猜想I成立。甲组同学认为小君同学的判断不科学,理由是_________ 。
(3)小兰同学取烧杯中的溶液少量于试管中,加入少量碳酸钙粉末,观察到有气泡产生,由此断定猜想Ⅱ成立。该实验发生反应的化学方程式是_________ 。
【实验拓展】请你用与(1)至(3)不同类别的试剂,设计另一种方案验证猜想Ⅱ成立。
实验操作:_________ ;现象:___________ 。
【提出问题】反应后溶液中的溶质是什么?
【假设猜想】经分析大家认为,反应后的溶液中一定含有的一种溶质是X。甲组同学的猜想如下:
猜想I,只有X; 猜想Ⅱ:有X和HCI;
猜想Ⅲ:有X和NaOH: 猜想Ⅳ:有X、HCl和NaOH。
X的化学式是
【实验探究】
(1)小红同学取烧杯中的溶液少量于斌管中,滴加几滴CuSO4溶液,无明显变化,说明猜想
(2)小君同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,认为猜想I成立。甲组同学认为小君同学的判断不科学,理由是
(3)小兰同学取烧杯中的溶液少量于试管中,加入少量碳酸钙粉末,观察到有气泡产生,由此断定猜想Ⅱ成立。该实验发生反应的化学方程式是
【实验拓展】请你用与(1)至(3)不同类别的试剂,设计另一种方案验证猜想Ⅱ成立。
实验操作:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】某小组在做 与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应,于是他们对反应后溶液中的溶质提出猜想,并进行了以下探究。
与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应,于是他们对反应后溶液中的溶质提出猜想,并进行了以下探究。
【提出问题】该溶液中的溶质含有哪些成分?
【猜想与假设】
(1)猜想Ⅰ:溶液中的溶质只有
猜想Ⅱ:溶液中的溶质有______
猜想Ⅲ:溶液中的溶质有 、
、
猜想Ⅳ:溶液中的溶质有 、
、 、
、
(2)请写出 与稀盐酸反应的化学方程式
与稀盐酸反应的化学方程式______ ,经过讨论,同学们直接得出猜想Ⅳ是不正确的,同学们的依据是______ 。为了验证余下的猜想,同学们又做了以下实验。
【进行实验】
(3)某小组的实验报告如下表:
【交流讨论】通过探究,同学请教老师:酸碱中和反应的微观实质是什么?
【证据与解释】
(4)为使该实验过程“可视化”,老师利用了 传感器进行实验
传感器进行实验 ,测定反应中溶液
,测定反应中溶液 的变化,得到曲线图
的变化,得到曲线图 。
。 中
中 点溶液中含有的微观粒子是
点溶液中含有的微观粒子是______ (填化学符号),能证明稀盐酸与氢氧化钠发生反应的证据是______ 。
(5)观察上述化学反应的反应物与生成物,发现酸与碱反应,生成盐和水,这类反应的微观实质是______ 。
 与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应,于是他们对反应后溶液中的溶质提出猜想,并进行了以下探究。
与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应,于是他们对反应后溶液中的溶质提出猜想,并进行了以下探究。【提出问题】该溶液中的溶质含有哪些成分?
【猜想与假设】
(1)猜想Ⅰ:溶液中的溶质只有

猜想Ⅱ:溶液中的溶质有
猜想Ⅲ:溶液中的溶质有
 、
、
猜想Ⅳ:溶液中的溶质有
 、
、 、
、
(2)请写出
 与稀盐酸反应的化学方程式
与稀盐酸反应的化学方程式【进行实验】
(3)某小组的实验报告如下表:
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞溶液 | 无明显现象 | 猜想Ⅲ不正确 |
| ②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钙 | 有气泡产生 | 猜想 |
【交流讨论】通过探究,同学请教老师:酸碱中和反应的微观实质是什么?
【证据与解释】
(4)为使该实验过程“可视化”,老师利用了
 传感器进行实验
传感器进行实验 ,测定反应中溶液
,测定反应中溶液 的变化,得到曲线图
的变化,得到曲线图 。
。 中
中 点溶液中含有的微观粒子是
点溶液中含有的微观粒子是
(5)观察上述化学反应的反应物与生成物,发现酸与碱反应,生成盐和水,这类反应的微观实质是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小红在实验室制取二氧化碳后,对反应后溶液中的溶质成分进行了如下探究:
【提出问题】溶液中溶质的成分是什么?
【作出猜想】猜想一:CaCl2;
猜想二:______ ;(填化学式)
【查阅资料】氯化钙溶液呈中性
【实验探究】
【实验反思】
(1)若要证明猜想二成立,你认为还可以选用的物质有______ (填字母代号)。
A.铜 B.氧化铜 C.硝酸银溶液 D.紫色石蕊溶液
(2)要使排放的溶液中溶质只有氯化钙,可加入过量的______ (填物质名称)。
【提出问题】溶液中溶质的成分是什么?
【作出猜想】猜想一:CaCl2;
猜想二:
【查阅资料】氯化钙溶液呈中性
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的上层清液于试管中,加入碳酸钠溶液至过量 | 猜想二正确 |
(1)若要证明猜想二成立,你认为还可以选用的物质有
A.铜 B.氧化铜 C.硝酸银溶液 D.紫色石蕊溶液
(2)要使排放的溶液中溶质只有氯化钙,可加入过量的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】如图1,化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。

(1)同学们观察到镁条在空气中剧烈燃烧,发出_______ ,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
(2)请写出镁条燃烧的化学方程式:_______ 。
(3)同学们通过称量发现:在石棉网上收集到生成物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律,你认为出现这样的实验结果的原因可能是_______ 。
(4)小红按如图2装置改进实验,验证了质量守恒定律,同时还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氨化镁可与水剧烈反应产生氨气,该气体能使酚酞溶液变成红色。
【做出猜想】黄色固体是Mg3N2。
【实验探究】请设计实验,验证猜想。
【反思与交流】
①氮化镁中氮元素的化合价是_______ 。
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是_______ 。
③图2中气球的作用是_______ 。

(1)同学们观察到镁条在空气中剧烈燃烧,发出
(2)请写出镁条燃烧的化学方程式:
(3)同学们通过称量发现:在石棉网上收集到生成物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律,你认为出现这样的实验结果的原因可能是
(4)小红按如图2装置改进实验,验证了质量守恒定律,同时还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氨化镁可与水剧烈反应产生氨气,该气体能使酚酞溶液变成红色。
【做出猜想】黄色固体是Mg3N2。
【实验探究】请设计实验,验证猜想。
| 实验操作 | 实验现象及结论 |
| 如图3,取燃烧生成物于小烧杯B中,加入适量 | 现象: 结论:燃烧产物中含Mg3N2 |
①氮化镁中氮元素的化合价是
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是
③图2中气球的作用是
您最近一年使用:0次
【推荐3】在食盐中加碘可以预防甲状腺肿大(俗称大脖子病),其中碘元素是以含碘钾盐形式加入的,某化学兴趣小组对加碘食盐中含碘钾盐的成分进行了探究。请参与探究并回答下列问题。
【提出问题】加碘食盐中含碘钾盐的成分是什么?
【查阅资料1】含碘钾盐主要有KI、KIO3。
【作出猜想】猜想一:KI;猜想二:______ (填化学式);猜想三:KI与KIO3的混合物。
【查阅资料2】
①KIO3与KI在酸性条件下能发生反应生成碘(I2),淀粉溶液遇I2变蓝色;②KI与AgNO3溶液可以反应,生成不溶于水的黄色AgI沉淀;③I2有毒,不能服用。
【讨论交流】小组同学根据资料进行讨论后,认为猜想______ (填“一”“二”或“三”)不正确,原因是______ 。
【实验验证】为验证其他猜想,小组同学设计了如下实验,请填写表格中空白处。
【实验结论】根据上述实验得知,加碘食盐中含碘钾盐是KIO3。
【实验拓展】小红按上述实验方法进行探究时,只准备了AgNO3溶液和KI溶液,请从下列生活用品中找出其他两种药品的替代物______ (填字母)。
A.米汤 B.白酒 C.小苏打 D.白醋
【提出问题】加碘食盐中含碘钾盐的成分是什么?
【查阅资料1】含碘钾盐主要有KI、KIO3。
【作出猜想】猜想一:KI;猜想二:
【查阅资料2】
①KIO3与KI在酸性条件下能发生反应生成碘(I2),淀粉溶液遇I2变蓝色;②KI与AgNO3溶液可以反应,生成不溶于水的黄色AgI沉淀;③I2有毒,不能服用。
【讨论交流】小组同学根据资料进行讨论后,认为猜想
【实验验证】为验证其他猜想,小组同学设计了如下实验,请填写表格中空白处。
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量加碘食盐于试管中,加水溶 解,再向试管中滴加AgNO3溶液 | 猜想一不成立 | |
实验二 | 另取少量加碘食盐于试管中,加水溶 解,先向试管中滴加稀硫酸酸化的KI 溶液,再向试管中滴加 | 溶液由无色变成蓝色 | 猜想二成立 |
【实验拓展】小红按上述实验方法进行探究时,只准备了AgNO3溶液和KI溶液,请从下列生活用品中找出其他两种药品的替代物
A.米汤 B.白酒 C.小苏打 D.白醋
您最近一年使用:0次



