金属及金属材料在生产、生活中有广泛的应用。
(1)生活中用铁锅做炊具,利用了铁的______ 性。铁锅易生锈,结合生活实际,写出一种防止铁锅生锈的具体方法______ 。铝的化学性质比铁活泼,但通常铝制品比铁制品更耐腐蚀的原因是______ ;
(2)我国古代曾用“湿法炼铜”“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。从减少空气污染的角度分析,相对环保的炼铜方法是______ ,写出其化学反应方程式______ ;
(3)已知Fe、R、Cr三种金属存在如下反应:Fe+ RCl2=R + FeCl2,Cr+FeSO4= Fe+CrSO4,则Fe、R、Cr三种金属的活动性由强到弱的顺序是______ ;
(4)含有锌粉6.5g,铁粉5.6g,铜粉3.2g,铝粉1.8g的混合物,与一定质量的稀硫酸反应,反应停止后,有6g固体剩余,则剩余固体是______ 。
(1)生活中用铁锅做炊具,利用了铁的
(2)我国古代曾用“湿法炼铜”“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。从减少空气污染的角度分析,相对环保的炼铜方法是
(3)已知Fe、R、Cr三种金属存在如下反应:Fe+ RCl2=R + FeCl2,Cr+FeSO4= Fe+CrSO4,则Fe、R、Cr三种金属的活动性由强到弱的顺序是
(4)含有锌粉6.5g,铁粉5.6g,铜粉3.2g,铝粉1.8g的混合物,与一定质量的稀硫酸反应,反应停止后,有6g固体剩余,则剩余固体是
更新时间:2021-08-14 02:06:42
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】氧化锌(ZnO)可作为紫外线吸收剂应用于化妆品中其一种生产工艺如下

(1)写出草酸铵中所含的原子团_____ 、_____ 。
(2)请补全“沉锌过程中发生反应的化学方程式ZnCl2+_____ =_____ ↓+2NH4Cl。
(3)“操作A”的名称是_____ 。
(4)“高温灼烧时草酸锌分解,预测可能生成的气体混合物:
猜想1:CO和O2猜想2:CO2和O2 猜想3:CO和CO2
预测的依据是:_____ 。
其中猜想(1)一定错误,因为_____ (写出化学方程式进行解释)。
请根据猜想3,书写草酸锌分解的化学方程式_____ 。

(1)写出草酸铵中所含的原子团
(2)请补全“沉锌过程中发生反应的化学方程式ZnCl2+
(3)“操作A”的名称是
(4)“高温灼烧时草酸锌分解,预测可能生成的气体混合物:
猜想1:CO和O2猜想2:CO2和O2 猜想3:CO和CO2
预测的依据是:
其中猜想(1)一定错误,因为
请根据猜想3,书写草酸锌分解的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】物质组成的探究是化学实验探究的重要内容。下面实验分别从定性、定量角度探究水的组成,请回答相关问题。
(1)为证明水不是由“水元素"组成的,1785年,拉瓦锡用水蒸气与红热铁管在高温下反应,实现了从水中脱去氧元素并获得氢气,同时生成四氧化三铁。模拟实验装置如图1。

①图1的玻璃管中反应的化学方程式为________ 。
②图I实验时,A、B两处应先加热________ (填“A”或“B”)处,理由是________ 。
③图2所示实验是通过直接分解水探究水的组成,以上两个实验均能推理得出水的组成元素,推理所依据的原理均为________ 。
(2)用图3所示装置可以定量测定水的组成(已知:H2+CuO Cu+H2O;装置D中干燥剂足量,其作用是充分吸收水蒸气)。C中固体物质在反应前后质量差为m1,D中物质在反应前后的质量差为m2。
Cu+H2O;装置D中干燥剂足量,其作用是充分吸收水蒸气)。C中固体物质在反应前后质量差为m1,D中物质在反应前后的质量差为m2。
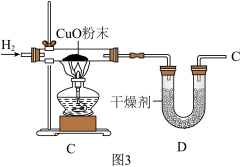
①据此可计算出水中H、O元素的质量比为________ (用含m1、m2的式子表示)。
②若实验中测得的H、O元素的质量比大于理论值,可能的原因是________ 。
A.通入的氢气没有干燥
B.加热前没有通入氢气排空气
C.氧化铜没有反应完
D.熄灭酒精灯后立即停止通入氢气
③有同学认为该装置存在缺陷,需要在c处连接一个装有干燥剂的干燥管,你认为________ (填“有”或“无”)必要。
(1)为证明水不是由“水元素"组成的,1785年,拉瓦锡用水蒸气与红热铁管在高温下反应,实现了从水中脱去氧元素并获得氢气,同时生成四氧化三铁。模拟实验装置如图1。

①图1的玻璃管中反应的化学方程式为
②图I实验时,A、B两处应先加热
③图2所示实验是通过直接分解水探究水的组成,以上两个实验均能推理得出水的组成元素,推理所依据的原理均为
(2)用图3所示装置可以定量测定水的组成(已知:H2+CuO
 Cu+H2O;装置D中干燥剂足量,其作用是充分吸收水蒸气)。C中固体物质在反应前后质量差为m1,D中物质在反应前后的质量差为m2。
Cu+H2O;装置D中干燥剂足量,其作用是充分吸收水蒸气)。C中固体物质在反应前后质量差为m1,D中物质在反应前后的质量差为m2。
①据此可计算出水中H、O元素的质量比为
②若实验中测得的H、O元素的质量比大于理论值,可能的原因是
A.通入的氢气没有干燥
B.加热前没有通入氢气排空气
C.氧化铜没有反应完
D.熄灭酒精灯后立即停止通入氢气
③有同学认为该装置存在缺陷,需要在c处连接一个装有干燥剂的干燥管,你认为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐3】阅读回答下列问题:
(1)汽车用铅酸蓄电池充电时发生反应的化学方程式为:2PbSO4+2X=PbO2+Pb+2H2SO4,X的化学式为______ ,其中PbO2中铅元素的化合价是______ 。
(2)某电镀厂排放的废液中含CuSO4、FeSO4、ZnSO4三种溶质,为减少水污染并节约成本,回收硫酸锌溶液、金属铁和铜,设计流程如图所示:______ 。
②步骤②加入Y的化学式为______ 。
③写出步骤③中发生反应的化学方程式______ (任写一个)。
(1)汽车用铅酸蓄电池充电时发生反应的化学方程式为:2PbSO4+2X=PbO2+Pb+2H2SO4,X的化学式为
(2)某电镀厂排放的废液中含CuSO4、FeSO4、ZnSO4三种溶质,为减少水污染并节约成本,回收硫酸锌溶液、金属铁和铜,设计流程如图所示:
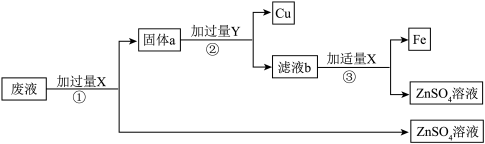
②步骤②加入Y的化学式为
③写出步骤③中发生反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)日常流通的1元、5角、1角硬币,应具有的化学性质是_________ ;
(2)根据下图的金属应用实例推断,金属具有的物理性质依次为________ 。

(3)小刚为比较锌、铁、银3种金属的活动性,向含有的Fe(NO3)2、AgNO3的混合液中加入一定量锌粉,如图实验所示,回答问题:

①根据实验操作过程_______ (填“能”或“不能”)判断Zn、Fe、Ag三种金属的活动性顺序。
②上述实验充分反应后过滤,得到滤渣和滤液。下列说法中正确的是_______ (填序号)。
a若滤液为浅绿色,则滤渣中可能有锌
b若滤液中一定有Zn(NO3)2、Fe(NO3)2,则也可能有AgNO3
c若滤渣中加稀盐酸无气泡产生,则滤液中一定有Zn2+、Fe2+
d若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有两种情况
(4)实验证明铁生锈实际上是铁与_______ 共同作用的结果。常用稀盐酸除铁锈,写出该反应的化学方程式________ 。
(5)我国自主研发制造的航母“山东舰”已于2019年12月17日正式入列海军,建造使用了大量的钛合金。一般情况下与组成它的纯金属相比,合金具有的特性是_________ 。
(1)日常流通的1元、5角、1角硬币,应具有的化学性质是
(2)根据下图的金属应用实例推断,金属具有的物理性质依次为

(3)小刚为比较锌、铁、银3种金属的活动性,向含有的Fe(NO3)2、AgNO3的混合液中加入一定量锌粉,如图实验所示,回答问题:

①根据实验操作过程
②上述实验充分反应后过滤,得到滤渣和滤液。下列说法中正确的是
a若滤液为浅绿色,则滤渣中可能有锌
b若滤液中一定有Zn(NO3)2、Fe(NO3)2,则也可能有AgNO3
c若滤渣中加稀盐酸无气泡产生,则滤液中一定有Zn2+、Fe2+
d若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有两种情况
(4)实验证明铁生锈实际上是铁与
(5)我国自主研发制造的航母“山东舰”已于2019年12月17日正式入列海军,建造使用了大量的钛合金。一般情况下与组成它的纯金属相比,合金具有的特性是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐2】金属材料广泛应用于生产、生活中。
(1)用铜作导线,利用了铜的延展性和_______________ 性。
(2)镁是一种活泼的金属,请写出镁与稀盐酸反应的化学方程式______________________ 。
(3)将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是__________________ ,相对原子质量最大的是____________________ 。

(4)向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是______________ (填字母序号)。
A若滤渣只含一种金属,则滤液中的溶质只有三种
B若滤液中含有两种金属离子,则滤渣中的固体只有两种
C若最终得到的滤渣质量仍为mg,则滤液中溶质最多有两种
D若向滤渣中加入稀盐酸,有气泡产生,则滤液中的溶质最多有两种
(1)用铜作导线,利用了铜的延展性和
(2)镁是一种活泼的金属,请写出镁与稀盐酸反应的化学方程式
(3)将等质量的A、B、C三种金属(生成物中金属元素均为+2价),分别放入质量分数相等且足量的稀盐酸中,产生H2的质量与反应时间的关系如图所示。A、B、C三种金属中,金属活动性由强到弱的顺序是

(4)向一定量的硝酸银和硝酸亚铁混合溶液中加入mg锌粉,充分反应后过滤,得到滤液和滤渣。下列分析正确的是
A若滤渣只含一种金属,则滤液中的溶质只有三种
B若滤液中含有两种金属离子,则滤渣中的固体只有两种
C若最终得到的滤渣质量仍为mg,则滤液中溶质最多有两种
D若向滤渣中加入稀盐酸,有气泡产生,则滤液中的溶质最多有两种
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】铝与铝的化合物有极其重要的用途。
(一)铝的存在
(1)铝是很活泼的金属,但铝制的炊具却耐腐蚀,其原因是___________ (用方程式表示)。
(2)使用铝制炊具会使人体摄入过量的“铝”,导致记忆力减退等不良症状。这里的“铝”是指___________ (填序号)。
A分子 B原子 C元素 D单质
(二)铝的利用:铝粒和生石灰、碳酸钠混合可制成发热包。
(3)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,放出大量的热,写出产生该现象的主要反应方程式___________ 。
(4)小明向使用后的发热包中加入稀盐酸,发现有气泡产生,于是他对产生的气体展开进一步探究。
【猜想与假设】小明认为该气体可能是a.H2;b.___________ ;c.H2和CO2的混合气体。
【实验设计】小明设计如图实验装置,对气体成分进行探究。

【实验验证】甲装置中的实验现象是___________ ,丁装置中黑色的粉末逐渐变为红色,试管口有水珠产生。证明猜想c正确。
若甲、乙装置交换位置,___________ (填“能”或“不能”)确定气体中含有CO2,写出化学方程式并说明理由___________ 。
(三)铝的化合物
硫酸铝铵晶体[NH4Al(SO4)2·xH2O]是一种用途广泛的含铝化合物。为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。

(5)固体甲是T1℃刚好完全失去结晶水的产物,则x=___________ 。(写出计算过程)
(6)T3℃时固体乙的成分是___________ (填字母)。
A Al(OH)3
B Al2(SO4)3
C Al2(SO4)3和Al(OH)3
(一)铝的存在
(1)铝是很活泼的金属,但铝制的炊具却耐腐蚀,其原因是
(2)使用铝制炊具会使人体摄入过量的“铝”,导致记忆力减退等不良症状。这里的“铝”是指
A分子 B原子 C元素 D单质
(二)铝的利用:铝粒和生石灰、碳酸钠混合可制成发热包。
(3)小明买了一盒自热米饭,取出发热包加入凉水,发生剧烈反应,放出大量的热,写出产生该现象的主要反应方程式
(4)小明向使用后的发热包中加入稀盐酸,发现有气泡产生,于是他对产生的气体展开进一步探究。
【猜想与假设】小明认为该气体可能是a.H2;b.
【实验设计】小明设计如图实验装置,对气体成分进行探究。

【实验验证】甲装置中的实验现象是
若甲、乙装置交换位置,
(三)铝的化合物
硫酸铝铵晶体[NH4Al(SO4)2·xH2O]是一种用途广泛的含铝化合物。为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。

(5)固体甲是T1℃刚好完全失去结晶水的产物,则x=
(6)T3℃时固体乙的成分是
A Al(OH)3
B Al2(SO4)3
C Al2(SO4)3和Al(OH)3
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】金属在日常生活中有着广泛的用途,常见金属的活动性顺序如图1。
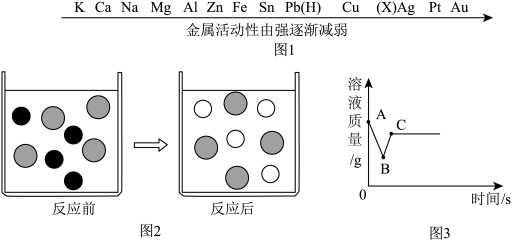
请回答下面问题
(1)图1金属活动性顺序表中的X是_____ (填写相应的元素符号)元素;
(2)若向CuSO4溶液中加入过量的Fe,充分反应后,能观察到的现象是________ ,如图2表示该反应前后溶液中存在的主要离子,请写出该图形代表的离子(填离子符号)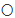 :
:____ ;
(3)向一定质量AgNO3,和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图3所示。图中B点溶液中,除水外还含有的物质有____ (填化学式),图中C点滤渣成分有____ (填化学式)。

请回答下面问题
(1)图1金属活动性顺序表中的X是
(2)若向CuSO4溶液中加入过量的Fe,充分反应后,能观察到的现象是
 :
:(3)向一定质量AgNO3,和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图3所示。图中B点溶液中,除水外还含有的物质有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】将锌、铁、铜三种金属同时放入一定量的硝酸银溶液中,充分反应后过滤,若滤纸上的金属有a种,滤液中的溶质有b种,则下列说法中正确的是( )
A若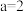 ,则b等于2或3
,则b等于2或3
B若向滤纸上的金属滴加硫酸溶液产生气体,则a一定等于4
C若 ,则b一定等于3
,则b一定等于3
D向滤液中加 溶液产生沉淀,b一定等于
溶液产生沉淀,b一定等于________
A若
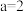 ,则b等于2或3
,则b等于2或3B若向滤纸上的金属滴加硫酸溶液产生气体,则a一定等于4
C若
 ,则b一定等于3
,则b一定等于3D向滤液中加
 溶液产生沉淀,b一定等于
溶液产生沉淀,b一定等于
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】金属材料与人类的生产和生活密切相关。
(1)下列用品中,主要利用金属导电性的是_____ (填字母,下同)。
A 铂金饰品
B 铁锅
C 铜导线
(2)人们在自然界中仅发现金、银等少数金属单质,其余金属元素都以化合物的形式存在,由此可说明金属的存在形式主要和金属的_____ 有关。
(3)铁制品生锈的原因是铁与空气中的_____ 共同接触的结果。防止自行车链条生锈的措施有_____ ,回收利用废旧金属制品的目的是_____ 。
(4)要比较Zn、Fe、Cu三种金属的活动性顺序,可选择的试剂有Fe、ZnCl2溶液和_____ 溶液。
(5)向硝酸铜溶液中加入一定量锌粉和铁粉的混合物,充分反应后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,有气泡产生。有关判断正确的是_____ 。
①滤渣中一定含有锌和铜
②滤渣中一定含有铁和铜,可能含有锌
③若滤液中含有2种溶质,则滤渣中一定含有锌
④若滤液呈无色,则滤渣中可能存在3种物质
A ①③ B ②③ C ①④ D ②④
(1)下列用品中,主要利用金属导电性的是
A 铂金饰品
B 铁锅
C 铜导线
(2)人们在自然界中仅发现金、银等少数金属单质,其余金属元素都以化合物的形式存在,由此可说明金属的存在形式主要和金属的
(3)铁制品生锈的原因是铁与空气中的
(4)要比较Zn、Fe、Cu三种金属的活动性顺序,可选择的试剂有Fe、ZnCl2溶液和
(5)向硝酸铜溶液中加入一定量锌粉和铁粉的混合物,充分反应后过滤,得到滤渣和滤液,向滤渣中滴加稀盐酸,有气泡产生。有关判断正确的是
①滤渣中一定含有锌和铜
②滤渣中一定含有铁和铜,可能含有锌
③若滤液中含有2种溶质,则滤渣中一定含有锌
④若滤液呈无色,则滤渣中可能存在3种物质
A ①③ B ②③ C ①④ D ②④
您最近一年使用:0次



