黄铜是铜锌合金。取10g黄铜于烧杯中,将120g稀硫酸分六次加入烧杯中,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
(1)该合金属于___________ 。(填物质类别)
(2)表中m=___________ 。
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
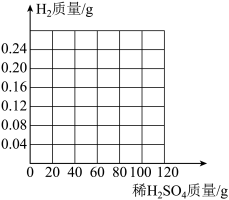
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 |
| 加入硫酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 剩余物的质量/g | 129.96 | 149.92 | m | 189.84 | 209.80 | 229.80 |
(2)表中m=
(3)所用稀硫酸的溶质质量分数(请根据化学方程式写出规范的计算步骤)
(4)请在下图画出:往10g黄铜加入稀硫酸,生成氢气质量的图像。

更新时间:2021-08-21 21:50:10
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】长久使用的热水瓶底部有一层水垢,主要成分是CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:取200g水垢,加入过量的稀盐酸,同时测量5分钟内生成气体的质量,结果如下表:
试回答下列问题:
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3_____(填已或未)反应完全?
(2)该水垢中CaCO3的质量分数是多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 30 | 50 | 60 | 66 | 66 |
试回答下列问题:
(1)4分钟后,产生的CO2不再增加,说明水垢中CaCO3_____(填已或未)反应完全?
(2)该水垢中CaCO3的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】某盐酸中混有少量的 MgCl2,小明为了测定该盐酸混合液中 HCl 的质量分数,进行如下图实验:
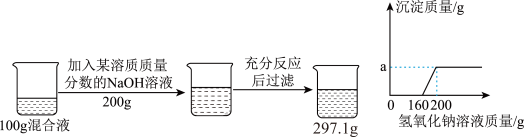
请结合如图实验数据,完成以下计算:
(1)观察上图的实验过程确定坐标图中 a 的数值为_____;
(2)所加NaOH 溶液的溶质质量分数为 20%,求该盐酸混合液中HCl 的质量分数。(写出计算过程;化学方程式:NaOH+HCl=NaCl+H2O;2NaOH+MgCl2=2NaCl+Mg(OH)2↓)

请结合如图实验数据,完成以下计算:
(1)观察上图的实验过程确定坐标图中 a 的数值为_____;
(2)所加NaOH 溶液的溶质质量分数为 20%,求该盐酸混合液中HCl 的质量分数。(写出计算过程;化学方程式:NaOH+HCl=NaCl+H2O;2NaOH+MgCl2=2NaCl+Mg(OH)2↓)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】金属是一种重要的材料,人类在6000年前就会炼铜,在约2500年前就会炼铁,在约200年前会炼铝。根据你的化学知识回答
(1)你认为金属大规模开发、利用的先后顺序跟下列那些因素有关_______
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属冶炼的难易程度
(2)钢铁生产和使用是人类文明和社会进步的重要标志,铁生锈也给人类带来巨大的损失,铁锈的主要成分是_____ ,把表面生锈的铁片浸入足量的稀硫酸中,首先观察到_____ 。过一会看到的现象是:_____ ,有关反应的化学方程式为:_______ 。
(3)黄铜是铜锌合金,外观很想黄金,不法分子常用黄铜冒充黄金行骗,请你说出一种鉴别二者的方法:______ 。
(4)为测定黄铜中铜的质量分数,取10g黄铜放入50g稀硫酸中恰好完全反应,生成氢气0.1g,试计算:黄铜中铜的质量分数。
(1)你认为金属大规模开发、利用的先后顺序跟下列那些因素有关
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属冶炼的难易程度
(2)钢铁生产和使用是人类文明和社会进步的重要标志,铁生锈也给人类带来巨大的损失,铁锈的主要成分是
(3)黄铜是铜锌合金,外观很想黄金,不法分子常用黄铜冒充黄金行骗,请你说出一种鉴别二者的方法:
(4)为测定黄铜中铜的质量分数,取10g黄铜放入50g稀硫酸中恰好完全反应,生成氢气0.1g,试计算:黄铜中铜的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】欲测定Cu﹣Zn合金及Cu﹣Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。
(1)你认为能测出合金中铜的质量分数的是_____ 合金。
(2)取该合金的粉末32.5g加入该硫酸充分反应,所加稀硫酸与生成的质量关系如图所示。
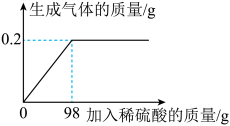
①生成气体的质量为_____ g。
②请计算该合金中铜的质量分数。_____ (请在写出第②问的详细解答过程)
(1)你认为能测出合金中铜的质量分数的是
(2)取该合金的粉末32.5g加入该硫酸充分反应,所加稀硫酸与生成的质量关系如图所示。

①生成气体的质量为
②请计算该合金中铜的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】黄铜是由铜和锌组成的合金,常用于制造阀门、水管等。化学小组利用某黄铜片样品进行了如下实验。
(1)按如图所示操作将黄铜片和纯铜片进行相互刻画,只有纯铜片上留下明显的划痕。据此得出的结论是______。
(2)证明此黄铜样品不是黄金,下列方法可行的是______(选填字母序号)。
A.直接观察颜色
B.在空气中灼烧后观察颜色
C.放入盐酸中观察是否被腐蚀
(3)将该样品加工成粉末,取一定质量的粉末加入硝酸银溶液中,充分反应后过滤,得到蓝色滤液和滤渣。则滤渣中一定有______,可能有______。
(4)利用如图所示装置测定该黄铜样品中铜的质量分数。取10g该黄铜粉末于烧杯中,分4次向其中加入稀盐酸。每次充分反应后称量烧杯及反应剩余物总质量,实验数据见下表。
请计算该黄铜样品中铜的质量分数______(写出计算过程)。

(1)按如图所示操作将黄铜片和纯铜片进行相互刻画,只有纯铜片上留下明显的划痕。据此得出的结论是______。
(2)证明此黄铜样品不是黄金,下列方法可行的是______(选填字母序号)。
A.直接观察颜色
B.在空气中灼烧后观察颜色
C.放入盐酸中观察是否被腐蚀
(3)将该样品加工成粉末,取一定质量的粉末加入硝酸银溶液中,充分反应后过滤,得到蓝色滤液和滤渣。则滤渣中一定有______,可能有______。
(4)利用如图所示装置测定该黄铜样品中铜的质量分数。取10g该黄铜粉末于烧杯中,分4次向其中加入稀盐酸。每次充分反应后称量烧杯及反应剩余物总质量,实验数据见下表。

| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸质量/g | 10 | 10 | 10 | 10 |
| 烧杯及反应剩余物质量/g | 125.56 | 135.52 | 145.50 | 155.50 |
请计算该黄铜样品中铜的质量分数______(写出计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某同学为探究铁合金中铁的质量分数,先后进行了三次实验(杂质不与稀硫酸反应),实验数据如下表:
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的铁完全反应了的次数是第______ 次。
(2)该铁合金中铁的质量分数是多少?
(3)第三次实验所得溶液溶质质量分数为多少?(结果保留至0.1%)。
| 实验次数 项目 | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 20 | 20 | 40 |
| 所加稀硫酸的质量/g | 100 | 120 | 80 |
| 生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的铁完全反应了的次数是第
(2)该铁合金中铁的质量分数是多少?
(3)第三次实验所得溶液溶质质量分数为多少?(结果保留至0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】同学为了测定某含杂质7%的黄铜(Cu、Zn)样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
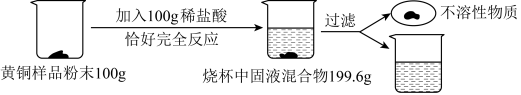
(1)发生反应的化学方程式为______ ;
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为______ ;
(3)反应生成的硫酸锌的质量为______ g;
(4)该黄铜样品中铜的质量分数是______ ;
(5)若工业上用100t含Cu2S80%的辉铜矿炼制上述黄铜样品,转化过程中损失10%,则可得到黄铜的质量为______ t。

(1)发生反应的化学方程式为
(2)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为
(3)反应生成的硫酸锌的质量为
(4)该黄铜样品中铜的质量分数是
(5)若工业上用100t含Cu2S80%的辉铜矿炼制上述黄铜样品,转化过程中损失10%,则可得到黄铜的质量为
您最近一年使用:0次

 ),放出气体的质量与所加稀硫酸(
),放出气体的质量与所加稀硫酸(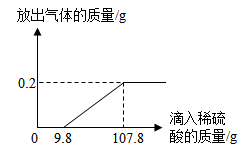
 Cu+H2O),请计算理论上最多可生产铜的质量。
Cu+H2O),请计算理论上最多可生产铜的质量。


