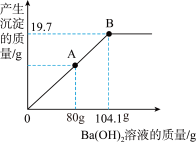
用托盘天平称取15.6 g Na2CO3和NaOH的混合物放入烧杯中,向烧杯里加入100g水,固体全部溶解,向所得溶液中滴加Ba(OH)2溶液,产生沉淀的质量与滴加Ba(OH)2溶液的质量关系曲线如图所示,请根据题意回答下列问题:
(1)用托盘天平称量Na2CO3和NaOH混合物的时候,砝码放在托盘天平的______ 盘(填“左”“右”之一);
(2)滴入Ba(OH)2溶液时,观察到的明显实验现象是______ 。
(3)当滴加Ba(OH)2溶液至图中A点时,烧杯中溶液含有的溶质有______ 种。
(4)计算当恰好完全反应时,溶液中溶质的质量质量分数为多少?

(1)用托盘天平称量Na2CO3和NaOH混合物的时候,砝码放在托盘天平的
(2)滴入Ba(OH)2溶液时,观察到的明显实验现象是
(3)当滴加Ba(OH)2溶液至图中A点时,烧杯中溶液含有的溶质有
(4)计算当恰好完全反应时,溶液中溶质的质量质量分数为多少?
更新时间:2021-09-26 00:11:05
|
相似题推荐
计算题
|
较难
(0.4)
真题
解题方法
【推荐1】取碳酸钠和氯化钠的白色固体混合物l4.6g,与68.3g一定质量分数的稀盐酸混合,恰好完全反应,所得溶液的质量为78.5g。试计算:
(1)生成气体的质量;
(2)反应后所得溶液中溶质的质量分数。
(1)生成气体的质量;
(2)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:先称取20g混合物样品,完全溶于81.99g水中,然后取用了一定质量分数的氯化钡溶液100g等分为4份,依次加入充分反应。实验数据见下表:
请分析计算:
(1)上表中x的数值为_______;
(2)原固体混合物中硫酸钠的质量分数是多少;
(3)第三次加入氯化钡溶液,充分反应后所得溶液的溶质质量分数。
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入氯化钡溶液质量(g) | 25 | 25 | 25 | 25 |
| 沉淀的质量(g) | 2.33 | x | 6.99 | 6.99 |
请分析计算:
(1)上表中x的数值为_______;
(2)原固体混合物中硫酸钠的质量分数是多少;
(3)第三次加入氯化钡溶液,充分反应后所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
(1)配制30g 10%的Na2CO3溶液.量取蒸馏水所需量筒的规格是 (从10、50、100中选择)mL.最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填序号).
A.30g B.10% C.Na2CO3溶液
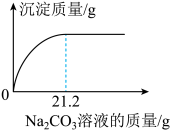
(2)测定未知浓度Ba(OH)2溶液的溶质质量分数.取50g Ba(OH)2溶液,逐滴滴加上述Na2CO3溶液的过程中,测得产生沉淀与加入Na2CO3溶液的质量关系如图所示.
①恰好完全反应时,消耗Na2CO3溶液的质量为 g.
②请通过计算确定Ba(OH)2溶液的溶质质量分数.
已知:Ba(OH)2+Na2CO3=BaCO3↓+2NaOH.

(1)配制30g 10%的Na2CO3溶液.量取蒸馏水所需量筒的规格是 (从10、50、100中选择)mL.最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填序号).
A.30g B.10% C.Na2CO3溶液
(2)测定未知浓度Ba(OH)2溶液的溶质质量分数.取50g Ba(OH)2溶液,逐滴滴加上述Na2CO3溶液的过程中,测得产生沉淀与加入Na2CO3溶液的质量关系如图所示.
①恰好完全反应时,消耗Na2CO3溶液的质量为 g.
②请通过计算确定Ba(OH)2溶液的溶质质量分数.
已知:Ba(OH)2+Na2CO3=BaCO3↓+2NaOH.
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末。烧杯中现有100g碳酸钠溶液,将150g氯化钙溶液分四次加入,充分反应,四次测量所得数据如表所示:
(1)m的值为_______。
(2)计算烧杯中100 g碳酸钠溶液中溶质的质量。(写出计算过程)
(3)在图中画出生成沉淀的质量与加入氯化钙溶液质量的关系曲线,并标注必要的数值。

| 次数 | 累计加入氯化钙溶液的质量/g | 烧杯中溶液的总质量/g |
| 一 | 40 | 134 |
| 二 | 80 | 168 |
| 三 | 120 | 205 |
| 四 | 150 | m |
(2)计算烧杯中100 g碳酸钠溶液中溶质的质量。(写出计算过程)
(3)在图中画出生成沉淀的质量与加入氯化钙溶液质量的关系曲线,并标注必要的数值。

您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】有一瓶较长时间敞口放置的熟石灰粉末试剂,为确定其变质情况,对该试剂进行如下定量测定:称取23.7g样品放入锥形瓶中,加入适量水充分振荡,再向锥形瓶中分步滴加一定浓度盐酸充分反应,测得数据如下表。
回答下列问题:
(1)加入120g盐酸并充分反应后,所得溶液中溶质的化学式为______ 。
(2)请列式求算出样品中所含变质产物碳酸钙的质量分数是多少?(精确到0.1%)
(3)画出产生气体的质量与加入盐酸质量的关系图。

(4)该样品中钙元素的质量分数是______ %(精确到0.1%)。
加入盐酸的总质量/g | 20 | 40 | 60 | 80 | 100 | 120 |
产生气体的总质量/g | 0 | 2.2 | 4.4 | 6.6 | m | 8.8 |
(1)加入120g盐酸并充分反应后,所得溶液中溶质的化学式为
(2)请列式求算出样品中所含变质产物碳酸钙的质量分数是多少?(精确到0.1%)
(3)画出产生气体的质量与加入盐酸质量的关系图。

(4)该样品中钙元素的质量分数是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】某同学用铁和稀硫酸在三个烧杯中进行了三次实验,实验数据如下表所示:
(1)第_____ 次实验中铁有剩余。
(2)称量上述铁粉需用到的仪器名称是_____ 。
(3)计算实验中所用的稀硫酸溶质的质量分数_____ (写出计算过程)。
| 第一次 | 第二次 | 第三次 | |
| 所取铁粉的质量/g | 5.6 | 5.6 | 8 |
| 所加稀硫酸的质量/g | 70 | 60 | 50 |
| 充分反应生成气体的质量/g | 0.2 | 0.2 | 0.2 |
(1)第
(2)称量上述铁粉需用到的仪器名称是
(3)计算实验中所用的稀硫酸溶质的质量分数
您最近一年使用:0次
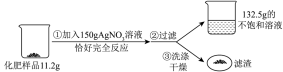
【推荐2】某化肥厂生产的氨肥标签如表所示。化学兴趣小组为测定其纯度,进行如图实验。(已知杂质全部溶于水,且不与硝酸银溶液反应)
(1)称量化肥样品时,需将化肥样品放在托盘天平的___________ (填“左盘”或“右盘”)上进行称量。
(2)2024年中央一号文件指出要确保粮食安全、全面推进乡村振兴。化肥的使用对发展粮食产业,助力乡村振兴有重要意义,下列关于化肥说法正确的是___________(填字母)。
(3)该化肥是否合格(写出计算过程,结果精确到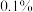 )。
)。
(4)求实验后得到的132.5g的不饱和溶液中溶质的质量分数为________ (结果精确到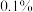 )。
)。
| XX化肥有限责任公司 氯化氨(  ) )净重25kg 纯度  |
|
(1)称量化肥样品时,需将化肥样品放在托盘天平的
(2)2024年中央一号文件指出要确保粮食安全、全面推进乡村振兴。化肥的使用对发展粮食产业,助力乡村振兴有重要意义,下列关于化肥说法正确的是___________(填字母)。
| A.氯化铵属于复合肥 | B.用熟石灰鉴别氯化铵和尿素[ ] ] |
| C.碳酸氢铵需密封保存于阴凉处 | D.为增加农作物产量,大量使用化肥和农药 |
(3)该化肥是否合格(写出计算过程,结果精确到
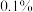 )。
)。(4)求实验后得到的132.5g的不饱和溶液中溶质的质量分数为
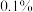 )。
)。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某兴趣小组同学欲测定黄铜(铜锌合金)中铜元素的含量,取10g黄铜样品于锥形瓶中,向其中分三次加入150g稀盐酸,充分反应后锥形瓶内物质总质量的变化情况如下表所示。
(1)用已校零的托盘天平称量10g黄铜时,观察到指针向右偏转,此时应该 。(填字母)
(2)表中第________ 次实验中反应物恰好完全反应。
(3)计算10g黄铜中铜的质量分数______ (写出计算过程)。
(4)上述反应中的150g稀硫酸是用质量分数为98%的浓硫酸稀释配制而成的,需要浓硫酸的质量为_____ g。
| 第一次 | 第二次 | 第三次 | |
| 加入稀硫酸的质量/g | 50 | 50 | 50 |
| 锥形瓶内物质的总质量/g | 59.9 | 109.8 | 159.8 |
| A.减少砝码 | B.增加黄铜 | C.向左调节平衡螺母 |
(3)计算10g黄铜中铜的质量分数
(4)上述反应中的150g稀硫酸是用质量分数为98%的浓硫酸稀释配制而成的,需要浓硫酸的质量为
您最近一年使用:0次

 。求:
。求: