向106 g质量分数为20%的碳酸钠溶液中逐滴加入质量分数为10%的稀盐酸,生成二氧化碳的质量随加入盐酸质量的变化关系如下图所示(不考虑CO2的溶解)。
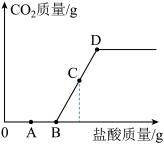
已知:OB段化学方程式:Na2CO3+HCl=NaCl+NaHCO3;
BD段(不含B点)化学方程式:NaHCO3+HCl=NaCl+H2O+CO2↑
请回答:
(1)二氧化碳由______ 种元素组成,碳和氧的原子个数比为______ 。
(2)NaHCO3的相对分子质量为______ 。
(3)B点对应的横坐标数值为______ 。
(4)假设C点横坐标为109.5,计算C点对应的二氧化碳质量。(写出计算过程)

已知:OB段化学方程式:Na2CO3+HCl=NaCl+NaHCO3;
BD段(不含B点)化学方程式:NaHCO3+HCl=NaCl+H2O+CO2↑
请回答:
(1)二氧化碳由
(2)NaHCO3的相对分子质量为
(3)B点对应的横坐标数值为
(4)假设C点横坐标为109.5,计算C点对应的二氧化碳质量。(写出计算过程)
更新时间:2021-11-06 15:07:14
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学从山上采集到一种石灰石,他取160g该样品进行煅烧实验(反应化学方程式 ,样品中杂质不参加反应),测得反应后固体的质量(m)与反应时间(t)的关系如表:
,样品中杂质不参加反应),测得反应后固体的质量(m)与反应时间(t)的关系如表:
请回答下列问题:
(1)t5时,该石灰石样品中CaCO3___________ (填“已”或“未”)完全反应,共生成CO2的质量为___________ ;
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
 ,样品中杂质不参加反应),测得反应后固体的质量(m)与反应时间(t)的关系如表:
,样品中杂质不参加反应),测得反应后固体的质量(m)与反应时间(t)的关系如表:| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m/g | 160 | 150 | 140 | 132 | 124 | 116 | 116 |
(1)t5时,该石灰石样品中CaCO3
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5g。试计算:
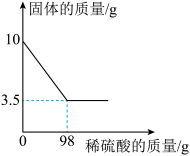
求:(1)铜样品中锌的质量是______(直接填结果);
(2)所用稀硫酸溶液的溶质质量分数是_____?(写过程)

求:(1)铜样品中锌的质量是______(直接填结果);
(2)所用稀硫酸溶液的溶质质量分数是_____?(写过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题。
(1)化学方程式 ,这个式子不仅表明了反应物是
,这个式子不仅表明了反应物是____ ,生成物是_______ ,反应条件是_______ ,还表示了参与反应的各物质之间的质量关系,即在点燃条件下,每_______ 份质量的硫与______ 份质量的氧气恰好完全反应生成______ 份质量的二氧化硫,该反应属于基本反应类型中的______ 反应。
(2)N(NO2)3是科学家 2011年发现的一种新型火箭燃料。试计算:
①N(NO2)3的相对分子质量______ ;
②N(NO2)3中氮元素和氧元素的质量比______ ;
③N(NO2)3中氮元素的质量分数______ 。
(1)化学方程式
 ,这个式子不仅表明了反应物是
,这个式子不仅表明了反应物是(2)N(NO2)3是科学家 2011年发现的一种新型火箭燃料。试计算:
①N(NO2)3的相对分子质量
②N(NO2)3中氮元素和氧元素的质量比
③N(NO2)3中氮元素的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铁是人体内氧的输送者,缺铁易患贫血。某贫血患者除正常饮食吸收铁元素外,还需服用含铁元素的某种药物,例如硫酸亚铁(FeSO4)。
(1)硫酸亚铁是由__ 种元素组成的___ (填“单质”或“化合物”);
(2)硫原子和氧原子个数比是____ ,硫酸亚铁中各元素的质量比是___ 。
(3)若治疗一个疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁(FeSO4)______ 克?(计算结果准确到0.01克)
(1)硫酸亚铁是由
(2)硫原子和氧原子个数比是
(3)若治疗一个疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁(FeSO4)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】当今,染发已经成为一种时尚,年轻人可以随自己的心情和喜好改变头发的颜色,给人眼前一亮的感觉。但是它在给予我们美丽的同时,会对我们的健康造成伤害,染发剂中的染料具有一定的毒性、刺激性和过敏性。例如,染发剂中普遍含有对苯二胺(其化学式为C6H8N2)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此,科学界告诫我们:慎用染发剂,少染发为好。

(1)该物质含有______ 种元素。
(2)该物质中碳元素和氢元素的质量比是__________ 。
(3)对苯二胺的化学式量(或相对分子质量)为_______________________ 。
(4)对苯二胺中氢元素的质量分数为______________ 。(结果保留到0.1%)。

(1)该物质含有
(2)该物质中碳元素和氢元素的质量比是
(3)对苯二胺的化学式量(或相对分子质量)为
(4)对苯二胺中氢元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】艾草中含有丰富的黄酮素(C15H10On) 黄酮素有很高的药用价值。请回答:
(1)黄酮素的相对分子质量是222,请计算出化学式中的n=______ 。
(2)黄酮素中碳、氢元素的质量比为______ (写最简比)。
(3)黄酮素中碳元素的质量分数为______ (计算结果精确到0.1%)。
(1)黄酮素的相对分子质量是222,请计算出化学式中的n=
(2)黄酮素中碳、氢元素的质量比为
(3)黄酮素中碳元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】新冠肺炎疫情期间,可用体积分数为75%的乙醇(C2H5OH)消毒液进行手和其他皮肤的消毒。但乙醇易燃,不适合用于室内环境消毒,使用时要注意安全。
请回答下列问题:
(1)乙醇由_______元素组成,相对分子质量为_______,分子中碳原子与氢原子的个数比为_______,碳元素与氢元素的质量比为_______。
(2)等质量的乙醇和水中氧元素的质量比是多少。(要求写出计算过程,求出最简整数比)
请回答下列问题:
(1)乙醇由_______元素组成,相对分子质量为_______,分子中碳原子与氢原子的个数比为_______,碳元素与氢元素的质量比为_______。
(2)等质量的乙醇和水中氧元素的质量比是多少。(要求写出计算过程,求出最简整数比)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】人体缺乏维生素C(简写Vc)就会患坏血病、如图是维生素C的说明书部分信息。已知Vc由碳、氢、氧三种元素组成。请回答:

(1)Vc的化学式为______ 。
(2)Vc中碳、氢、氧元素的质量比为______ (写最简比)。Vc中碳元素的质量分数是______ (保留小数点后一位)。
(3)小明爸爸每天服用该Vc片剂,小明建议爸爸可食用西红柿来代Vc片,若100g西红柿含Vc 30mg,则小明爸爸每天食用西红柿______ g,即可达到服用上述Vc片的效果。

(1)Vc的化学式为
(2)Vc中碳、氢、氧元素的质量比为
(3)小明爸爸每天服用该Vc片剂,小明建议爸爸可食用西红柿来代Vc片,若100g西红柿含Vc 30mg,则小明爸爸每天食用西红柿
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】小李用盐酸与碳酸钙粉末反应验证质量守恒定律,实验装置如图
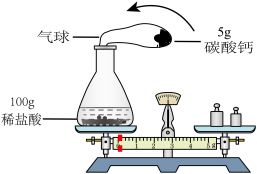
(1)根据实验目的,小李必须测量的数据是 。
A 锥形瓶质量 B 气球质量
C 反应前整个反应装置(包括里边的物质)质量 D 反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,再将碳酸钙粉末倒入锥形瓶中。反应结束后,气球鼓起,天平向右倾斜。小李按规范操作重新实验,得到相同结果。请你帮他分析原因 。
(3)反应结束后,锥形瓶中无固体剩余,则生成气体的质量是多少?将剩余溶液蒸干得到固体的质量是多少(写出计算过程)。

(1)根据实验目的,小李必须测量的数据是 。
A 锥形瓶质量 B 气球质量
C 反应前整个反应装置(包括里边的物质)质量 D 反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,再将碳酸钙粉末倒入锥形瓶中。反应结束后,气球鼓起,天平向右倾斜。小李按规范操作重新实验,得到相同结果。请你帮他分析原因 。
(3)反应结束后,锥形瓶中无固体剩余,则生成气体的质量是多少?将剩余溶液蒸干得到固体的质量是多少(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】某化工厂生产的纯碱中含有少量NaCl杂质,其产品包装袋上标有:碳酸钠≥96%.为了证实该产品中碳酸钠的含量,某同学取12g该样品放入烧杯中,称得烧杯和样品总质量为132.0g再把100g稀盐酸平均分成4次加入烧杯中,每次充分反应后烧杯和剩余物总质量如下:(每次反应产生的CO2气体都全部从烧杯中逸出)
请你根据表中数据分析:①第1次充分反应后产生的CO2气体质量是______ g
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)____
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 充分反应后烧杯和剩余物总质量/g | 155.2 | 178.4 | 202.6 | 227.6 |
请你根据表中数据分析:①第1次充分反应后产生的CO2气体质量是
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】如图是厨房中某品牌食用纯碱的成分表,兴趣小组同学称取16g样品置于烧杯中,并将烧杯放在电子天平上,加入50g稀盐酸(足量),用玻璃棒不断搅拌,每分钟记录一次天平示数,具体数据如下表:

(1)玻璃棒的作用是___________ 。
(2)分析表中数据可知,第___________ 分钟,样品与稀盐酸已完全反应,完全反应时产生气体的总质量是___________ g。
(3)通过计算说明成分表的标注是否真实。(写出计算过程,结果保留到0.1%)
(4)若实验中使用浓盐酸,会导致碳酸钠的质量分数测量结果___________ (选填“不变”、“偏小”或“偏大”)。

| 时间(分钟) | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 天平示数(g) | 116.0 | 112.7 | 110.5 | 109.4 | 109.4 | 109.4 | 109.4 |
(1)玻璃棒的作用是
(2)分析表中数据可知,第
(3)通过计算说明成分表的标注是否真实。(写出计算过程,结果保留到0.1%)
(4)若实验中使用浓盐酸,会导致碳酸钠的质量分数测量结果
您最近一年使用:0次



