学习了二氧化锰对过氧化氢溶液分解有催化作用的知识后,同学们对催化剂产生了兴趣,他们开展了以下探究。
实验探究一:比较催化剂种类对过氧化氢溶液分解的影响
【查阅资料】
(1)很多植物对过氧化氢溶液的分解有催化作用。
(2)压强传感器可以测量密闭体系内气体压强的变化。
【实验操作】
(1)在27.8℃,100.7kPa时,将具支试管的支管通过胶皮管与压强传感器连接(如图1所示),取2.0g植物碎末放入具支试管中。
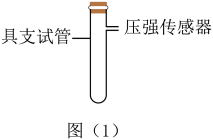
(2)用量筒量取2mL3%过氧化氢溶液,倒入具支试管中并立即塞上橡胶塞,同时启动数据采集程序采集数据。更换相同质量,不同种类的植物碎末,重复实验(1)和(2)。
(3)不加入植物碎末,重复实验(1)和(2),做空白实验。
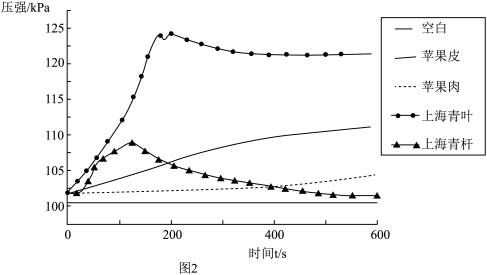
(4)将采集到的数据用电脑进行处理,得到反应前后压强随时间变化曲线如图2。
实验操作(3)的目的是_____ 。
【实验结论1】由图2可知,催化效果最好的是_____ 。
【交流反思】上海青叶作催化剂时,200s前曲线迅速升高的原因是_____ ;200s后曲线略有下降的原因是_____ 。除此之外,你还可以从图2中得出的结论是:_____ 。
实验探究二:比较催化剂用量对过氧化氢溶液分解的影响
【进行实验】
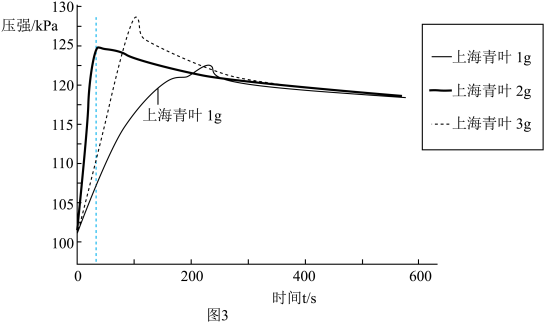
在30.2℃,压强100.5kPa时,选择上海青叶碎末用量分别为1g、2g、3g,均与2mL3%过氧化氢溶液反应,获得数据如图3所示。
【实验结论2】
由图3可知,在t1秒内,上海青叶用量为_____ 时,过氧化氢溶液分解速率最快;图中三条曲线最终将重合在一起,其理由是_____ 。
【拓展延伸】
某些植物、氧化铜、猪肝、二氧化锰等都可以做过氧化氢溶液分解的催化剂,除此以外,你还知道_____ 可以作过氧化氢溶液分解的催化剂。
实验探究一:比较催化剂种类对过氧化氢溶液分解的影响
【查阅资料】
(1)很多植物对过氧化氢溶液的分解有催化作用。
(2)压强传感器可以测量密闭体系内气体压强的变化。
【实验操作】
(1)在27.8℃,100.7kPa时,将具支试管的支管通过胶皮管与压强传感器连接(如图1所示),取2.0g植物碎末放入具支试管中。

(2)用量筒量取2mL3%过氧化氢溶液,倒入具支试管中并立即塞上橡胶塞,同时启动数据采集程序采集数据。更换相同质量,不同种类的植物碎末,重复实验(1)和(2)。
(3)不加入植物碎末,重复实验(1)和(2),做空白实验。
(4)将采集到的数据用电脑进行处理,得到反应前后压强随时间变化曲线如图2。
实验操作(3)的目的是
【实验结论1】由图2可知,催化效果最好的是
【交流反思】上海青叶作催化剂时,200s前曲线迅速升高的原因是


实验探究二:比较催化剂用量对过氧化氢溶液分解的影响
【进行实验】
在30.2℃,压强100.5kPa时,选择上海青叶碎末用量分别为1g、2g、3g,均与2mL3%过氧化氢溶液反应,获得数据如图3所示。
【实验结论2】
由图3可知,在t1秒内,上海青叶用量为
【拓展延伸】
某些植物、氧化铜、猪肝、二氧化锰等都可以做过氧化氢溶液分解的催化剂,除此以外,你还知道
更新时间:2021-11-23 14:42:38
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组的同学知道二氧化锰能作过氧化氢分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂。
【实验验证】
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂,氧化铝的化学式为_______ 。
【反思提高】经过讨论,有的同学认为只有上述两个实验,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验,原因是:____ 。
于是大家设计进行实验三:
【实验目的】探究___________ 。
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行___________ ,洗涤,干燥,称量;④对比反应前后氧化铝的质量。
【交流讨论】如果___________ ,通过以上实验探究说明氧化铝可以作过氧化氢分解的催化剂。在讨论过程中,有的同学认真阅读课本中催化剂的描述后提出,以上三个实验还不足以证明氧化铝是过氧化氢分解的催化剂,还应该补充证明的实验,才更加科学严谨。
【提出问题】氧化铝能不能作过氧化氢分解的催化剂呢?
【作出猜想】氧化铝能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡,木条不复燃 | 常温下过氧化氢溶液分解速率很慢 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,然后将带火星的木条伸入试管中 | 氧化铝能加快过氧化氢的分解速率 |
【得出结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能作过氧化氢分解的催化剂,氧化铝的化学式为
【反思提高】经过讨论,有的同学认为只有上述两个实验,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验,原因是:
于是大家设计进行实验三:
【实验目的】探究
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行
【交流讨论】如果
您最近一年使用:0次
【推荐2】高锰酸钾是初中常用的一种试剂,它可以和很多物质反应,发生颜色变化。小明和小丽把 经硫酸酸化的高锰酸钾溶液和草酸[H2C2O4]溶液混合,发现刚开始反应时溶液褪色不明显,但不久后褪色速度突然加快。为了探究反应过程中褪色速度加快的原因,小明查到了如下资料:
资料1:2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大。反应加快;温度开高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。小明经过分析,否定了假设一,理由是____________________ 。
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4,发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是_________________ 。这一实验基于的假设是_________________________ 。
资料1:2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+8H2O+10CO2↑
资料2:通常情况下,反应物浓度变大。反应加快;温度开高,反应加快。
(1)根据这些资料,小明提出了两个假设。
假设一:褪色速度突然加快是由反应物浓度变大引起的;
假设二:褪色速度突然加快是由反应过程中温度升高引起的。小明经过分析,否定了假设一,理由是
(2)小丽针对假设二进行实验探究后,经过思考,又做了如下实验:
把经硫酸酸化的高锰酸钾溶液等分为两份,分装A、B两试管,同时向两支试管中加入等量等浓度的草酸溶液,并置于同一水浴中。迅速向A试管中加入一定量的MnSO4,发现A试管中溶液褪色明显快于B试管。上述实验中,把2支试管置于同一水浴中的目的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组对氯酸钾分解反应的催化剂进行研究,经查阅资料得知氯酸钾除了跟二氧化锰混合加热能加快反应速率,与氧化铁混合加热也能较快产生氧气.在相同的加热条件下,完成表中实验:
【实验探究】
【交流讨论】
(1)设置实验1的目的是_______ ;实验2中“?”处应填_______ 。
(2)表中所列三种催化剂中催化效果最佳的是_______ 。
(3)写出氯酸钾在 催化作用下受热分解的符号表达式
催化作用下受热分解的符号表达式_______ 。
【提出问题】
(4)维持加热条件不变,用实验1再继续收集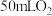 ,发现所需时间明显少于
,发现所需时间明显少于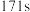 ,原因可能是
,原因可能是_______ 。
【实验反思】
(5)要确定氧化铁在此反应中作催化剂,还要证明它在化学反应前后质量和_______ 不变。
(6)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集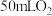 所需时间外,还可以测量相同时间内
所需时间外,还可以测量相同时间内_______ 。
【实验探究】
| 实验编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量g | 收集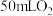 所需时间/s 所需时间/s |
| 1 | 5 | O | 0 | 171 |
| 2 | ? |  粉末 粉末 | 0.5 | 49 |
| 3 | 5 |  粉末 粉末 | 0.5 | 58 |
| 4 | 5 |  粉末 粉末 | 0.5 | 154 |
(1)设置实验1的目的是
(2)表中所列三种催化剂中催化效果最佳的是
(3)写出氯酸钾在
 催化作用下受热分解的符号表达式
催化作用下受热分解的符号表达式【提出问题】
(4)维持加热条件不变,用实验1再继续收集
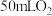 ,发现所需时间明显少于
,发现所需时间明显少于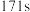 ,原因可能是
,原因可能是【实验反思】
(5)要确定氧化铁在此反应中作催化剂,还要证明它在化学反应前后质量和
(6)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集
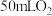 所需时间外,还可以测量相同时间内
所需时间外,还可以测量相同时间内
您最近一年使用:0次
【推荐1】管道疏通剂又称管道疏通颗粒,是一种新型厨卫管道深层清洁产品,主要针对厨卫管道内的油脂、毛发、菜渣、纸棉纤维等各种有机物质造成的堵塞进行疏通。某小组同学对管道疏通剂产生了浓厚的兴趣,并展开了一系列探究活动。
任务一:管道疏通剂的使用原理
【查阅资料】管道疏通剂的主要成分为氢氧化钠、过碳酸钠(化学式为2Na2CO3·3H2O2)、溶解剂。向管道疏通剂中加水,会放出热量,并有大量气体产生。
【交流讨论】
(1)根据以上资料分析,疏通剂疏通下水道时生成的气体可能是___________ 。
(2)热的氢氧化钠溶液能除去下水道中的油脂,利用了氢氧化钠___________ 的化学性质。
任务二:探究疏通剂溶于水发生反应的生成物
(3)填表:
任务三:定量比较过碳酸钠与某浓度过氧化氢制取氧气的效率
【查阅资料】要产生150mL氧气,若用过氧化氢溶液制取,则需9.11mL5%的过氧化氢溶液和0.2g二氧化锰;若用过碳酸钠制取,则需1.41g过碳酸钠和0.2g二氧化锰,并加水至9.11mL。运用控制变量法进行实验,测得前20min数据如图。
(4)2~20min内,曲线变化趋势是相同时间内,___________ (填“过碳酸钠”或“5%过氧化氢溶液”)产生的氧气量较多。
任务一:管道疏通剂的使用原理
【查阅资料】管道疏通剂的主要成分为氢氧化钠、过碳酸钠(化学式为2Na2CO3·3H2O2)、溶解剂。向管道疏通剂中加水,会放出热量,并有大量气体产生。
【交流讨论】
(1)根据以上资料分析,疏通剂疏通下水道时生成的气体可能是
(2)热的氢氧化钠溶液能除去下水道中的油脂,利用了氢氧化钠
任务二:探究疏通剂溶于水发生反应的生成物
(3)填表:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量管道疏通剂样品于试管中,加入适量水,将带火星的木条伸入试管内 | 有氧气生成 | |
| ②取少量①中的溶液于试管中,滴加 | 有碳酸钠生成 |
任务三:定量比较过碳酸钠与某浓度过氧化氢制取氧气的效率
【查阅资料】要产生150mL氧气,若用过氧化氢溶液制取,则需9.11mL5%的过氧化氢溶液和0.2g二氧化锰;若用过碳酸钠制取,则需1.41g过碳酸钠和0.2g二氧化锰,并加水至9.11mL。运用控制变量法进行实验,测得前20min数据如图。
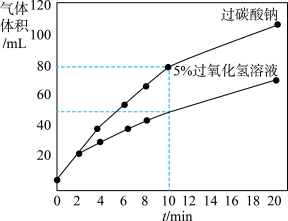
(4)2~20min内,曲线变化趋势是相同时间内,
您最近一年使用:0次
【推荐2】实验室常用过氧化氢溶液制取氧气。实验小组同学对该反应进行探究。
实验1:验证二氧化锰是过氧化氢分解的催化剂。

(1)过氧化氢分解的符号表达式为__________ 。
(2)Ⅳ中过滤需要的玻璃仪器有烧杯、玻璃棒和_______ ;称得的固体质量为______ g。
(3)证明二氧化锰能加快过氧化氢分解速率的实验现象是____________ 。
实验2:探究催化剂种类和质量对过氧化氢分解的催化效果的影响

【进行实验】
称取催化剂置于三颈瓶中,塞紧胶塞,用注射器将3 mL 5%过氧化氢溶液快速注入。测定氧气浓度达到最大值时所用的时间,实验记录如下:
注:①氧气浓度达到最高值时H2O2已完全分解。
②在可控范围内,过氧化氢分解速率越快,催化效果越好。
【解释与结论】
(4)实验2中,效果最好的催化剂是________ 。
(5)实验⑤⑥⑦的目的是__________ 。
【反思与评价】
(6)继续实验,发现活性炭比MnO2的催化效果差。其实验方案:称取0.03 g活性炭置于三颈瓶中,塞紧胶塞,用注射器将3 mL 5%过氧化氢溶液快速注入。在初始温度30℃时测定,测定结果是______ 。
实验1:验证二氧化锰是过氧化氢分解的催化剂。

(1)过氧化氢分解的符号表达式为
(2)Ⅳ中过滤需要的玻璃仪器有烧杯、玻璃棒和
(3)证明二氧化锰能加快过氧化氢分解速率的实验现象是
实验2:探究催化剂种类和质量对过氧化氢分解的催化效果的影响

【进行实验】
称取催化剂置于三颈瓶中,塞紧胶塞,用注射器将3 mL 5%过氧化氢溶液快速注入。测定氧气浓度达到最大值时所用的时间,实验记录如下:
| 序号 | 初始温度/℃ | 催化剂种类 | 催化剂质量/g | 氧气浓度达到最高值时所用时间/s |
| ① | 30 | MnO2 | 0.03 | 8 |
| ② | 30 | FeCl3 | 0.03 | 32 |
| ③ | 30 | FeCl3 | 0.04 | 29 |
| ④ | 30 | FeCl3 | 0.05 | 28 |
| ⑤ | 30 | CuCl2 | 0.03 | 3364 |
| ⑥ | 30 | CuCl2 | 0.04 | 837 |
| ⑦ | 30 | CuCl2 | 0.05 | 464 |
②在可控范围内,过氧化氢分解速率越快,催化效果越好。
【解释与结论】
(4)实验2中,效果最好的催化剂是
(5)实验⑤⑥⑦的目的是
【反思与评价】
(6)继续实验,发现活性炭比MnO2的催化效果差。其实验方案:称取0.03 g活性炭置于三颈瓶中,塞紧胶塞,用注射器将3 mL 5%过氧化氢溶液快速注入。在初始温度30℃时测定,测定结果是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题。
(1)【探究实验一】浓度对化学反应速率的影响
通过实验可得出结论:当其他条件相同时,过氧化氢的浓度越高,分解的速率
(2)【探究实验二】
此实验的目的是探究________ 对过氧化氢分解速率的影响,可得出的结论是________ 。
(1)【探究实验一】浓度对化学反应速率的影响
| 实验步骤 | 现象 |
| 1.取一支试管加入5g克5%的H2O2溶液,然后加入1g二氧化锰 | 缓慢有少量气泡冒出 |
| 2.另取一支试管加入 | 迅速有大量气泡冒出 |
(2)【探究实验二】
| 序号 | 溶液浓度 | 溶液质量/g | 温度/℃ | 收集的氧气体积/ml | 反应时间/S |
| 1 | 30% | 12 | 40 | 125 | 148 |
| 2 | 30% | 12 | 90 | 125 | 82 |
您最近一年使用:0次
【推荐1】某化学兴趣小组同学以“比较铝和锌的金属活动性强弱”为课题进行探究,下面是小华同学和小明同学探究的主要过程:
【提出问题】铝和锌两种金属,哪一种金属活动性更强?
【实验原理】小华同学利用常温下两种金属与酸反应,测定收集等体积氢气所需的时间,判断金属活动性强弱;小明同学利用金属与金属化合物溶液的反应比较金属活动性强弱。
【进行实验】
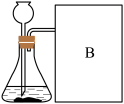
实验一:下图是小华的实验装置图,实验中B处宜采用的气体收集方法是______ 。
实验二:小明的实验方案
【分析与评价】
①写出铝与硫酸锌溶液反应的化学方程式________ 。
②两位同学的实验结论刚好相反,你判断______ 同学实验结论错误,理由是_____ 。
【拓展延伸】
为继续探究金属锌的化学性质,小敏向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向固体中加入足量稀盐酸,有气泡产生,则固体中含有的金属是_____ ,滤液中一定含有的金属离子是________ 。
【提出问题】铝和锌两种金属,哪一种金属活动性更强?
【实验原理】小华同学利用常温下两种金属与酸反应,测定收集等体积氢气所需的时间,判断金属活动性强弱;小明同学利用金属与金属化合物溶液的反应比较金属活动性强弱。
【进行实验】
实验一:下图是小华的实验装置图,实验中B处宜采用的气体收集方法是

| 实验编号 | 实验1 | 实验2 |
| 金属 | 1g表面未氧化的锌粒 | 1g表面打磨过的铝片 |
| 酸溶液 | 10mL10%的稀盐酸溶液 | 10mL10%的稀硫酸溶液 |
| 收集20mL氢气所需的时间 | 42s | 64s |
| 实验结论 | 根据实验现象,得出Zn | |
| 实验步骤 | 实验现象 | 实验结论 |
| 将表面打磨过的铝片插入硫酸锌溶液中 | 金属活动性:Al>Zn |
①写出铝与硫酸锌溶液反应的化学方程式
②两位同学的实验结论刚好相反,你判断
【拓展延伸】
为继续探究金属锌的化学性质,小敏向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向固体中加入足量稀盐酸,有气泡产生,则固体中含有的金属是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】科学探究是奇妙的过程,请你一起参与实验探究,并填写下列空白:
【提出问题】小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。小明联想到自己曾经用二氧化锰做过氧化氢分解的催化剂,他想,水泥块能否也可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡,冲洗、干燥,并进行以下探究。
【猜想】水泥块能作过氧化氢分解的催化剂。
【实验验证】
(1)请完善下面表格。
【结论】水泥块能加快过氧化氢的分解速率,故水泥块能作过氧化氢分解的催化剂。
【讨论与反思】
(2)小芳认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,她觉得需要增加一个探究实验:探究________ 。
【实验步骤】①准确称量水泥块的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量,对比反应前后水泥块的质量。
【分析】
(3)如果水泥块反应前后质量不变,则说明水泥块可以作为过氧化氢分解的催化剂。但小华认为,要证明小明的猜想,小芳的补充实验还是不足够,还需要再补充一个探究实验:探究________ 。
【结论】
(4)经过探究,最终确定水泥块可以作为过氧化氢分解得催化剂,请写出此反应的文字表达式:________ 。
【提出问题】小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。小明联想到自己曾经用二氧化锰做过氧化氢分解的催化剂,他想,水泥块能否也可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡,冲洗、干燥,并进行以下探究。
【猜想】水泥块能作过氧化氢分解的催化剂。
【实验验证】
(1)请完善下面表格。
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管中放入一根带火星的小木条 | 有少量气泡,木条 | 常温下过氧化氢溶液几乎不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 有大量气泡,木条复燃 |
【结论】水泥块能加快过氧化氢的分解速率,故水泥块能作过氧化氢分解的催化剂。
【讨论与反思】
(2)小芳认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,她觉得需要增加一个探究实验:探究
【实验步骤】①准确称量水泥块的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量,对比反应前后水泥块的质量。
【分析】
(3)如果水泥块反应前后质量不变,则说明水泥块可以作为过氧化氢分解的催化剂。但小华认为,要证明小明的猜想,小芳的补充实验还是不足够,还需要再补充一个探究实验:探究
【结论】
(4)经过探究,最终确定水泥块可以作为过氧化氢分解得催化剂,请写出此反应的文字表达式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学课上,化学兴趣小组完成《碱的化学性质实验》探究,发现CO2与NaOH溶液反应时无明显现象,老师提示同学们:可以从有某种生成物的角度或没有某种反应物的角度验证反应进行。于是,在老师指导下,设计了如下实验继续探究,(装置已连接好,气密性良好,止水夹a和b已关闭,部分仪器已略去),如图。

【查阅资料】①CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计;②常温下NaOH易溶于乙醇,Na2CO3微溶于乙醇。
【进行实验】
(1)把注射器中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是_____ ;写出该反应的化学方程式_____ 。
(2)把导管d移出澄清石灰水,打开止水夹a,b.再从导管c端往三口烧瓶中鼓入N2,目的是_____ 。过了一段时间后,先把导管d放入澄清石灰水中,接着关闭止水夹a,再把注射器Ⅱ中的稀盐酸(足量)注入三口烧瓶内,观察到三口烧瓶中产生气泡,_____ ,请写出产生气泡的化学方程式_____ 。该实验是从生成物角度验证了CO2与NaOH溶液发生了反应。
(3)请你再从反应物的角度设计实验验证CO2与NaOH溶液发生了反应_____ 。
【总结归纳】对于无明显现象的反应,可以通过改变实验装置,创设新的情境,观察到明显的反应现象,从而判断反应的发生。

【查阅资料】①CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计;②常温下NaOH易溶于乙醇,Na2CO3微溶于乙醇。
【进行实验】
(1)把注射器中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是
(2)把导管d移出澄清石灰水,打开止水夹a,b.再从导管c端往三口烧瓶中鼓入N2,目的是
(3)请你再从反应物的角度设计实验验证CO2与NaOH溶液发生了反应
【总结归纳】对于无明显现象的反应,可以通过改变实验装置,创设新的情境,观察到明显的反应现象,从而判断反应的发生。
您最近一年使用:0次



