计算:
(1)硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。取6.60g硅钢样品于烧杯中,将60.00g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应)。实验测得相关数据如表:
①根据表中数据判断,稀硫酸加入到第______ 次,铁恰好反应完全。
②表中W=______ g;6.60g硅钢样品中含铁的质量为______ g。
③计算该硅钢与稀硫酸充分反应后共产生多少g氢气。______ (写出详细过程)
(2)运用手持技术探究金属与酸的反应。向烧瓶内注入等量等浓度的稀硫酸,分别剪取长约0.4cm、宽约0.4cm的镁、铁、铜金属条,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图),点击采集得到如图所示的气压变化曲线。回答下列问题:

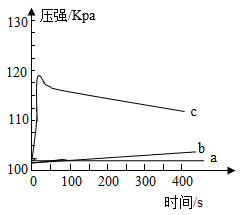
①金属Cu对应的曲线是______ 。
②曲线c在40s左右达到最高点后又略微下降的原因是______ 。
(1)硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。取6.60g硅钢样品于烧杯中,将60.00g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应)。实验测得相关数据如表:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 稀硫酸的质量 | 10.00g | 10.00g | 10.00g | 10.00g | 10.00g | 10.00g |
| 剩余固体质量 | 5.48g | Wg | 3.24g | 2.12g | 1.00g | 1.00g |
①根据表中数据判断,稀硫酸加入到第
②表中W=
③计算该硅钢与稀硫酸充分反应后共产生多少g氢气。
(2)运用手持技术探究金属与酸的反应。向烧瓶内注入等量等浓度的稀硫酸,分别剪取长约0.4cm、宽约0.4cm的镁、铁、铜金属条,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图),点击采集得到如图所示的气压变化曲线。回答下列问题:


①金属Cu对应的曲线是
②曲线c在40s左右达到最高点后又略微下降的原因是
更新时间:2021-12-05 13:09:02
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属在生活、生产中有着广泛的应用,种类繁多的金属材料已成为社会发展的重要物质基础。
(1)“芯片”是电子产品的核心部件,氮化嫁是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法错误的是______。

(2)铁制品锈蚀的过程,实际上是铁与空气中的______ 同时发生化学反应的过程。
(3)在实验室里,可以利用如图装置制得铁。

①将实验装置组装好后,设计了下列实验操作步骤:
a、通入一氧化碳气体;
b.停止加热;
c、给玻璃管加热;
d、停止通入一氧化碳气体;
e、检查装置气密性。
则正确的操作顺序是______ (填序号)。
②硬质玻璃管中的现象是______ ;反应方程式______ 。
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施______ 。
④工业上,高炉炼铁时,炉内要加入焦炭,焦炭的作用是______ 。
(4)工业上常用赤铁矿石冶炼生铁。现要生产5.6t含铁96%的生铁,需要含氧化铁80%的赤铁矿石的质量是多少?
(1)“芯片”是电子产品的核心部件,氮化嫁是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法错误的是______。

| A.图中m的值为3 |
| B.镓原子在化学反应中易得到电子 |
| C.镓元素的位置应该在Z处 |
| D.镓的最外层电子数与Al相同 |
(2)铁制品锈蚀的过程,实际上是铁与空气中的
(3)在实验室里,可以利用如图装置制得铁。

①将实验装置组装好后,设计了下列实验操作步骤:
a、通入一氧化碳气体;
b.停止加热;
c、给玻璃管加热;
d、停止通入一氧化碳气体;
e、检查装置气密性。
则正确的操作顺序是
②硬质玻璃管中的现象是
③从环保角度考虑,还需对以上装置进行改进,请简述改进措施
④工业上,高炉炼铁时,炉内要加入焦炭,焦炭的作用是
(4)工业上常用赤铁矿石冶炼生铁。现要生产5.6t含铁96%的生铁,需要含氧化铁80%的赤铁矿石的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】钢铁是使用最多的金属材料。
(1)生铁和钢是含碳量不同的两种铁合金,含碳量比较:生铁______ 钢(填“大于”、“等于”或“小于”)。
(2)下列关于铁及铁制品的说法中,正确的是______(填字母)。
(3)工业上冶炼钢铁的主要工艺流程如下:

①石灰石(主要成分为CaCO3)在高温下可将铁矿石中的SiO2转变为炉渣(CaSiO3),同时生成一种氧化物。该反应的化学方程式为______ 。
②从物质组成的角度分析,炼钢炉中通入O2的目的是______ 。
(4)取5.7g某铁合金样品(假设样品中只含铁和碳),加入到盛有足量稀硫酸的烧杯中,实验得到氢气的质量如表。
通过计算判断该铁合金属于生铁还是钢。(写出计算过程)。
(1)生铁和钢是含碳量不同的两种铁合金,含碳量比较:生铁
(2)下列关于铁及铁制品的说法中,正确的是______(填字母)。
| A.铁元素在地壳中的含量居于第四位 | B.沙漠地区的铁制品锈蚀较慢 |
| C.不锈钢保温杯可长时间盛放酸性饮品 | D.淬火后的缝衣钢针不能弯曲 |
(3)工业上冶炼钢铁的主要工艺流程如下:

①石灰石(主要成分为CaCO3)在高温下可将铁矿石中的SiO2转变为炉渣(CaSiO3),同时生成一种氧化物。该反应的化学方程式为
②从物质组成的角度分析,炼钢炉中通入O2的目的是
(4)取5.7g某铁合金样品(假设样品中只含铁和碳),加入到盛有足量稀硫酸的烧杯中,实验得到氢气的质量如表。
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 0 | 0.06 | 0.11 | 0.15 | 0.18 | 0.20 | 0.20 | 0.20 | 0.20 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】早在春秋战国时期,我国就开始生产和使用铁制品,时至今日,社会快速发展,钢铁仍然是我国使用最多的金属材料,请围绕金属铁开展主题式学习活动。
主题一:铁的认识
(1)铁元素在元素周期表中的信息及原子结构示意图如图所示,请回答:

①铁的原子序数为________ 。
②根据铁原子结构示意图可知,第三电子层X的数值为________ ,在化学变化中,铁原子容易失去电子,形成________ (选填“阳离子”或“阴离子”)。
(2)从物质类别角度分析,铁属于________ (选填“混合物”、“化合物”或“单质”),从物质的微观构成认识,铁是由____ (填具体微粒名称)构成。
主题二:铁的性质及应用
(3)铝的抗腐蚀性强于铁,为什么锤子、剪刀等用铁制而不用铝制________ 。
(4)下列铁制品中,利用了金属导热性的是________ (填字母)。
(5)不能用铁制容器配制农业上使用的波尔多液杀菌剂(成分中含有硫酸铜),原因是________ (用化学方程式表示)。
主题三:铁的来源及冶炼
铁资源在自然界中常以化合物的形式存在,工业上从含有铁元素并有开采价值的矿石中提炼金属铁。
【资料卡片】生铁和钢是含碳量不同的两种铁合金,其中生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(6)工业上冶炼钢铁的主要工艺流程如下图:

①工业上用赤铁矿石(主要成分 )炼铁的化学方程式
)炼铁的化学方程式 ,化学计量数a、b、c依次分别为
,化学计量数a、b、c依次分别为________ (填数字)。
②从物质成分的角度分析,生铁炼钢过程中,炼钢炉中通入O2的目的是________ 。
③用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量为________ t(保留整数)。
主题四:铁的锈蚀和防护
(7)为防止铁的锈蚀,下列采取的措施合理的是________ (填字母)。
A.为防止学校操场上的健身器材生锈,可在其表面喷漆
B.家中常用的铁锅,使用后洗净擦干,并保持表面洁净干燥
C.化学实验室的铁架台生锈了,保留其表面的铁锈,防止继续生锈
【活动总结】金属资源是自然界为人类提供的宝贵财富,请珍爱我们赖以生存的自然环境。也希望同学们通过不断的学习,今后能在金属的开采、利用及保护等方面为社会作出贡献。
主题一:铁的认识
(1)铁元素在元素周期表中的信息及原子结构示意图如图所示,请回答:

①铁的原子序数为
②根据铁原子结构示意图可知,第三电子层X的数值为
(2)从物质类别角度分析,铁属于
主题二:铁的性质及应用
(3)铝的抗腐蚀性强于铁,为什么锤子、剪刀等用铁制而不用铝制
(4)下列铁制品中,利用了金属导热性的是
A.河北沧州铁狮子 |
B.不锈钢水壶 |
C.铸铁井盖 |
(5)不能用铁制容器配制农业上使用的波尔多液杀菌剂(成分中含有硫酸铜),原因是
主题三:铁的来源及冶炼
铁资源在自然界中常以化合物的形式存在,工业上从含有铁元素并有开采价值的矿石中提炼金属铁。
【资料卡片】生铁和钢是含碳量不同的两种铁合金,其中生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(6)工业上冶炼钢铁的主要工艺流程如下图:

①工业上用赤铁矿石(主要成分
 )炼铁的化学方程式
)炼铁的化学方程式 ,化学计量数a、b、c依次分别为
,化学计量数a、b、c依次分别为②从物质成分的角度分析,生铁炼钢过程中,炼钢炉中通入O2的目的是
③用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量为
主题四:铁的锈蚀和防护
(7)为防止铁的锈蚀,下列采取的措施合理的是
A.为防止学校操场上的健身器材生锈,可在其表面喷漆
B.家中常用的铁锅,使用后洗净擦干,并保持表面洁净干燥
C.化学实验室的铁架台生锈了,保留其表面的铁锈,防止继续生锈
【活动总结】金属资源是自然界为人类提供的宝贵财富,请珍爱我们赖以生存的自然环境。也希望同学们通过不断的学习,今后能在金属的开采、利用及保护等方面为社会作出贡献。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】小华利用周末与妈妈一起打扫房间,她发现了许多与化学有关的现象和问题。请你与她一起分析,并回答有关问题:
(1)清理卫生间的过程中,她使用了洗洁精、洁厕灵和84消毒液三种清洁剂,查阅资料得知其有效成分如表所示:
①据其有效成分可知洗洁精呈_____ (填“酸性”、“碱性”或“中性”),若用pH试纸测定洗洁精的pH,应该_______ (填大于7、小于7或等于7);
②84消毒液中的NaClO在类别上属于(选填序号)___ ,其中氯元素的化合价为_____ ;(A酸B碱C盐D氧化物E有机物F无机物G化合物H单质)
③小华认为洁厕灵可用于铁制品表面除锈,发生反应的化学方程式为____ ;该反应所属基本反应类型为_______ 。
④查阅资料知:洁厕灵与84消毒液混合发生反应:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为____ ,X是一种有毒的气体,常有因此而发生中毒的事件,所以不可以把洁厕灵与84消毒液混合使用。
(2)接着她们又对厨房进行了清理:
①在调料柜中发现了两包标签模糊的白色粉末状物质,妈妈回忆说是淀粉和纯碱,小华做了一个简单的实验就将二者区分开了。她的实验方法是________ ;
②妈妈发现一口铝锅表面发黄,就用钢丝球进行擦洗。小华发现后立即予以制止,她的理由是______ 。
(3)打扫过程中小华发现家中好几部报废的手机。科学的迅速发展,导致手机产品的更迭加速。我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。能否回收其中的铜?为此小华与班级化学兴趣小组设计并进行了如下实验。已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。

①将电路板粉碎成粉末的目的是________________ 。
②步骤A所得滤液中的溶质除硫酸外,还有_______________ 。
③步骤B中的实验现象是:固体部分溶解,_____________ 。
④步骤D中反应的化学方程式是_____________ 。
(1)清理卫生间的过程中,她使用了洗洁精、洁厕灵和84消毒液三种清洁剂,查阅资料得知其有效成分如表所示:
| 名称 | 洗洁精 | 洁厕灵 | 84消毒液 |
| 有效成分 | 表面活性剂、NaOH | HCl | NaClO |
①据其有效成分可知洗洁精呈
②84消毒液中的NaClO在类别上属于(选填序号)
③小华认为洁厕灵可用于铁制品表面除锈,发生反应的化学方程式为
④查阅资料知:洁厕灵与84消毒液混合发生反应:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为
(2)接着她们又对厨房进行了清理:
①在调料柜中发现了两包标签模糊的白色粉末状物质,妈妈回忆说是淀粉和纯碱,小华做了一个简单的实验就将二者区分开了。她的实验方法是
②妈妈发现一口铝锅表面发黄,就用钢丝球进行擦洗。小华发现后立即予以制止,她的理由是
(3)打扫过程中小华发现家中好几部报废的手机。科学的迅速发展,导致手机产品的更迭加速。我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。能否回收其中的铜?为此小华与班级化学兴趣小组设计并进行了如下实验。已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。

①将电路板粉碎成粉末的目的是
②步骤A所得滤液中的溶质除硫酸外,还有
③步骤B中的实验现象是:固体部分溶解,
④步骤D中反应的化学方程式是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属在生产生活中有着广泛的应用。

(1)利用金属导热性的实例之一是__________ 。
(2)铝制品具有很强的抗腐蚀性,原因是__________ (用化学方程式表示)。
(3)合金是重要的金属材料,图中能表示锡铅合金熔点的是__________ (选填“a”“b”或“c”)。
(4)金属钛在航天、军事、医学等领域有广泛的应用。常温下,钛不溶于水,不和溶质质量分数小于5%的稀盐酸和稀硫酸反应。工业上常用金红石(含有TiO2)大规模生产钛,反应流程如下:

①写出反应Ⅰ的化学方程式:__________ ;
②请设计从Ti和Mg的混合物中获得纯净金属钛的实验方案:__________ 。

(1)利用金属导热性的实例之一是
(2)铝制品具有很强的抗腐蚀性,原因是
(3)合金是重要的金属材料,图中能表示锡铅合金熔点的是
(4)金属钛在航天、军事、医学等领域有广泛的应用。常温下,钛不溶于水,不和溶质质量分数小于5%的稀盐酸和稀硫酸反应。工业上常用金红石(含有TiO2)大规模生产钛,反应流程如下:

①写出反应Ⅰ的化学方程式:
②请设计从Ti和Mg的混合物中获得纯净金属钛的实验方案:
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
【推荐3】已知一种固体化合物由C、H、O、Cu四种元素组成。向盛有该化合物的试管中加入稀盐酸,产生大量气泡,固体逐渐溶解,得到蓝色溶液。已知这种蓝色溶液是氯化铜溶液。
(1)探究产生的气体是什么。
(猜想)①可能是氢气;②____ ③____ 。(填两种即可)
(实验)请你针对②和③猜想中的一种,设计实验,验证你的猜想。_____
(2)从蓝色溶液中提取金属铜。现利用该溶液制取金属铜,过程如下:
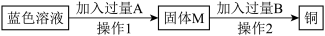
①加入过量的A的目的是____ ,反应化学方程式为____ 。
②加入足量B的目的是____ ,如何确定此目的已经达到? ________ 。
(3)已知“铜锈”的主要成分是碱式碳酸铜,其化学式为Cu2(OH)2CO3。请推测“铜锈”是铜与空气中的______ 共同作用的结果。试写出用稀盐酸除去“铜锈”的化学方程式________ 。
(1)探究产生的气体是什么。
(猜想)①可能是氢气;②
(实验)请你针对②和③猜想中的一种,设计实验,验证你的猜想。
(2)从蓝色溶液中提取金属铜。现利用该溶液制取金属铜,过程如下:

①加入过量的A的目的是
②加入足量B的目的是
(3)已知“铜锈”的主要成分是碱式碳酸铜,其化学式为Cu2(OH)2CO3。请推测“铜锈”是铜与空气中的
您最近一年使用:0次



