28.7g的氯化钠和硝酸钠的混合物,溶于100g水中,向所得溶液中加入134g的硝酸银溶液,恰好完全反应,得到溶液的质量是234g.计算:原混合物中钠元素的质量分数.(已知:AgNO3+NaCl=AgCl↓+NaNO3;计算结果精确到1%)
2012·山东聊城·中考模拟 查看更多[4]
(已下线)2012届山东省东阿县第二中学中考模拟2化学试卷(已下线)2012届北京市东城区中考二模化学试卷(已下线)2013-2014北京市延庆区中考一模化学试卷北京市第156中学2019届九年级下学期中考综合模拟化学试题
更新时间:2016-11-28 11:14:47
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】金属电镀前需进行除油处理,碳酸钠和氢氧化钠的混合物可用于配制碱性除油液。兴趣小组取 3.3g 该混合物,加水配制成 45g 样品溶液,分成三等份,分别加入不同质量的氯化钙溶液,测定充分反应后生成沉淀的质量如下表,请计算:
(1)配制样品溶液需用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和______ ,称取样品时,不能放在纸片上直接称量,其原因是________ 。
(2)三次实验中恰好完全反应的实验序号为_______ 。
(3)计算样品中碳酸钠的质量分数。(写出计算过程,结果精确到 0.1%)
(4)实验 1 所得滤液中含有的溶质有______ (用符号表示)。
| 实验序号 | 1 | 2 | 3 |
| 加入氯化钙溶液的质量/g | 10 | 20 | 30 |
| 生成沉淀的质量/g | 0.25 | 0.5 | 0.5 |
(2)三次实验中恰好完全反应的实验序号为
(3)计算样品中碳酸钠的质量分数。(写出计算过程,结果精确到 0.1%)
(4)实验 1 所得滤液中含有的溶质有
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】探究质量守恒定律时,老师将10g铁钉放入足量硫酸铜溶液中,得到了6.4g的铜单质。实验过程中使用的铁钉并非纯铁(杂质不参与反应)。
按要求回答下列问题:
(1)根据实验分析,该反应______ (填“是”或“否”)遵循质量守恒定律。
(2)列式计算该铁钉样品中铁单质的质量分数。(要求写出计算过程)
(3)在给出的坐标上,画出反应过程中固体总质量随参加反应的Fe的质量变化的关系曲线,并标出相关坐标点。

按要求回答下列问题:
(1)根据实验分析,该反应
(2)列式计算该铁钉样品中铁单质的质量分数。(要求写出计算过程)
(3)在给出的坐标上,画出反应过程中固体总质量随参加反应的Fe的质量变化的关系曲线,并标出相关坐标点。

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】现有碳酸钙、氯化钙组成的混合物样品。小军想计算混合物中各成分的质量,进行了如下图所示的实验:

请回答。下列问题:
(1)写出发生反应的化学方程式____________________________;
(2)列出求解生成沉淀质量x的比例式______________________;
(3)混合物样品中各成分的质量比为____________________;
(4)在加入碳酸钠溶液的过程中,烧杯中溶质质量的变化情况为_____________________;
(5)若最终所得的不饱和溶液B的溶质的质量分数为5%,则加入水的质量为__________。

请回答。下列问题:
(1)写出发生反应的化学方程式____________________________;
(2)列出求解生成沉淀质量x的比例式______________________;
(3)混合物样品中各成分的质量比为____________________;
(4)在加入碳酸钠溶液的过程中,烧杯中溶质质量的变化情况为_____________________;
(5)若最终所得的不饱和溶液B的溶质的质量分数为5%,则加入水的质量为__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】已知某溶液中的溶质可能是HCl、NaOH、CaCl2中的一种或两种,为确定该溶液中溶质的成分及含量,进行以下实验。
(1)取少量溶液于试管中,滴入2滴无色酚酞试液,酚酞不变色,溶液中一定不存在____。
(2)为了进一步测定成分及含量,重新取120g溶液于烧杯中,逐滴加入20.0%的Na2CO3溶液,测得滴加溶液的质量与产生沉淀的关系(图1)和滴加溶液的质量与烧杯中溶液的pH关系(图2)。 (已知: CaCl2溶液呈中性)回答下列问题

①该溶液中溶质的化学式为_________
②计算溶液中氯化氢的质量分数。(写出计算过程)
③m1=_____ g;m2=____g.
(1)取少量溶液于试管中,滴入2滴无色酚酞试液,酚酞不变色,溶液中一定不存在____。
(2)为了进一步测定成分及含量,重新取120g溶液于烧杯中,逐滴加入20.0%的Na2CO3溶液,测得滴加溶液的质量与产生沉淀的关系(图1)和滴加溶液的质量与烧杯中溶液的pH关系(图2)。 (已知: CaCl2溶液呈中性)回答下列问题

①该溶液中溶质的化学式为_________
②计算溶液中氯化氢的质量分数。(写出计算过程)
③m1=_____ g;m2=____g.
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】菱铁矿(主要成分是FeCO3)是炼铁的原料,现取20. 0g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。

(1)完成化学反应方程式: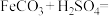 _____
_____
(2)20. 0g菱铁矿中FeCO3的质量分数为_____;
(3)列式计算恰好完全反应时,所得溶液的质量;
(4)向上述所得溶液中加入_____g 水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。

(1)完成化学反应方程式:
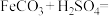 _____
_____
(2)20. 0g菱铁矿中FeCO3的质量分数为_____;
(3)列式计算恰好完全反应时,所得溶液的质量;
(4)向上述所得溶液中加入_____g 水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。
您最近一年使用:0次



