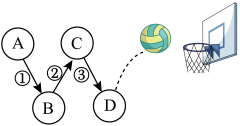
A-E为初中化学五种不同类别的常见物质。已知A和B可配制波尔多液,D中金属元素的质量分数为70%,E为世界年产量最高的金属。它们之间相互关系如图所示,图中“—”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)。请回答下列问题:
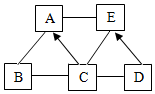
(1)物质B的另外一种用途_________ ;
(2)写出D→E反应的化学方程式为_________ ;
(3)写出C和D反应的化学方程式为_________ 。

(1)物质B的另外一种用途
(2)写出D→E反应的化学方程式为
(3)写出C和D反应的化学方程式为
更新时间:2022/04/15 15:31:09
|
相似题推荐
【推荐1】某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性,按如图所示进行实验(滤纸条用酚酞试液浸泡并晾干)。已知NH4HCO3 NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4。
NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4。_______ ,B中氢氧化钠固体的作用是①干燥气体;②_______ (用化学方程式表示)。
(2)E烧杯中液面上倒置的漏斗的作用是_______ 。该同学看到现象_______ ,得出了正确的结论。
 NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4。
NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4。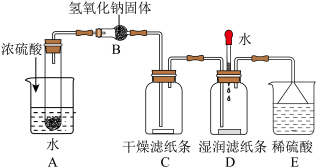
(2)E烧杯中液面上倒置的漏斗的作用是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】高纯硅的制备以石英砂(主要成分是二氧化硅)为原料,生产过程示意图如下图。
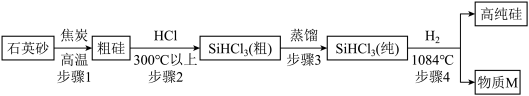
(1)上述四个步骤中属于物理变化的是步骤_____ 。
(2)二氧化硅的化学式是_____ 。
(3)物质M是该生产过程中可循环使用的物质,写出步骤4中发生反应的化学方程式:_____ ,反应的基本类型是_____ 。

(1)上述四个步骤中属于物理变化的是步骤
(2)二氧化硅的化学式是
(3)物质M是该生产过程中可循环使用的物质,写出步骤4中发生反应的化学方程式:
您最近一年使用:0次
【推荐3】化学助力科技强国。请根据你所学的化学知识回答下列问题:
(1)“碳捕捉与封存”是我国的一项先进技术,运用“碳捕捉与封存”技术,这些CO2将不会进入大气,将被压到地下或海水中封存,该技术有利于控制______ 的加剧。
(2)我国“手撕钢”材料处于国际领先,其厚度不足0.02mm,只有A4纸的四分之一,可用于“折叠屏手机”屏等。将钢板轧成“手撕钢”,利用了金属的______ 性。
(3)由北京理工大学孙逢春院士牵头的北京冬奥会新能源汽车项目团队研发的锂离子动力电池,在40℃环境下可一键启动新能源汽车。该电池在工作时能量转化形式为______ 能转化成电能。某品牌新能源汽车定位系统微电脑控制器应用了一种新型材料氮化铝(A1N)。工业上在氮气流中由氧化铝与焦炭在高温条件下制得氮化铝,并生成一种可燃性气体,该反应的化学方程式为______ 。
(1)“碳捕捉与封存”是我国的一项先进技术,运用“碳捕捉与封存”技术,这些CO2将不会进入大气,将被压到地下或海水中封存,该技术有利于控制
(2)我国“手撕钢”材料处于国际领先,其厚度不足0.02mm,只有A4纸的四分之一,可用于“折叠屏手机”屏等。将钢板轧成“手撕钢”,利用了金属的
(3)由北京理工大学孙逢春院士牵头的北京冬奥会新能源汽车项目团队研发的锂离子动力电池,在40℃环境下可一键启动新能源汽车。该电池在工作时能量转化形式为
您最近一年使用:0次
【推荐1】按要求用化学用语填空:
(1)纯碱中的阴离子:______ ;
(2)炉具清洁剂中去污的成分:______ ;
(3)赤铁矿的主要成分:______ ;
(4)标出过氧化氢中氧元素的化合价:______ ;
(5)保持氦气化学性质的微粒______ ;
(6)鉴别氯化铵和氯化钠:(用化学方程式表示)______ 。
(1)纯碱中的阴离子:
(2)炉具清洁剂中去污的成分:
(3)赤铁矿的主要成分:
(4)标出过氧化氢中氧元素的化合价:
(5)保持氦气化学性质的微粒
(6)鉴别氯化铵和氯化钠:(用化学方程式表示)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】铁是一种重要的金属材料。
(1)工业上用 和赤铁矿(主要成分
和赤铁矿(主要成分 )炼铁的化学方程式为
)炼铁的化学方程式为________ 。
(2)下列矿石可以用于炼铁的是________(填字母序号)
(3)铁生锈的条件为________ 。
(1)工业上用
 和赤铁矿(主要成分
和赤铁矿(主要成分 )炼铁的化学方程式为
)炼铁的化学方程式为(2)下列矿石可以用于炼铁的是________(填字母序号)
A.铝土矿(主要成分 ) ) |
B.磁铁矿(主要成分 ) ) |
C.白云石矿[主要成分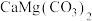 ] ] |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】锂被誉为“新能源金属”、“金属味精”和“推动世界前进的金属”,具有极高的战略价值。碳酸锂是生产金属锂制品的基础材料。以β-锂辉石为原料,用硫酸焙烧法制取碳酸锂的工艺流程(部分试剂和步骤等已略去)如下。
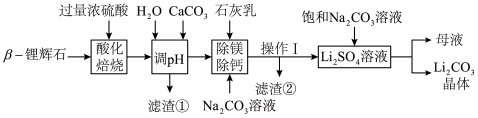
【资料】
①β-锂辉石的主要成分是Li2O·Al2O3·4SiO2,含少量Ca、Mg元素。
②
(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是___________ 。
(2)“调pH”步骤中,加入CaCO3的作用是___________ 。
(3)在“除镁除钙”步骤中,先加入石灰乳,再加入Na2CO3溶液。添加试剂的顺序不能调换,其原因是___________ 。
(4)操作I的名称为___________ ,滤渣②的成分是___________ 。
(5)Li2CO3和Li2SO4的溶解度如下表所示:
为了提高产品的纯度,需要将得到的晶体洗涤,需选用___________ ℃的水。

【资料】
①β-锂辉石的主要成分是Li2O·Al2O3·4SiO2,含少量Ca、Mg元素。
②

(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是
(2)“调pH”步骤中,加入CaCO3的作用是
(3)在“除镁除钙”步骤中,先加入石灰乳,再加入Na2CO3溶液。添加试剂的顺序不能调换,其原因是
(4)操作I的名称为
(5)Li2CO3和Li2SO4的溶解度如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】N是空气中含量最高的元素。
(1)将含N物质进行分类,按要求写出化学式
(2)镓元素的信息如图。
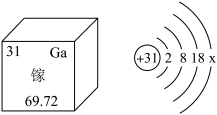
请设计理论上制备硝酸镓的三种方案(要求含镓原料分别属于不同的化合物类别)
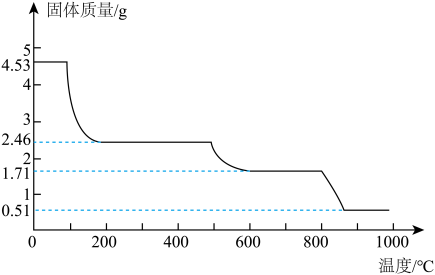
(3)若硫酸铝依晶体[NH4Al(SO4)2]·12H2O,相对分子质量453]
①加热过程中,其质量随时间的变化如图所示。据此判断,从200℃到50℃间固体是否还存在结晶水,并作出解释。_______ (是或否),_______ 。
②写出一个能与硫酸铝溶液发生反应的原子团_______ 。(写离子符号)
(1)将含N物质进行分类,按要求写出化学式
| 单质 | 引起酸雨的氧化物 | 酸 | 含氮的不同化合价的盐 |
| N2 | HNO3 |

请设计理论上制备硝酸镓的三种方案(要求含镓原料分别属于不同的化合物类别)
| 方案 | 预期反应的化学方程式 |
| ① | |
| ② | |
| ③ |
①加热过程中,其质量随时间的变化如图所示。据此判断,从200℃到50℃间固体是否还存在结晶水,并作出解释。

②写出一个能与硫酸铝溶液发生反应的原子团
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A~H是初中化学常见的物质,其中A是发酵粉的主要成分之一,B是常用调味品,E、F的俗称分别是熟石灰、纯碱。它们之间的相互转化关系如图所示。
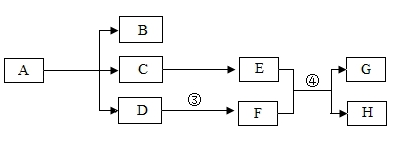
(1)写出A、B的化学式:A___________ B__________ ;
(2)在物质的分类中,D属于_________ (填“酸”、“碱”、“盐”或“氧化物”);
(3)图中④反应化学方程式为_______________________________________ 。

(1)写出A、B的化学式:A
(2)在物质的分类中,D属于
(3)图中④反应化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A~E是初中化学常见的5种物质,已知A和E是黑色固体,B常温下是液体,D是白色固体。它们之间的反应关系如图所示(部分物质已略去),“→”指一种物质可反应生成另一种物质,“一”指两种物质可发生反应。
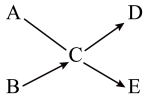
(1)请写出下列物质的名称:A______ ;D______ 。
(2)B→C反应的文字表达式为______ 。
(3)C→E反应的文字表达式为______ 。

(1)请写出下列物质的名称:A
(2)B→C反应的文字表达式为
(3)C→E反应的文字表达式为
您最近一年使用:0次