新型冠状病毒肺炎威胁着人们的身体健康。为杀灭新型冠状病毒,84消毒液、过氧乙酸、75%的消毒酒精等医用消毒剂走进了百姓家。
资料一:84消毒液[有效成分为次氯酸钠(NaClO)]和ClO2,是常用含氯消毒剂。
资料二:酒精易挥发、易燃,常用作酒精灯和内燃机的燃料。使用75%的酒精消毒时一定要注意防火!
资料三:过氧乙酸(C2H4O3)是一种高效消毒剂。
回答下列问题:
(1)NaClO属于______(填字母序号)。
(2)ClO2的名称为______ 。
(3)从资料二中可归纳出酒精的物理性质是______ ,酒精的用途是______ 。
(4)实验中,不小心将酒精灯碰倒在桌上燃烧起来,简单的灭火措施是______ 。
(5)下列仪器不能用酒精灯加热的是______(填字母序号)。
(6)过氧乙酸(C2H4O3)分子中碳、氢、氧的原子个数比是______ ,过氧乙酸中碳元素的质量分数为______ (精确到0.1%)。
资料一:84消毒液[有效成分为次氯酸钠(NaClO)]和ClO2,是常用含氯消毒剂。
资料二:酒精易挥发、易燃,常用作酒精灯和内燃机的燃料。使用75%的酒精消毒时一定要注意防火!
资料三:过氧乙酸(C2H4O3)是一种高效消毒剂。
回答下列问题:
(1)NaClO属于______(填字母序号)。
| A.混合物 | B.化合物 | C.氧化物 |
(3)从资料二中可归纳出酒精的物理性质是
(4)实验中,不小心将酒精灯碰倒在桌上燃烧起来,简单的灭火措施是
(5)下列仪器不能用酒精灯加热的是______(填字母序号)。
| A.燃烧匙 | B.试管 | C.量筒 | D.蒸发皿 |
更新时间:2022-04-16 22:29:02
|
相似题推荐
【推荐1】阅读下列短文,回答问题。
富氧水是以饮用水为基质,加压充入氧气制得的。普通饮用水常温条件下的溶解氧含量通常介于6~8mg/L,而国内外市场中的富氧水中的溶解氧含量一般在40~150mg/L。富氧水对健康的影响,学术界一直存在争议。有研究认为若水中氧含量过高或常喝富氧水会加速氧化,使人体衰老。无论是吸氧还是喝氧,对健康人都是弊多利少。人们在“喝氧”的问题上应采取慎重态度,勿做非明智的选择。
(1)从上述短文可以看出氧气的化学性质是___________ 。
(2)生活中若要降低富氧水的硬度,可用___________ 的方法。
(3)普通饮用水净化过程中,除去颜色和气味,所用的物质是___________ 。
(4)下列有关富氧水的说法正确的是___________。(填字母)
富氧水是以饮用水为基质,加压充入氧气制得的。普通饮用水常温条件下的溶解氧含量通常介于6~8mg/L,而国内外市场中的富氧水中的溶解氧含量一般在40~150mg/L。富氧水对健康的影响,学术界一直存在争议。有研究认为若水中氧含量过高或常喝富氧水会加速氧化,使人体衰老。无论是吸氧还是喝氧,对健康人都是弊多利少。人们在“喝氧”的问题上应采取慎重态度,勿做非明智的选择。
(1)从上述短文可以看出氧气的化学性质是
(2)生活中若要降低富氧水的硬度,可用
(3)普通饮用水净化过程中,除去颜色和气味,所用的物质是
(4)下列有关富氧水的说法正确的是___________。(填字母)
| A.属于混合物 | B.与水的性质完全相同 | C.应大量喝富氧水 |
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下面的短文,回答有关问题。
为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂——ClO2在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,熔点-59℃,沸点11℃。在常温下,1L水中大约能溶解2.9gClO2;ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085%Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂。我国从2000年起就逐渐用ClO2取代氯气(Cl2)对饮用水进行消毒,以减少水中有害的含氯物质。
(1)ClO2的名称是___________ ,分子中氯元素的化合价是___________ 。
(2)下列消毒剂中,不属于“含氯消毒剂”的是___________(填字母序号)。
(3)ClO2的化学性质有___________ 、___________ (写出两点即可)。
(4)下列有关ClO2的说法错误的是___________(填字母序号)。
(5)ClO2遇热水生成次氯酸和氯气、氧气,该反应的文字表达式是___________ 。
(6)化学式ClO2在宏观上表示物质的组成,还能表示___________ ;在微观上可以表示一个___________ 。
为抑制新冠病毒传播,“含氯消毒剂”被广泛使用,其中就包含一种新型灭菌消毒剂——ClO2在通常情况下,ClO2是一种有刺激性气味的黄绿色气体,熔点-59℃,沸点11℃。在常温下,1L水中大约能溶解2.9gClO2;ClO2受热或者见光易分解,具有强氧化性和很强的腐蚀性。含有2%的ClO2和0.085%Na2CO3的水溶液无色、无臭、无腐蚀性,常温下稳定,不易分解;该溶液用于杀菌、消毒的同时,还有除臭、防霉、保鲜等作用,是特性优良,高效安全的消毒剂。我国从2000年起就逐渐用ClO2取代氯气(Cl2)对饮用水进行消毒,以减少水中有害的含氯物质。
(1)ClO2的名称是
(2)下列消毒剂中,不属于“含氯消毒剂”的是___________(填字母序号)。
| A.84消毒液(含NaClO) | B.双氧水(H2O2) |
| C.氯气(Cl2) | D.过氧乙酸(C2H4O3) |
(4)下列有关ClO2的说法错误的是___________(填字母序号)。
| A.0℃时,ClO2为黄绿色气体 |
| B.常温下,水中能溶解一定量的ClO2 |
| C.用棕色试剂瓶盛装ClO2并置于冷暗处保存 |
| D.用于饮用水消毒,ClO2比氯气更安全 |
(6)化学式ClO2在宏观上表示物质的组成,还能表示
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下列短文,回答相关文献题。
过氧化氢可用于消毒杀菌,具有不稳定性,常温下会分解。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。过氧化氢的产生量与温度、湿度等环境条件密切相关。当使用硅材料、相对湿度为55%时,得到过氧化氢的最大浓度随温度变化关系如图所示。

(1)过氧化氢可用于消毒杀菌,这是利用了过氧化氢的______ (填“物理”或“化学”)性质。
(2)过氧化氢不稳定的原因是______ (用化学反应方程式表示)。
(3)图中a点(-2.8℃)未生成过氧化氢的原因可能是____________ 。
(4)水和过氧化氢组成元素相同但化学性质不同的原因是____________ 。
(5)下列说法错误的是______。
过氧化氢可用于消毒杀菌,具有不稳定性,常温下会分解。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。过氧化氢的产生量与温度、湿度等环境条件密切相关。当使用硅材料、相对湿度为55%时,得到过氧化氢的最大浓度随温度变化关系如图所示。

(1)过氧化氢可用于消毒杀菌,这是利用了过氧化氢的
(2)过氧化氢不稳定的原因是
(3)图中a点(-2.8℃)未生成过氧化氢的原因可能是
(4)水和过氧化氢组成元素相同但化学性质不同的原因是
(5)下列说法错误的是______。
| A.水蒸气在冷凝过程中可能发生化学变化 |
| B.水蒸气在玻璃表面冷凝得到的液滴一定为纯净物 |
| C.一定条件下,水蒸气冷凝可用于材料表面的绿色消毒 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某研究小组模拟工业利用黄铜矿(主要含CuFeS2、SiO2,其中SiO2及少量其他杂质不参与反应且难溶于水)制备胆矾晶体(CuSO4·5H2O),其流程如图所示:
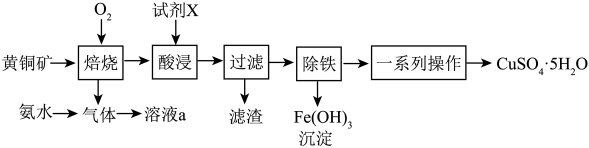
请回答下列问题:
(1)“焙烧”前,常将黄铜矿粉碎,其目的是______ 。
(2)CuFeS2在“焙烧”后生成三种常见的氧化物,其中一种为红棕色固体,请写出该化学反应方程式______ 。
(3)“酸浸”时使用的试剂X为______ ,“滤渣”的主要成分为______ 。(写化学式)
(4)为了从溶液中得到胆矾晶体,进行的“一系列操作”为蒸发浓缩、______ 、过滤、洗涤、干燥。

请回答下列问题:
(1)“焙烧”前,常将黄铜矿粉碎,其目的是
(2)CuFeS2在“焙烧”后生成三种常见的氧化物,其中一种为红棕色固体,请写出该化学反应方程式
(3)“酸浸”时使用的试剂X为
(4)为了从溶液中得到胆矾晶体,进行的“一系列操作”为蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】根据微观示意图回答下列问题。
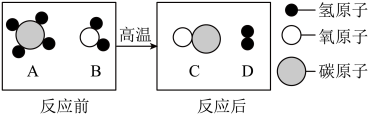
(1)在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如下所示。①A,B,C,D四种物质中,属于氧化物的是_________________ (请用化学式表示)②写出该反应的化学方程式 __________________ 在该反应中,生成C和D的质量比为 ______________________
(2)下图是CO与O2反应的微观示意图,反应前后没有发生变化的粒子是___________ (填序号)

A.①② B.②③ C.③④ D.④⑤

(1)在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如下所示。①A,B,C,D四种物质中,属于氧化物的是
(2)下图是CO与O2反应的微观示意图,反应前后没有发生变化的粒子是

A.①② B.②③ C.③④ D.④⑤
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面科普短文。
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。

由上图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用是热门研究方向之一、例如,通过光催化可将H2O、CO2转化为H2、CO、CH4、CH3OH(甲醇)等太阳能燃料,示意图如下左图。
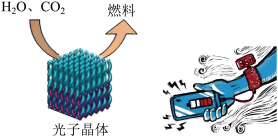
随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(BiTes)/纤维素复合热点薄膜电池",能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(如上右图)。
在新能源的开发和利用中,化学起着不可替代的作用,
依据短文内容回答下列问题:
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是_____ 、_____ 。
(2)复合热点薄膜电池中碲化铋(Bi2Te3)由_____ 种元素组成。
(3)H2O、CO2转化得到的太阳能燃料中,属于氧化物的是_____ ;该过程属于_____ (填“物理”或“化学”)变化。
(4)下列说法正确的是_____(填字母)。
化石能源是目前应用最广泛的能源,但其储量有限,不可再生。《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低碳转型。

由上图可见,太阳能、风能等其他可再生能源在能源结构中所占比例日益增多。太阳能的利用是热门研究方向之一、例如,通过光催化可将H2O、CO2转化为H2、CO、CH4、CH3OH(甲醇)等太阳能燃料,示意图如下左图。

随着科技的进步,能源将得到更充分的利用。例如,利用照明灯、人体散发的热量灯生活中随处可见的废热发电。我国研发的“柔性、可裁剪碲化铋(BiTes)/纤维素复合热点薄膜电池",能充分贴合人体体表,实现利用体表散热为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(如上右图)。
在新能源的开发和利用中,化学起着不可替代的作用,
依据短文内容回答下列问题:
(1)比较2015、2030和2050年能源结构中的化石能源,所占比例降低的是
(2)复合热点薄膜电池中碲化铋(Bi2Te3)由
(3)H2O、CO2转化得到的太阳能燃料中,属于氧化物的是
(4)下列说法正确的是_____(填字母)。
| A.生活中的废热可转化为电能 |
| B.石油和太阳能都属于可再生能源 |
| C.科技进步会促进能源的利用 |
| D.能源结构向多元、清洁、低碳转型 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水和过氧化氢发生分解反应都能生成氧气,小明同学发现取质量均为34克的H2O和H2O2充分发生分解反应后,H2O2生成的氧气的质量较小,他进行了以下计算与思维过程,最终明白了原因。
(1)请计算,34克H2O2中氧元素的质量_______ ,34克H2O中氧元素的质量_______ (保留小数点后一位)。
(2)请写出通电分解水的符号表达式_____ ,过氧化氢制取氧气反应的符号表达式____ 。
(3)请解释H2O2分解生成的O2质量较小的原因_____ 。
(1)请计算,34克H2O2中氧元素的质量
(2)请写出通电分解水的符号表达式
(3)请解释H2O2分解生成的O2质量较小的原因
您最近一年使用:0次
【推荐2】请回答下列问题。
(1)若用如图所示装置制取氧气,请将气体收集装置补画完整______ 。

(2)现有一种铁矿石含氧化铁(Fe2O3)。某铁矿厂实验室取样200 g该铁矿石,经研究其中所含铁元素的质量为98 g,请你帮助他们计算一下该铁矿石中氧化铁的百分含量:_______ 。
(1)若用如图所示装置制取氧气,请将气体收集装置补画完整

(2)现有一种铁矿石含氧化铁(Fe2O3)。某铁矿厂实验室取样200 g该铁矿石,经研究其中所含铁元素的质量为98 g,请你帮助他们计算一下该铁矿石中氧化铁的百分含量:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】(1)按要求从氮气、氧气、一氧化碳、氯化银、氢氧化铜、碳酸氢钠中选择合适的物质,将其化学式填写在下列横线上。
①一种能供给呼吸的气体_____ ;
②一种可作还原剂的氧化物_____ ;
③一种难溶性的碱_____ ;
④一种可作发酵粉的盐_____ 。
(2)材料,通常被视为人类社会进化的里程碑,对于材料的认和利用能力,往往决定着社会的形态与人类生活的质量,称人类文明史称为世界材料史毫不为过。当历史进入20世纪下半叶开始的新技术革命时代后,新材料已成为各个高技术领域发展的突破口,没有新材料的开发应用,便谈不上新的技术产品和产业进步。
①我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式H25N34O3Cl)该物质是超高能材料。具有高密度,高爆轰性能等优点,在航空航天上可做推进剂,未来军事火药方面有重大意义。该全氮阴离子盐属于_____ (选填“混合物”“有机物”“无机物”之一),它的一个分子中含有_____ 个原子。
②科学家研发出一种高强度钢化平板玻璃,强度较之普通玻璃提高数倍,承载能力增大,改善了易碎性质,使用安全,可广泛应用在建筑工程行业中。生产玻璃的原材料有石英砂、纯碱、石灰石等,在纯碱的主要成分Na2CO3,中,所含元素的质量分数最小的元素是_____ (填元素名称)。
③稀土高铁铝合金电缆是具有国际先进技术和自主知识产权的新型材料,广泛应用于高铁建设中。制作电缆材料的原料之一是乙烯基三甲氧基硅烷(C5H12O3Si)。在乙烯基三甲氧基硅烷商甲氧基硅烷中碳、氢两种元素的质量比为_____ (填最简整数比)在它一个分子中氢、氧两元素原子个数之比为_____ (填最简整数比)。
④诺贝尔化学奖曾授予进行“钯催化交叉偶联反应”研究的三化位化学家,他们采用钯催化将碳原子连接在起制造新的有机材料。下列说法不正确的是_____ (选填下列序号之一)。
A 该制造过程属于化学变化
B 钯催化剂能催化所有的反应
C 这项研究有利于人类合成复杂分子
D 利用该技术能改变合成途径,降低反应发生的条件
①一种能供给呼吸的气体
②一种可作还原剂的氧化物
③一种难溶性的碱
④一种可作发酵粉的盐
(2)材料,通常被视为人类社会进化的里程碑,对于材料的认和利用能力,往往决定着社会的形态与人类生活的质量,称人类文明史称为世界材料史毫不为过。当历史进入20世纪下半叶开始的新技术革命时代后,新材料已成为各个高技术领域发展的突破口,没有新材料的开发应用,便谈不上新的技术产品和产业进步。
①我国科学家最近成功合成了世界上首个全氮阴离子盐(化学式H25N34O3Cl)该物质是超高能材料。具有高密度,高爆轰性能等优点,在航空航天上可做推进剂,未来军事火药方面有重大意义。该全氮阴离子盐属于
②科学家研发出一种高强度钢化平板玻璃,强度较之普通玻璃提高数倍,承载能力增大,改善了易碎性质,使用安全,可广泛应用在建筑工程行业中。生产玻璃的原材料有石英砂、纯碱、石灰石等,在纯碱的主要成分Na2CO3,中,所含元素的质量分数最小的元素是
③稀土高铁铝合金电缆是具有国际先进技术和自主知识产权的新型材料,广泛应用于高铁建设中。制作电缆材料的原料之一是乙烯基三甲氧基硅烷(C5H12O3Si)。在乙烯基三甲氧基硅烷商甲氧基硅烷中碳、氢两种元素的质量比为
④诺贝尔化学奖曾授予进行“钯催化交叉偶联反应”研究的三化位化学家,他们采用钯催化将碳原子连接在起制造新的有机材料。下列说法不正确的是
A 该制造过程属于化学变化
B 钯催化剂能催化所有的反应
C 这项研究有利于人类合成复杂分子
D 利用该技术能改变合成途径,降低反应发生的条件
您最近一年使用:0次



