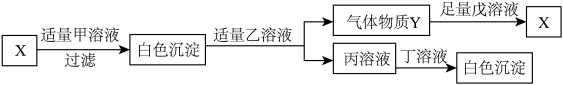
实验室有以下四组未贴标签溶液,需要对每组内两种溶液加以区分。
提供的试剂:a.氯化钡溶液 b.碳酸钠溶液 c.二氧化碳 d.稀盐酸
在提供的试剂中(每种试剂只能使用一次),能鉴别I、II、III三组溶液的试剂,依次是____ 、_____ 、______ (用字母“a”“b”“c”“d”表示)。写出第IV组鉴别时发生反应的化学方程式_______ 。
| I.碳酸钠、氢氧化钠 | II.氢氧化钙、氢氧化钠 |
| III.氢氧化钙、氯化钙 | IV.稀盐酸、稀硫酸 |
在提供的试剂中(每种试剂只能使用一次),能鉴别I、II、III三组溶液的试剂,依次是
2022·上海静安·二模 查看更多[1]
更新时间:2022-06-24 18:58:18
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】补全实验报告。
| 序号 | 目的 | 装置及操作 | 现象 | 解释或结论 | |
| (1) | 研究酸的化学性质 | 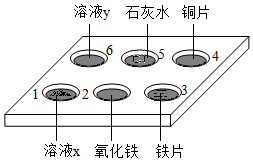 | 向3和4中滴加盐酸 | 盐酸能与F反应,不与Cu反应 | |
| (2) | 向2中滴加盐酸 | 固体减少,得到黄色溶液 | 化学方程式为 | ||
| (3) | 研究碱的化学性质 | 向5中滴加 | 产生白色沉淀 | 生成了难溶于水的白色碳酸钙 | |
| (4) | 向1和6中滴加紫色石蕊溶液 | 1中溶液变红,6中溶液变蓝 | 溶液x显酸性,溶液y显碱性 | ||
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】为了维护南海权益,我国在2012年宣布成立了三沙市。这是维护国家主权的象征,同时也是因为海洋资源十分丰富,有广泛的利用价值。其中通过海水晾晒即可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
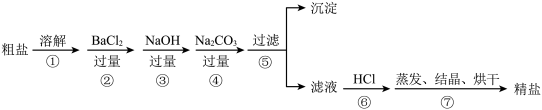
(1)根据以上信息,请写出海水中所含的主要阴离子的符号___________ 。
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的________ (填离子符号,下同),第④步加过量Na2CO3的目的是除去海水中和所加入试剂中的_____ 。第⑥步其实显示的是加适量盐酸,其目的是除去多余的___________ 。
(3)在第④步操作中,选择的除杂试剂不能用K2CO3代替Na2CO3,理由是______ 。

(1)根据以上信息,请写出海水中所含的主要阴离子的符号
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的
(3)在第④步操作中,选择的除杂试剂不能用K2CO3代替Na2CO3,理由是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列化学反应方程式:
(1)氢氧化钠溶液和硫酸铜溶液_____ 。
(2)硝酸银溶液和稀盐酸_____ 。
(3)稀硫酸除铁锈_____ 。
(4)硝酸钡溶液和硫酸溶液_____ 。
(5)碳酸钠溶液和氢氧化钙溶液_____ 。
(1)氢氧化钠溶液和硫酸铜溶液
(2)硝酸银溶液和稀盐酸
(3)稀硫酸除铁锈
(4)硝酸钡溶液和硫酸溶液
(5)碳酸钠溶液和氢氧化钙溶液
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A~H是初中化学常见的物质,下图所示为物质间相互转化关系图。其中B是一种可做干燥剂的氧化物,C气体可用于灭火,X是一种常见的酸,且只含有两种元素(其中部分反应物、生成物、反应条件已略去,箭头所指为生成物),请回答下列问题:

(1)H的化学式是_____________ ;
(2)反应①发生的条件是________________ ;
(3)反应②的基本类型是________ ;
(4)反应④的化学方程式_______________________ 。

(1)H的化学式是
(2)反应①发生的条件是
(3)反应②的基本类型是
(4)反应④的化学方程式
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】人类社会的文明进步与金属材料的发展关系密切。
(1)战国牛虎铜案,是云南青铜文化艺术的杰作。青铜是重要的铜合金,其硬度__ (填“大于”或“小于”)纯铜。
(2)铝能压制铝箔,是因为铝具有良好的_____ 。
(3)金属锈蚀会造成巨大浪费。下列做法能防止铁制品生锈的有___ 。(填字母序号)
A 水龙头表面镀铬
B 菜刀使用过后浸泡在食盐水中
C 自行车支架喷漆
D 保留铁栅栏表面的铁锈
(4)镁是一种银白色固体,密度为1.74g/cm3,熔点为650℃,沸点为1090℃,质地轻、有延展性。在空气中燃烧时会发出耀眼的白光,放热,生成白色固体。一些烟花和照明弹里都含有镁粉,就是利用了这一性质。镁还能和乙醇、水反应生成氢气。将镁条在酒精灯火焰上点燃,伸入盛有二氧化碳的集气瓶中,会观察到镁条剧烈燃烧,发生置换反应,反应结束后,可看到集气瓶内壁附着黑色固体碳(C)。依据文章内容,回答下列问题。
①写出镁具有的物理性质_____ (一条即可)。
②金属镁的用途有______ (一条即可)。
③如果存放在仓库中的少量金属镁发生了火灾,消防官兵可以选用_____ 灭火。
A 沙土 B 二氧化碳 C 水
(5)将一定量锌粉加入到适量硝酸铝、硝酸亚铁和硝酸银的混合溶液中,充分反应后,过滤,得到滤渣和滤液,下列说法正确的是_____ (填字母)。
A 滤液中一定含有的金属阳离子是Zn2+和A13+
B 若滤液为无色,则滤渣中一定有银和铁
C 取少量滤液,加入氯化钠溶液,无明显现象,则滤渣的组成有4种情况
D 取少量滤渣,加入过量稀盐酸,产生气泡,则滤渣中一定不含银
(1)战国牛虎铜案,是云南青铜文化艺术的杰作。青铜是重要的铜合金,其硬度
(2)铝能压制铝箔,是因为铝具有良好的
(3)金属锈蚀会造成巨大浪费。下列做法能防止铁制品生锈的有
A 水龙头表面镀铬
B 菜刀使用过后浸泡在食盐水中
C 自行车支架喷漆
D 保留铁栅栏表面的铁锈
(4)镁是一种银白色固体,密度为1.74g/cm3,熔点为650℃,沸点为1090℃,质地轻、有延展性。在空气中燃烧时会发出耀眼的白光,放热,生成白色固体。一些烟花和照明弹里都含有镁粉,就是利用了这一性质。镁还能和乙醇、水反应生成氢气。将镁条在酒精灯火焰上点燃,伸入盛有二氧化碳的集气瓶中,会观察到镁条剧烈燃烧,发生置换反应,反应结束后,可看到集气瓶内壁附着黑色固体碳(C)。依据文章内容,回答下列问题。
①写出镁具有的物理性质
②金属镁的用途有
③如果存放在仓库中的少量金属镁发生了火灾,消防官兵可以选用
A 沙土 B 二氧化碳 C 水
(5)将一定量锌粉加入到适量硝酸铝、硝酸亚铁和硝酸银的混合溶液中,充分反应后,过滤,得到滤渣和滤液,下列说法正确的是
A 滤液中一定含有的金属阳离子是Zn2+和A13+
B 若滤液为无色,则滤渣中一定有银和铁
C 取少量滤液,加入氯化钠溶液,无明显现象,则滤渣的组成有4种情况
D 取少量滤渣,加入过量稀盐酸,产生气泡,则滤渣中一定不含银
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】下列框图中的物质均为初中化学常见的物质,其中A是一种建筑材料的主要成分,B是黑色粉末,E溶液显碱性,F与H可用来配制波尔多液。下图是它们之间的相互转化关系。回答:
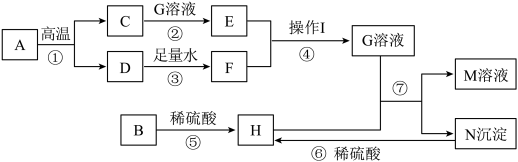
回答下列问题:
(1)写出物质的化学式:B___________ ,M___________ 。
(2)操作Ⅰ为___________ 。
(3)反应⑥的化学方程式为___________ 。

回答下列问题:
(1)写出物质的化学式:B
(2)操作Ⅰ为
(3)反应⑥的化学方程式为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】实验室有A、B、C、D、E、F六瓶溶液,另有六张写有Na2CO3、BaCl2、Ca(NO3)2、KCl、稀H2SO4、AgNO3的标签.现将部分瓶内溶液各取少许进行两两混合实验,结果如图所示(说明:“↓”表示生成沉淀、“↑”表示生成气体,“﹣”表示无明显变化或生成微溶物,空格表示该实验未做.)由实验结果:判断各瓶上应贴的标签是:A_____ ;B_____ ;C_____ ;D_____ ;E_____ ;F_____ 。


您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】实验员老师整理药品时,发现一瓶失去标签的白色固体,可能为NaCl、Na2CO3中的一种。取少量白色固体放入水中配成溶液,通过以下操作即可判断:
(1)若向配制溶液中加硝酸银溶液和稀硝酸,只出现白色沉淀,则是______________ ,
发生反应的化学方程式__________________________________________________ 。
(2)若向配制溶液中加稀盐酸,如有____________ 产生,则是___________________ 。
(1)若向配制溶液中加硝酸银溶液和稀硝酸,只出现白色沉淀,则是
发生反应的化学方程式
(2)若向配制溶液中加稀盐酸,如有
您最近一年使用:0次
【推荐3】追寻化学家的足迹,请你使用下图A~G的装置并像化学家一样进行实验研究。
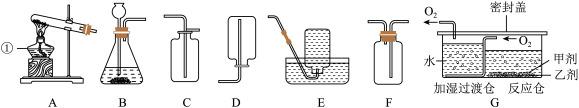
I、舍勒是最早制得氧气的化学家之一。他获得氧气的方法主要有:a.加热分解硝酸钾、氧化汞、碳酸银等;b.用二氧化锰与浓硫酸加热。
(1)图中仪器①的名称是______ 。如果要收集一瓶纯净的氧气,你最建议使用的收集装置是______ (填字母)。
(2)“便携式制氧器”装置可用于家庭输氧,其工作原理如图G所示。该装置使用甲试剂为白色固体(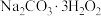 ),作制氧剂;乙试剂为二氧化锰,作催化剂。该制氧机的制氧原理有两步:
),作制氧剂;乙试剂为二氧化锰,作催化剂。该制氧机的制氧原理有两步:
第一步:
第二步:______ (用化学方程式表示)。
利用上述实验室仪器模拟组装该制氧机时,装置B相当于制氧机中的______ (填“反应仓”或“加湿过滤仓”)。
Ⅱ、我国化学家侯德榜发明了侯氏制碱法,为世界制碱工业技术发展作出杰出贡献。侯氏制碱法中重要的一步是向饱和食盐水中先后通入足量的氨气(极易溶于水)和二氧化碳制 。
。
(3)制备氨气。实验室常选择加热熟石灰和氯化铵固体混合物的方法制备氨气。制取氨气的发生装置可选图中的装置______ (填字母)。
(4)制备二氧化碳气体。实验室常用装置B制备二氧化碳,检查该装置气密性的方法是______ 。
(5)配制饱和食盐水。步骤为:计算、称量、______ 、溶解。
(6)制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是______(填字母)。

I、舍勒是最早制得氧气的化学家之一。他获得氧气的方法主要有:a.加热分解硝酸钾、氧化汞、碳酸银等;b.用二氧化锰与浓硫酸加热。
(1)图中仪器①的名称是
(2)“便携式制氧器”装置可用于家庭输氧,其工作原理如图G所示。该装置使用甲试剂为白色固体(
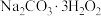 ),作制氧剂;乙试剂为二氧化锰,作催化剂。该制氧机的制氧原理有两步:
),作制氧剂;乙试剂为二氧化锰,作催化剂。该制氧机的制氧原理有两步:第一步:

第二步:
利用上述实验室仪器模拟组装该制氧机时,装置B相当于制氧机中的
Ⅱ、我国化学家侯德榜发明了侯氏制碱法,为世界制碱工业技术发展作出杰出贡献。侯氏制碱法中重要的一步是向饱和食盐水中先后通入足量的氨气(极易溶于水)和二氧化碳制
 。
。(3)制备氨气。实验室常选择加热熟石灰和氯化铵固体混合物的方法制备氨气。制取氨气的发生装置可选图中的装置
(4)制备二氧化碳气体。实验室常用装置B制备二氧化碳,检查该装置气密性的方法是
(5)配制饱和食盐水。步骤为:计算、称量、
(6)制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是______(填字母)。
| A.氯化钡溶液 | B.硝酸银溶液 | C.稀硝酸 | D.稀盐酸 |
您最近一年使用:0次