金泽钢铁公司从国外订购一批铁矿石(主要成分Fe2O3)。按照合同规定,铁矿石中氧化铁的质量分数不得低于80%。铁矿石到货后,技术人员称取样品20g,用质量分数为15%的稀盐酸150g与之恰好完全反应(杂质不与稀盐酸反应)。试计算:
(1)按照合同规定,此批铁矿石是否合格?
(2)铁矿石中铁元素的质量分数是多少?(计算结果保留1位小数)
(1)按照合同规定,此批铁矿石是否合格?
(2)铁矿石中铁元素的质量分数是多少?(计算结果保留1位小数)
更新时间:2022/07/05 07:22:51
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】氢化钙(CaH2)固体是登山运动员常用的能源提供剂,用它与水反应生成氢气供燃烧之需,反应的化学方程式为 。现有252 g氢化钙与足量的水反应,生成氢气的质量为多少克?
。现有252 g氢化钙与足量的水反应,生成氢气的质量为多少克?
 。现有252 g氢化钙与足量的水反应,生成氢气的质量为多少克?
。现有252 g氢化钙与足量的水反应,生成氢气的质量为多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某课外活动小组为测定当地石灰石中所含碳酸钙的质量分数,取来了一些矿石,并将160g稀盐酸平均分成4份,放入4个烧杯中进行试验,结果如下:(杂质不溶于水,不与稀盐酸反应)
(1)第 次实验中碳酸钙有剩余,m= g。
(2)计算这种石灰石矿中碳酸钙的质量分数?
(3)在图中画出第三次实验中生成二氧化碳质量随碳酸钙质量变化的图像(标出关键点坐标)
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入样品质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.40 | m |
(2)计算这种石灰石矿中碳酸钙的质量分数?
(3)在图中画出第三次实验中生成二氧化碳质量随碳酸钙质量变化的图像(标出关键点坐标)

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】电导率是衡量电解质溶液导电能力大小的物理量.溶液电导率大小变化可以反映电解质溶液中离子浓度的大小变化。下图是向100mL一定溶质质量分数的Ba(OH)2溶液中分别滴加稀H2SO4溶液和稀Na2SO4溶液的过程中溶液电导率随时间变化图。回答下列问题。
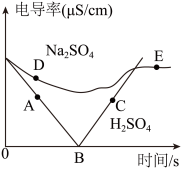
(1)写出Ba(OH)2与H2SO4反应的化学方程式_______________。
(2)若在图中A-E各点对应的溶液中滴加酚酞,则溶液呈红色的有____________。
(3) D-→E的反应过程中,溶液中数目始终增多的微粒有___________。
(4)经测定,B点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数__________(写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。

(1)写出Ba(OH)2与H2SO4反应的化学方程式_______________。
(2)若在图中A-E各点对应的溶液中滴加酚酞,则溶液呈红色的有____________。
(3) D-→E的反应过程中,溶液中数目始终增多的微粒有___________。
(4)经测定,B点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数__________(写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某钙片的标签如下图所示,已知此钙片成分中只有碳酸钙含有钙元素。
(1)通过计算说明此标签中的含钙量______错误。(填“有”或“无”)
(2)为测定其真实的含钙量,小东取10片钙片放入足量盐酸中,发生化学反应是;CaCO3+2HCl=CaCl2+H2O+CO2↑,充分反应后总质量减少了3.3克。
请计算:① 每片此钙片含碳酸钙的质量。(写出计算过程)
② 每片此钙片含钙元素的质量。
| 执行标准:GB1413-99 主要成分:碳酸钙 含钙量:每片含钙0.75g 每瓶50片,重 40 g (中外合资xx公司出品) |
(2)为测定其真实的含钙量,小东取10片钙片放入足量盐酸中,发生化学反应是;CaCO3+2HCl=CaCl2+H2O+CO2↑,充分反应后总质量减少了3.3克。
请计算:① 每片此钙片含碳酸钙的质量。(写出计算过程)
② 每片此钙片含钙元素的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某钙片的标签如下,且知此钙片成分中只有碳酸钙(CaCO3)含有钙元素。
(1)钙片标签含钙量标明每片含钙0.75g,这里的“钙”是指______(填字母)。
(2)碳酸钙的相对分子质量为______ 。
(3)其中Ca、C、O元素的原子个数比是______ ;Ca、C、O元素质量比为______ (填最简整数比)。
(4)通过计算说明此标签中的含钙量是否合理?
(5)如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片。请计算每天他需补充碳酸钙多少克?
执行标准:GH1413—00每瓶50片,净重40g 主要成分:碳酸钙含钙量:每片含钙0.75g(中外合资xx公司出品 |
| A.分子 | B.原子 | C.元素 | D.离子 |
(3)其中Ca、C、O元素的原子个数比是
(4)通过计算说明此标签中的含钙量是否合理?
(5)如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片。请计算每天他需补充碳酸钙多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某实验小组取用铜和氧化铜的混合物20g,向其中逐滴加入稀H2SO4,测得剩余固体的质量与加入稀H2SO4的质量关系如图所示。回答下列问题:
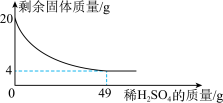
(1)实验中发生的反应属于基本反应类型中的__________ 反应。
(2)计算稀H2SO4中溶质的质量分数(写出计算过程)。

(1)实验中发生的反应属于基本反应类型中的
(2)计算稀H2SO4中溶质的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】草木灰是植物燃烧后的残余物,草木灰中几乎含有植物体内所有的矿物质元素。草木灰的主要成分是碳酸钾,干木柴烧出来的草木灰pH为12左右且无任何杂质。某化学兴趣小组取来干木柴燃烧后产生的草木灰69g,并向其中加入稀盐酸进行反应。实验过程中的pH图像如图所示,求:
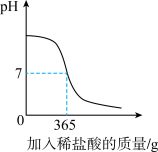
(1)当溶液为中性时,加入稀盐酸的质量为______________ g。
(2)计算实验所用的稀盐酸的溶质质量分数。_______________________

(1)当溶液为中性时,加入稀盐酸的质量为
(2)计算实验所用的稀盐酸的溶质质量分数。
您最近一年使用:0次



