在生活生产中,合锰物质的应用较为广泛。取12.27g硫酸锰铵晶体[(NH4)2SO4·MnSO4·7H2O]用下图装置进行酸锰铵晶体的热分解实验。

[查阅资料]371℃时,(NH4)2SO4·MnSO4·7H2O(相对分子质量409)完全失去结晶水。剩余物质在850℃完全分解为锰的某氧化物、NH3、H2O、SO2、SO3。
(1)加热前后及过程中均通入N2,停止加热后继续通N2的目的是______ (写出两条)。
(2)控制不同的温度对A中固体加热,测得装置B和C中质量变化如下表、剩余固体质量随温度变化如图所示。
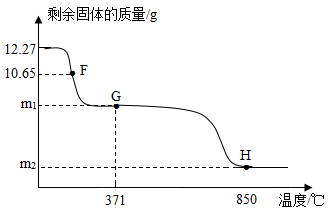
①图中m1的值为______ ,m2的值为______ 。
②F点对应固体的化学式______ 。

[查阅资料]371℃时,(NH4)2SO4·MnSO4·7H2O(相对分子质量409)完全失去结晶水。剩余物质在850℃完全分解为锰的某氧化物、NH3、H2O、SO2、SO3。
(1)加热前后及过程中均通入N2,停止加热后继续通N2的目的是
(2)控制不同的温度对A中固体加热,测得装置B和C中质量变化如下表、剩余固体质量随温度变化如图所示。
| 温度/℃ | 室温 | 371 | 850 |
| B装置/g | 200.00 | 203.78 | 208.96 |
| C装置/g | 200.00 | 200.00 | 201.02 |

①图中m1的值为
②F点对应固体的化学式
更新时间:2022-07-08 15:09:40
|
相似题推荐
实验题
|
适中
(0.65)
名校
解题方法
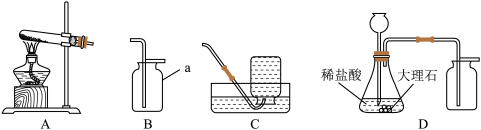
【推荐1】化学实验是进行科学探究的重要途径。某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并回答问题:
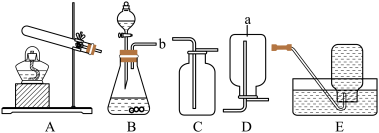

(1)仪器a的名称是______ 。
(2)实验室用加热高锰酸钾固体制取并收集一瓶纯净的氧气,可选用的装置组合是______ (填字母序号)。
(3)实验室制取二氧化碳的化学方程式是______ ,只能用向上排空气法收集二氧化碳的原因是______ 。
(4)实验室用过氧化氢溶液和二氧化锰制取氧气的主要操作步骤有:①检查装置的气密性;②收集并验满气体;③装入药品;④组装仪器。正确的操作顺序是______ (填数字序号)。
(5)F是密封良好充满空气的单气阀充气袋,现用F收集一袋较纯净的氢气,则导气管口b、c连接之前需进行的一项操作是______ 。


(1)仪器a的名称是
(2)实验室用加热高锰酸钾固体制取并收集一瓶纯净的氧气,可选用的装置组合是
(3)实验室制取二氧化碳的化学方程式是
(4)实验室用过氧化氢溶液和二氧化锰制取氧气的主要操作步骤有:①检查装置的气密性;②收集并验满气体;③装入药品;④组装仪器。正确的操作顺序是
(5)F是密封良好充满空气的单气阀充气袋,现用F收集一袋较纯净的氢气,则导气管口b、c连接之前需进行的一项操作是
您最近一年使用:0次
【推荐2】化学是以实验为基础的学科,正确选择实验装置是实验成功的关键。某小组利用如图仪器制取 和
和 ,请回答下列问题。
,请回答下列问题。
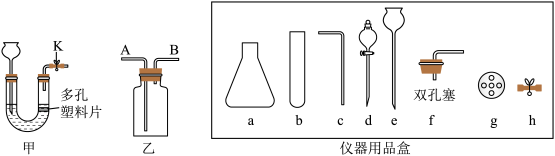
(1) 的实验室制法:实验室用装置甲制取
的实验室制法:实验室用装置甲制取 ,反应过程中,若关闭K,观察到的现象是
,反应过程中,若关闭K,观察到的现象是_____ 。从“仪器用品盒”中选择_____ (填序号)组装的发生装置与装置甲有相同优点。
(2) 的实验室制法:反应的化学方程式为
的实验室制法:反应的化学方程式为_____ ;用装置乙集满 后将其导出使用时,水应从
后将其导出使用时,水应从_____ (填“A”或“B”)端通入。
 和
和 ,请回答下列问题。
,请回答下列问题。
(1)
 的实验室制法:实验室用装置甲制取
的实验室制法:实验室用装置甲制取 ,反应过程中,若关闭K,观察到的现象是
,反应过程中,若关闭K,观察到的现象是(2)
 的实验室制法:反应的化学方程式为
的实验室制法:反应的化学方程式为 后将其导出使用时,水应从
后将其导出使用时,水应从
您最近一年使用:0次
【推荐1】实验室常用的气体制取装置如下,请回答。
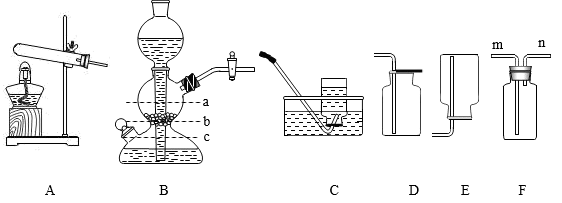
(1)装置B的名称是___ 。
(2)若选用A装置制氧气,反应的化学方程式为__________________ ,向试管中加入药品的正确操作是__ 。
Ⅰ 先加氯酸钾,后加二氧化锰
Ⅱ 先加二氧化锰,后加氯酸钾
Ⅲ 加入混合均匀的氯酸钾和二氧化锰
(3)某同学用A装置制备氧气时发现试管位置太高,不能用外焰加热,则应调节下图中的旋钮___ (填“①”、“②”或“③”)。

(4)选择C装置收集氧气,当看到____________________ ,说明气体收集满了。
(5)实验室制备CO2的化学方程式是_______ ,常选B作为发生装置,选择依据是___________ ,其优点是______ 。若用F装置收集CO2,气体从________ (填“m”或“n”)端通入,验满的方法是____________ 。集满一瓶CO2气体后,关闭玻璃活塞,待反应完全停止后,容器中的液面位置是________ (填“a”、“b”或“c”)。
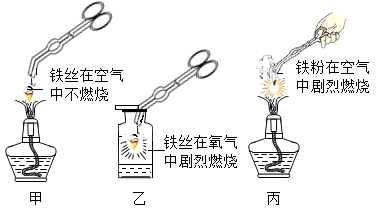
(5)下图是铁在不同情况下与氧气反应的实验。比较实验甲与乙,产生不同现象的原因是______ ;实验乙中集气瓶预留少量水的作用是_________ ;实验丙与乙的产物相同,写出反应的化学方程式_________ 。
(6)实验室用5%过氧化氢溶液和二氧化锰制取氧气,充分反应后得到0.05mol氧气,请问至少需要多少g过氧化氢溶液?_______ (根据化学方程式例式计算)

(1)装置B的名称是
(2)若选用A装置制氧气,反应的化学方程式为
Ⅰ 先加氯酸钾,后加二氧化锰
Ⅱ 先加二氧化锰,后加氯酸钾
Ⅲ 加入混合均匀的氯酸钾和二氧化锰
(3)某同学用A装置制备氧气时发现试管位置太高,不能用外焰加热,则应调节下图中的旋钮

(4)选择C装置收集氧气,当看到
(5)实验室制备CO2的化学方程式是
(5)下图是铁在不同情况下与氧气反应的实验。比较实验甲与乙,产生不同现象的原因是

(6)实验室用5%过氧化氢溶液和二氧化锰制取氧气,充分反应后得到0.05mol氧气,请问至少需要多少g过氧化氢溶液?
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某小组同学在实验室进行中和反应实验:往氢氧化钠溶液中滴入酚酞溶液,观察到溶液变红色,再逐滴加入稀盐酸,并不停搅拌,直至溶液恰好变成无色。盐酸与氢氧化钠反应的化学方程式为____ ,实验中用胶头滴管滴加盐酸并不停搅拌的目的是______ 。
(1)实验中观察到,滴入一定量稀盐酸后,溶液中有少量气泡产生,产生这一现象的原因是___ 。
(2)为测定该样品中碳酸钠的质量分数,某小组同学设计如图所示实验,其中试样中滴加有酚酞溶液。
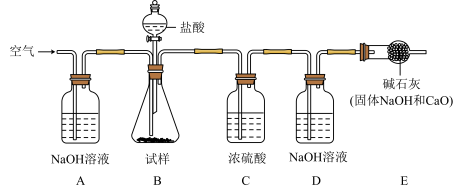
①实验中需持续、缓慢通入空气,其目的是使试样与滴入的稀盐酸充分反应、__ 。
②实验中取氢氧化钠溶液的质量为100g,试样溶液恰好变成无色时,滴入稀盐酸的质量为75g,稀盐酸的溶质质量分数为14.6%,实验后测知D中溶液的质量增加了2.2g,则试样中碳酸钠的质量分数为__ ,如果没有C装置,则测定结果将__ (选填“偏大”、“不受影响”或“偏小”)。
(1)实验中观察到,滴入一定量稀盐酸后,溶液中有少量气泡产生,产生这一现象的原因是
(2)为测定该样品中碳酸钠的质量分数,某小组同学设计如图所示实验,其中试样中滴加有酚酞溶液。

①实验中需持续、缓慢通入空气,其目的是使试样与滴入的稀盐酸充分反应、
②实验中取氢氧化钠溶液的质量为100g,试样溶液恰好变成无色时,滴入稀盐酸的质量为75g,稀盐酸的溶质质量分数为14.6%,实验后测知D中溶液的质量增加了2.2g,则试样中碳酸钠的质量分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】以下是实验室常用的部分仪器。
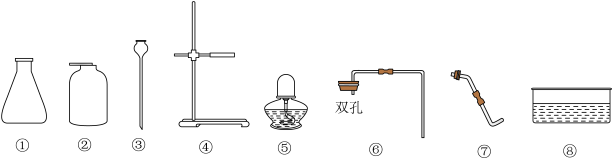
(1)仪器③的名称是_______ ;
(2)用过氧化氢溶液和二氧化锰混合物制氧气时,选用的发生装置是______ ,反应的化学方程式为_____________ 。要收集0.64g氧气,需要H2O2的质量是____ g
(3)同学们用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊。小英认为澄清石灰水已经变质;小青认为得到的CO2中混有_____ 气体。他们为了证明自己的猜想进行了如下实验:
①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊;
②小青取______ 与块状石灰石反应制取的CO2,并将产生的气体通入原澄清石灰水中,变浑浊,请写出石灰水变浑浊的化学方程式__________________________ 。
(4)乙炔是一种无色、无味、难溶水的气体,密度和空气接近,收集乙炔气体可选用的装置是____________ 。

(1)仪器③的名称是
(2)用过氧化氢溶液和二氧化锰混合物制氧气时,选用的发生装置是
(3)同学们用浓盐酸和块状石灰石反应制取二氧化碳,并将得到的气体通入澄清石灰水中,始终没有发现澄清石灰水变浑浊。小英认为澄清石灰水已经变质;小青认为得到的CO2中混有
①小英将气体通入到新制的澄清石灰水中,但仍未发现澄清的石灰水变浑浊;
②小青取
(4)乙炔是一种无色、无味、难溶水的气体,密度和空气接近,收集乙炔气体可选用的装置是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】小明在市场看到,鱼老板将一勺白色粉末“鱼浮灵”加入水中,有气泡产生,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种白色粉末展开了相关探究。
【查阅资料】Ⅰ、“鱼浮灵”主要成分是过碳酸钠(化学式为2Na2CO3∙3H2O2),俗称固体双氧水,该晶体具有Na2CO3和H2O2的双重性质。
Ⅱ、为了方便保存,过碳酸钠样品可能添加少量的MgSO4和硅酸镁中的一种或二种作为稳定剂。
Ⅲ、硅酸镁不溶于水。
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出,将带火星木条伸入试管中,______ ,不能得出是否有氧气生成。
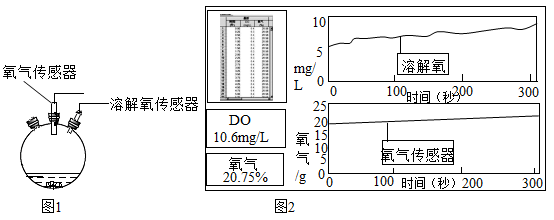
(2)通过数字实验进一步探究,如图1所示,在三颈烧瓶中加入“鱼浮灵”和适量水,三颈烧瓶两端分别插入氧气传感器、溶解氧传感器(氧气传感器用于测定装置内气体中氧气的含量变化,溶解氧传感器用于测定溶液中溶解氧气的含量变化)测定的图像如图2,根据溶解氧传感器测得的曲线可以得出结论:______ 。
(3)结合曲线,实验中小明看不到明显现象的原因是______ 。
(4)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是______(填序号)。
(5)利用实验室限选试剂,设计实验确定该样品中是否添加少量的MgSO4。
限选试剂:稀盐酸、稀H2SO4、BaCl2溶液、蒸馏水、AgNO3溶液
【实验反思】步骤2中,加该试剂的目的是:______ 。
【查阅资料】Ⅰ、“鱼浮灵”主要成分是过碳酸钠(化学式为2Na2CO3∙3H2O2),俗称固体双氧水,该晶体具有Na2CO3和H2O2的双重性质。
Ⅱ、为了方便保存,过碳酸钠样品可能添加少量的MgSO4和硅酸镁中的一种或二种作为稳定剂。
Ⅲ、硅酸镁不溶于水。

(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出,将带火星木条伸入试管中,
(2)通过数字实验进一步探究,如图1所示,在三颈烧瓶中加入“鱼浮灵”和适量水,三颈烧瓶两端分别插入氧气传感器、溶解氧传感器(氧气传感器用于测定装置内气体中氧气的含量变化,溶解氧传感器用于测定溶液中溶解氧气的含量变化)测定的图像如图2,根据溶解氧传感器测得的曲线可以得出结论:
(3)结合曲线,实验中小明看不到明显现象的原因是
(4)在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是______(填序号)。
| A.二氧化锰 | B.稀盐酸 | C.硫酸钠 | D.石灰水 |
限选试剂:稀盐酸、稀H2SO4、BaCl2溶液、蒸馏水、AgNO3溶液
| 实验操作 | 预期现象和必要结论 |
| 步骤1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤。 | |
| 步骤2:取少量步骤1所得的滤液于试管中,加入 | |
| 步骤3:取少量步骤2所得的溶液液于试管中,加入 |
【实验反思】步骤2中,加该试剂的目的是:
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
【推荐2】学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显___ 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有____ 产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗_______ ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想_____ 一定不正确,理由是_______ .小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为_______________________
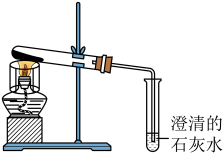
(4)小美和小刚继续探究固体成分,设计了如下实验:
通过实验证明小苏打受热会分解,反应的化学方程式为:________________________ .通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有:____ (答出一点即可).
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想

(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
通过实验证明小苏打受热会分解,反应的化学方程式为:
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】氯碱厂通过海水晒盐和电解饱和食盐水法制的NaOH和Cl2。回答下列问题:
(1)为除去粗盐中可溶性的钙盐、镁盐、硫酸盐等杂质,需要按照一定顺序加入试剂。依次加入的试剂为______ 。
(2)生产时,利用氢氧化钠和氯化钠溶解温度差异(如下表),将10%NaCl和50%NaOH采用特定操作进行处理,从而获得NaCl晶体和NaOH浓溶液(该过程为“脱盐工序”)。
①脱盐工序中,所采取的操作是______ 。
②采用过滤方法分离NaCl晶体和NaOH浓溶液时,滤纸上要放两张甚至多张滤纸,其原因是______ 。
(3)氯气有毒性,可与氢氧化钠溶液发生反应。下图为某同学在实验室利用氯气制取S2Cl2的装置图。
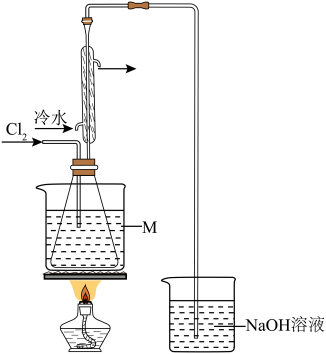
已知,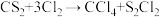 (反应温度约为130℃);
(反应温度约为130℃);
S2Cl2、CS2和CCl4的沸点依次为137℃、47℃、77℃。
①冷凝管的作用是______ 。
②盛装在M烧杯中的液体能否为水?______ 。判断的理由是______ 。
③反应产物S2Cl2在______ 中(填仪器名称)。
④实验完毕停止通入氯气后拆除装置,最先的操作应当是______ 。
(1)为除去粗盐中可溶性的钙盐、镁盐、硫酸盐等杂质,需要按照一定顺序加入试剂。依次加入的试剂为
(2)生产时,利用氢氧化钠和氯化钠溶解温度差异(如下表),将10%NaCl和50%NaOH采用特定操作进行处理,从而获得NaCl晶体和NaOH浓溶液(该过程为“脱盐工序”)。
| 温度/℃ | 1 | 20 | 40 | 60 |
| NaOH/g | 42 | 109 | 129 | 174 |
| NaCl/g | 35.7 | 36 | 36.6 | 37.3 |
②采用过滤方法分离NaCl晶体和NaOH浓溶液时,滤纸上要放两张甚至多张滤纸,其原因是
(3)氯气有毒性,可与氢氧化钠溶液发生反应。下图为某同学在实验室利用氯气制取S2Cl2的装置图。

已知,
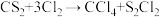 (反应温度约为130℃);
(反应温度约为130℃);S2Cl2、CS2和CCl4的沸点依次为137℃、47℃、77℃。
①冷凝管的作用是
②盛装在M烧杯中的液体能否为水?
③反应产物S2Cl2在
④实验完毕停止通入氯气后拆除装置,最先的操作应当是
您最近一年使用:0次

 的收集装置
的收集装置

