康康同学对化学中的计算问题十分感兴趣,他自己命制了两道试题请同学解答。
(1)试题1:将四种盐①Na2CO3、②NaHCO3、③CaCO3、④K2CO3分别投入等质量、等浓度的足量稀盐酸中,充分反应后所得四种溶液的质量相等,则投入盐的质量由小到大的顺序为________ (填序号)。
(2)试题2:在由上述四种盐组成的混合物中,若氧元素的质量分数为32%,则混合物中碳元素的质量分数为_________ ?小明同学经过思考后,指出该题存在一个科学性错误,请你指出该错误:_________ 。
(1)试题1:将四种盐①Na2CO3、②NaHCO3、③CaCO3、④K2CO3分别投入等质量、等浓度的足量稀盐酸中,充分反应后所得四种溶液的质量相等,则投入盐的质量由小到大的顺序为
(2)试题2:在由上述四种盐组成的混合物中,若氧元素的质量分数为32%,则混合物中碳元素的质量分数为
更新时间:2022-07-16 20:51:17
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】氮气、氧气、二氧化碳都是空气的重要成分。
(1)工业上利用液态氮和液态氧的_________ 不同,使空气中的氮气和氧气分离。
(2)在实验室里可以通过加热混有二氧化锰的氯酸钾固体制取氧气,该反应的化学方程式为_____________________________________ 。
(3)工业上煅烧石灰石可制得生石灰和二氧化碳。现煅烧6t石灰石(杂质不参与反应),完全反应后制得了2.2t二氧化碳,则该石灰石中碳酸钙的质量分数是多少___ ?
(1)工业上利用液态氮和液态氧的
(2)在实验室里可以通过加热混有二氧化锰的氯酸钾固体制取氧气,该反应的化学方程式为
(3)工业上煅烧石灰石可制得生石灰和二氧化碳。现煅烧6t石灰石(杂质不参与反应),完全反应后制得了2.2t二氧化碳,则该石灰石中碳酸钙的质量分数是多少
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
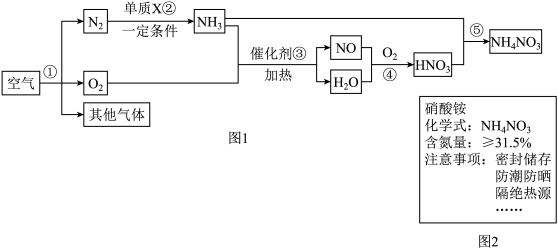
【推荐2】工业上用N2和H2合成NH3是人类科学技术的一项重大突破。
(1)①N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的_________ (填“物理”或“化学”)性质。
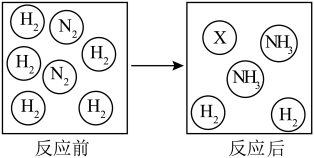
②一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为_________ (填化学式)。 。
。
①尿素为农作物生长提供的主要营养元素为__________ 。
②尿素可用于去除大气污染物中的NO,其化学反应为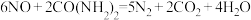 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少__________ ?(请将计算过程写到答题卡上)
(1)①N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的
②一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为
 。
。①尿素为农作物生长提供的主要营养元素为
②尿素可用于去除大气污染物中的NO,其化学反应为
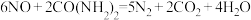 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】弘扬中国航天精神,星辰大海永不止步。

(1)2022年11月29日23时08分,神舟十五号与神舟十四号航天员乘组“胜利会师”,一起在中国人自己的“太空家园“里留下了一张足以载入史册的太空合影。搭载神舟十五号载人飞船的长征二号F遥十五运载火箭以偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作为推动剂,发生反应的化学方程式为: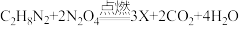 。
。
①则X的化学式______ 。
②该反应中,生成二氧化碳和水的质量比为______ (填最简整数比)。
(2)2021年4月29日,天和号空间站核心舱在文昌太空港成功发射。天和号核心太空舱的太阳能电池板使用了一种全新的材料——柔性砷化镓(GaAs),与传统的太阳能电池板有着天壤之别。
①在砷化镓(GaAs)中,Ga元素的化合价为+3价,则As元素的化合价为______ 。
②传统太阳能电池板的半导体材料高纯硅,可以利用石英砂(上要成分是SiO2)制得,在高温条件下,SiO2和碳可以发生化学反应,生成硅和一氧化碳,请写出该反应的化学方程式:______ 。
(3)2020年12月24日,长征五号遥五运载火箭成功把“嫦娥五号”探测器送至地月转移轨道。长征五号芯一级燃料是液氧和液氢,填补了我国大推力无毒无污染液体火箭发动机的空白。

①写出氢气与氧气发生反应的化学方程式:______ 。
②列举氢能源的三条优点:______ 。

(1)2022年11月29日23时08分,神舟十五号与神舟十四号航天员乘组“胜利会师”,一起在中国人自己的“太空家园“里留下了一张足以载入史册的太空合影。搭载神舟十五号载人飞船的长征二号F遥十五运载火箭以偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作为推动剂,发生反应的化学方程式为:
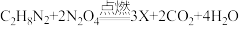 。
。①则X的化学式
②该反应中,生成二氧化碳和水的质量比为
(2)2021年4月29日,天和号空间站核心舱在文昌太空港成功发射。天和号核心太空舱的太阳能电池板使用了一种全新的材料——柔性砷化镓(GaAs),与传统的太阳能电池板有着天壤之别。
①在砷化镓(GaAs)中,Ga元素的化合价为+3价,则As元素的化合价为
②传统太阳能电池板的半导体材料高纯硅,可以利用石英砂(上要成分是SiO2)制得,在高温条件下,SiO2和碳可以发生化学反应,生成硅和一氧化碳,请写出该反应的化学方程式:
(3)2020年12月24日,长征五号遥五运载火箭成功把“嫦娥五号”探测器送至地月转移轨道。长征五号芯一级燃料是液氧和液氢,填补了我国大推力无毒无污染液体火箭发动机的空白。

①写出氢气与氧气发生反应的化学方程式:
②列举氢能源的三条优点:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】下图中的A~I表示几种初中化学常见的物质,其中A、D、I是氧化物,I中两种元素质量之比为3:4;B元素在地壳中的含量位居第三;C由三种元素组成;G为紫红色。图中“—— ”表示两端的物质间能发生化学反应;“ → ”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。

(1)写出E的化学式___________ 。
(2)写出B →A反应的化学方程式__________________ 。
(3)反应①、②和③的基本反应类型相同,该基本反应类型是_______
(4)写出H与D反应的化学方程式____________________ 。

(1)写出E的化学式
(2)写出B →A反应的化学方程式
(3)反应①、②和③的基本反应类型相同,该基本反应类型是
(4)写出H与D反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】现有一份由Fe、FeSO4和Fe2(SO4)3组成的混合物,其中氧元素的质量分数为8%,则混合物中铁元素的质量分数为______ ;Fe(OH)2在空气中会与水、氧气发生化合反应生成Fe(OH)3,该反应的化学方程式为______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】中国航空、航天领域的进步离不开中国科学的研究。
(1)间苯二胺(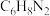 )是合成新材料的重要原料之一。间苯二胺中,氮元素属于
)是合成新材料的重要原料之一。间苯二胺中,氮元素属于______ (填“金属”或“非金属”)元素;氢元素和氮元素的质量比为______ (最简整数比);______ 元素质量分数最大。
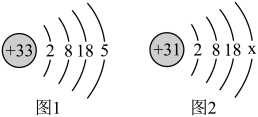
(2)如图1、2所示分别为砷.镓的原子结构示意图。据图回答,
______ ;砷、镓两种元素化学性质不同,原因是______ (填序号)。
a.质子数不同b.中子数不同c.相对原子质量不同d.最外层电子数不同
(3)核能的开发是解决能源紧缺的重要途径。如图3所示是核聚变的微观示意图。
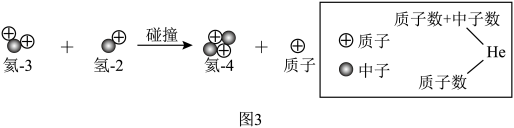
氦-3和氦-4都是氦元素,原因是它们的原子核内都有______ 个质子;根据氦-3的原子符号 写出氦-4的原子符号
写出氦-4的原子符号______ 。

(1)间苯二胺(
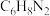 )是合成新材料的重要原料之一。间苯二胺中,氮元素属于
)是合成新材料的重要原料之一。间苯二胺中,氮元素属于(2)如图1、2所示分别为砷.镓的原子结构示意图。据图回答,

a.质子数不同b.中子数不同c.相对原子质量不同d.最外层电子数不同
(3)核能的开发是解决能源紧缺的重要途径。如图3所示是核聚变的微观示意图。

氦-3和氦-4都是氦元素,原因是它们的原子核内都有
 写出氦-4的原子符号
写出氦-4的原子符号
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐2】以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4·7H2O,流程如下:

已知:硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
回答下列问题:
(1)“酸浸”时,MgCO3发生反应的化学方程式是______ 。
(2)“转化”时主要反应是NaClO+MnSO4+H2O=MnO2↓+NaCl+H2SO4,氯元素反应前后化合价变化情况是______ (选填“升高”或“降低”)。
(3)“操作Ⅰ”是:蒸发浓缩、降温结晶、过滤、洗涤、低温干燥。降温结晶应控制的温度范围是______ (填选项编号)。
A.-3.9~1.8℃ B.1.8~48.2℃ C.48.2~67.5℃ D.67.5~200℃
若降温结晶的温度高于应控制范围,得到的产品中镁元素质量分数______ (选填“大于”、“等于”或“小于”)9.76%。
(4)无水硫酸镁是低钠盐的一种成分。将产品加热脱水制取无水硫酸镁,发现高于900℃时剩余固体中镁元素质量分数大于20%,可能的原因是______ 。

已知:硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃ | -3.9~1.8 | 1.8~48.2 | 48.2~67.5 | 67.5~200 |
析出晶体 | MgSO4·12H2O | MgSO4·7H2O | MgSO4·6H2O | MgSO4·H2O |
(1)“酸浸”时,MgCO3发生反应的化学方程式是
(2)“转化”时主要反应是NaClO+MnSO4+H2O=MnO2↓+NaCl+H2SO4,氯元素反应前后化合价变化情况是
(3)“操作Ⅰ”是:蒸发浓缩、降温结晶、过滤、洗涤、低温干燥。降温结晶应控制的温度范围是
A.-3.9~1.8℃ B.1.8~48.2℃ C.48.2~67.5℃ D.67.5~200℃
若降温结晶的温度高于应控制范围,得到的产品中镁元素质量分数
(4)无水硫酸镁是低钠盐的一种成分。将产品加热脱水制取无水硫酸镁,发现高于900℃时剩余固体中镁元素质量分数大于20%,可能的原因是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】如下图所示,A-I是初中化学中常见的物质,A、C是两种常见液体且组成元素相同,B、F是黑色粉末,H是蓝色沉淀,E是含钠元素的化合物,部分反应物和生成物已略,“→”表示物质转化。
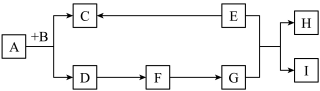
(1)物质F的化学式为_______ ;
(2)写出E物质在生活中的一种用途_______ ;
(3)写出反应E+G→H+I的化学方程式_______ 。

(1)物质F的化学式为
(2)写出E物质在生活中的一种用途
(3)写出反应E+G→H+I的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】已知A-H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据图示的转化关系(图中反应条件均已略去),请回答:
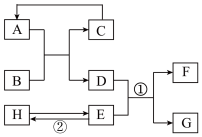
(1)写出下列物质的化学式:B______ 、C______ 。
(2)写出物质D的一种用途:______ 。
(3)写出下列反应的化学方程式:①_______ ;其基本反应类型是_______ 。A+B→C+D的方程式_______ 。

(1)写出下列物质的化学式:B
(2)写出物质D的一种用途:
(3)写出下列反应的化学方程式:①
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A~H是初中化学常见的物质,它们之间的关系如图所示(“→”表示物质间的转化关系,“一”表示两端的物质能发生化学反应),虚线圈中的两种物质类别相同。A的浓溶液有吸水性,在实验室常用作干燥剂;C可用来改良酸性土壤;D广泛应用于肥皂、石油、造纸、纺织和印染等工业,在生活中可用来去除油污;E的水溶液为浅绿色,F可与生石灰、水配制成具有杀菌作用的波尔多液;A的稀溶液与G发生复分解反应生成F与H。

(1)写出下列物质的化学式:B________ 、F_________ 。
(2)写出C转化为D的化学方程式_________ 。
(3)写出A的稀溶液与G发生反应的化学方程式__________ 。
(4)分类观是化学的核心观念之一,以上8种物质没有涉及到的物质类别是________ 。

(1)写出下列物质的化学式:B
(2)写出C转化为D的化学方程式
(3)写出A的稀溶液与G发生反应的化学方程式
(4)分类观是化学的核心观念之一,以上8种物质没有涉及到的物质类别是
您最近一年使用:0次