实验探究一:小明学习了过氧化氢溶液分解知识后,脑洞大开,还想寻找新的催化剂,于是设计了如下探究方案:
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的符号表达式_______ 。
实验探究二:小明继续探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如表:
①根据上述实验数据得出的结论:能使带火星的小木条复燃的_______ (填一定或不一定)是纯氧。
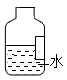
②在集气瓶中注入占其容器50%的水(如图),用排水法收集氧气,刚好将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,小木条_______ (填“复燃”或“不复燃”)理由是_______ 。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
| 实验步骤及操作 | 实验现象 | 实验结论及解释 |
Ⅰ.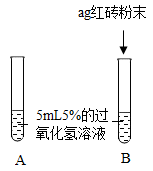 | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是 ②红砖粉末能改变过氧化氢分解速率 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的 |
Ⅲ.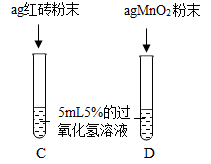 | 两试管中均产生气泡且 | 红砖粉末的催化效果没有二氧化锰粉末好 |
【实验探究】请写出红砖粉末(成分以Fe2O3表示)催化过氧化氢溶液分解反应的符号表达式
实验探究二:小明继续探究带火星的木条在不同体积分数氧气中的复燃情况,部分实验数据记录如表:
| 氧气体积分数(%) | 30 | 40 | 60 | 70 |
| 带火星的木条 | 不变 | 稍亮 | 复燃 | 复燃 |
①根据上述实验数据得出的结论:能使带火星的小木条复燃的
②在集气瓶中注入占其容器50%的水(如图),用排水法收集氧气,刚好将瓶内的水排尽,用带火星的木条在该集气瓶中进行实验,小木条

更新时间:2022-11-03 11:09:32
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】二氧化锰可作过氧化氢分解的催化剂,兴趣小组的同学想探究过氧化氢分解有没有其他催化剂。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】
(1)A试管中产生的气体是_______ 。
(2)实验Ⅱ证明氧化铁的_______ 在反应前后没有发生变化。实验Ⅲ中如果a=_______ g,则证明氧化铁的_______ 在反应前后没有发生变化,可以作过氧化氢分解的催化剂。
(3)写出氧化铁催化过氧化氢分解的文字表达式:________ 。
【实验评价】实验设计Ⅳ的目的是_______ ,其中b=_______ g。若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是_______ 。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5ml 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入1g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称重,所得固体质量为ag | / |
| Ⅳ.分别量取5ml 5%过氧化氢溶液放入C、D两支试管中,向C试管中加入1g氧化铁粉末,向D试管中加入bg二氧化锰粉末,观察现象 | / |
(1)A试管中产生的气体是
(2)实验Ⅱ证明氧化铁的
(3)写出氧化铁催化过氧化氢分解的文字表达式:
【实验评价】实验设计Ⅳ的目的是
您最近一年使用:0次
【推荐2】氯酸钾是实验室制取氧气的主要原料之一,我们常用二氧化锰作为反应的催化剂来加快氯酸钾的反应速率。
(1)请写出该反应的符号表达式:_______________ 。那么,氧化铜可以代替二氧化锰作为氯酸钾反应的催化剂吗?某化学兴趣小组的同学就此问题进行了如下的实验探究:
【提出问题】氧化铜可以作为氯酸钾反应的催化剂吗?
【猜想与假设】
(2)猜想Ⅰ:氧化铜不能作为氯酸钾反应的催化剂;
猜想Ⅱ:_______________ 。
【查阅资料】氯酸钾和氯化钾都是可溶于水的固体,氧化铜是一种不溶于水的粉末状固体。
【实验验证】
实验一:
(3)①组装实验装置,并检查装置_______________ 。
②在大试管中装入一定质量的氯酸钾,加热试管并用排水集气法收集产生的气体,一段时间后观察到导管口有很少量的气泡产生。
③向实验②的大试管中加入 a g 的氧化铜粉末后重新进行实验,立刻观察到导管口产生大量气泡。
④待导管口不再产生气泡后,重新向试管中加入少量的氯酸钾,如此反复多次,观察现象。
实验二:
将实验后的固体溶解于足量的水中并进行过滤,将过滤后所得的固体洗净、干燥、称量。
【解释与结论】
(4)实验一中,反复多次进行实验的目的是_______________ 。
(5)实验二中,最终所得固体质量仍为 a g。结合实验一的实验现象可知猜想_______________ (填“Ⅰ”或“Ⅱ”)正确。
【拓展延伸】
(6)实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体和氯酸钾固体混合加热,则氯酸钾的分解速率大大加快。高锰酸钾在氯酸钾的分解反应中______ (填“是”或“不是”)作催化剂,理由是 _______________ 。
(1)请写出该反应的符号表达式:
【提出问题】氧化铜可以作为氯酸钾反应的催化剂吗?
【猜想与假设】
(2)猜想Ⅰ:氧化铜不能作为氯酸钾反应的催化剂;
猜想Ⅱ:
【查阅资料】氯酸钾和氯化钾都是可溶于水的固体,氧化铜是一种不溶于水的粉末状固体。
【实验验证】
实验一:
(3)①组装实验装置,并检查装置
②在大试管中装入一定质量的氯酸钾,加热试管并用排水集气法收集产生的气体,一段时间后观察到导管口有很少量的气泡产生。
③向实验②的大试管中加入 a g 的氧化铜粉末后重新进行实验,立刻观察到导管口产生大量气泡。
④待导管口不再产生气泡后,重新向试管中加入少量的氯酸钾,如此反复多次,观察现象。
实验二:
将实验后的固体溶解于足量的水中并进行过滤,将过滤后所得的固体洗净、干燥、称量。
【解释与结论】
(4)实验一中,反复多次进行实验的目的是
(5)实验二中,最终所得固体质量仍为 a g。结合实验一的实验现象可知猜想
【拓展延伸】
(6)实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体和氯酸钾固体混合加热,则氯酸钾的分解速率大大加快。高锰酸钾在氯酸钾的分解反应中
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”。他设计并完成了如表所示的探究实验,请你帮他填写下表划线部分的空格:
(1)在该同学的三个探究实验中,实验一和实验二起的作用是_____ 。
(2)小英同学认为仅由上述实验还不能完全得出“二氧化锰是氯酸钾受热分解的催化剂”的结论,她补充设计了两个方面的探究实验:
第一方面的实验操作中包含了两次称量,其目的是:_____ 。
第二方面的实验是要验证从反应后的剩余物中分离出的MnO2是否还能加快KClO3的分解。
从质量守恒定律考虑,用高锰酸钾和氯酸钾都能制得氧气,其原因是_____ 。
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 各步骤结论 | 总结 | |||
| 实验一 | 将氯酸钾装在试管中加热至融化,再往试管中伸入带火星的木条。 | 木条复燃 | 氯酸钾受热能分解产生氧气,但是反应速率慢。 化学方程式为: | 二氧化锰是氯酸钾受热分解的催化剂。 |
| 实验二 | 加热装在试管中的二氧化锰,然后往试管中伸入带火星的木条。 | 木条不复燃 | ||
| 实验三 | 木条迅速复燃 | |||
(1)在该同学的三个探究实验中,实验一和实验二起的作用是
(2)小英同学认为仅由上述实验还不能完全得出“二氧化锰是氯酸钾受热分解的催化剂”的结论,她补充设计了两个方面的探究实验:
第一方面的实验操作中包含了两次称量,其目的是:
第二方面的实验是要验证从反应后的剩余物中分离出的MnO2是否还能加快KClO3的分解。
从质量守恒定律考虑,用高锰酸钾和氯酸钾都能制得氧气,其原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某研究小组发现,将一片土豆片放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。该小组同学进行了如下探究。
【提出问题】土豆能不能作过氧化氢分解的催化剂呢?
【作出猜想】土豆能作过氧化氢分解的催化剂。
【实验验证】
【分析数据、得出结论】
(1)实验①、②证明:土豆能______ 。
实验③、④证明:土豆的_______ 和______ 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(2)写出土豆催化过氧化氢分解的文字表达式:_______ 。
【实验拓展】
(3)该研究小组又做了比较土豆与二氧化锰的催化效果的实验(如下图)。实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计相关数据见下表

上述实验中的“待测数据”指_______ ;最后的结果表明二氧化锰的催化效果好,则a______ b(填“>”、“<”或“=”)。
(4)查阅资料得知:氧化铜、硫酸铜、猪肝等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_______ 。
a.MnO2只能作为过氧化氢溶液分解的催化剂
b.同一个化学反应可以有多种催化剂
c.催化剂只能加快化学反应的速率
d.用作催化剂的物质不可能是其它反应的反应物或生成物
【提出问题】土豆能不能作过氧化氢分解的催化剂呢?
【作出猜想】土豆能作过氧化氢分解的催化剂。
【实验验证】
| 实验 | 实验操作 | 实验现象 |
| ① | 在试管中加入过氧化氢溶液,然后将带火星的木条伸入试管中 | 木条不复燃 |
| ② | 在装有过氧化氢溶液的试管中加入0.5g土豆,然后将带火星的木条伸入试管中 | 产生大量的气泡,木条复燃 |
| ③ | 待②中反应结束,将试管中将试管里的剩余物进行过滤、洗涤、干燥、称量 | 称得固体质量为0.5g |
| ④ | 将③中所得固体放入试管中,重新加入过氧化氢溶液,然后将带火星的木条伸入试管中 | 产生大量的气泡,木条复燃 |
(1)实验①、②证明:土豆能
实验③、④证明:土豆的
(2)写出土豆催化过氧化氢分解的文字表达式:
【实验拓展】
(3)该研究小组又做了比较土豆与二氧化锰的催化效果的实验(如下图)。实验时均以生成25mL气体为准,其他可能影响实验的因素均忽略不计相关数据见下表

| 实验 | 3%过氧化氢溶液体积 | 其他物质质量 | 待测数据 |
| I | 20mL | 鲜土豆片0.5g | a |
| II | 20mL | 二氧化锰0.5g | b |
(4)查阅资料得知:氧化铜、硫酸铜、猪肝等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是
a.MnO2只能作为过氧化氢溶液分解的催化剂
b.同一个化学反应可以有多种催化剂
c.催化剂只能加快化学反应的速率
d.用作催化剂的物质不可能是其它反应的反应物或生成物
您最近一年使用:0次
【推荐2】关于催化剂的研究是一项重要的课题,某化学兴趣小组开展了“探究催化剂的奥秘”项目式学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_____(填字母)。
【任务二】定量探究催化剂的催化效果
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。同学们分别用等量、颗粒大小相同的三种金属氧化物作催化剂进行实验,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
(2)用氯酸钾制取氧气,若替代二氧化锰作催化剂,根据上表分析,最佳的金属氧化物应选择_____ 。
【设计并完成实验】
(3)实验一:将3.0g氯酸钾放在试管中加热;
实验二:将3.0g氯酸钾与1.0g二氧化锰混合均匀加热;
实验三:将xg氯酸钾与1.0g氧化铜混合均匀加热;
①请写出检验试管中生成氧气的方法:_____ 。
②通过实验二与实验三可以比较出不同催化剂对实验的影响,则实验三中x的值为_____ ,写出实验三反应的化学方程式:_____ 。
③对比实验_____ (填“一”或“二”)和实验三的不同现象,可证明氧化铜能加快氯酸钾的分解速率。
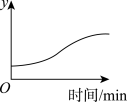
(4)加热一定量的氯酸钾和氧化铜的混合物,某变量y随时间的变化趋势如图所示。则纵坐标y表示的是_____(填字母)。
【实验结论】
(5)_____ 。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_____(填字母)。
| A.不加入催化剂化学反应就不能发生 |
| B.在过氧化氢溶液中加入二氧化锰,则生成氧气的质量将增加 |
| C.催化剂的化学性质在化学反应前后不发生改变 |
【任务二】定量探究催化剂的催化效果
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。同学们分别用等量、颗粒大小相同的三种金属氧化物作催化剂进行实验,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 催化剂 | 氧化铁 | 氧化铝 | 氧化铜 |
| 开始反应/℃ | 420 | 515 | 305 |
| 剧烈反应/℃ | 490 | 540 | 350 |
(2)用氯酸钾制取氧气,若替代二氧化锰作催化剂,根据上表分析,最佳的金属氧化物应选择
【设计并完成实验】
(3)实验一:将3.0g氯酸钾放在试管中加热;
实验二:将3.0g氯酸钾与1.0g二氧化锰混合均匀加热;
实验三:将xg氯酸钾与1.0g氧化铜混合均匀加热;
①请写出检验试管中生成氧气的方法:
②通过实验二与实验三可以比较出不同催化剂对实验的影响,则实验三中x的值为
③对比实验
(4)加热一定量的氯酸钾和氧化铜的混合物,某变量y随时间的变化趋势如图所示。则纵坐标y表示的是_____(填字母)。

| A.固体中氧化铜的质量 |
| B.固体中氯酸钾的质量 |
| C.固体中氧化铜的质量分数 |
【实验结论】
(5)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某“氧系茶垢清洁剂”外观为白色粉末,主要成分为过碳酸钠(2Na2CO3·3H2O2),能快速清洁茶具上附着的茶垢。某兴趣小组对该茶垢清洁剂展开探究。
资料:过碳酸钠具有Na2CO3与H2O2的双重性质,遇酸产生CO2,受热或遇水易分解;
【问题一】使用时,将产品倒入茶具中,加入60℃~70℃的热水,立即产生大量气泡。
探究该气泡成分:
提出猜想:猜想一:O2;猜想二:CO2;猜想三:……
实验验证:取少量该茶垢清洁剂于试管中,向其中加入适量60℃~70℃的热水,塞上带导管的橡皮塞,将生成的气体通入澄清石灰水,发现澄清石灰水_____ ;打开橡皮塞,向其中伸入_____ ,观察到预期的现象,证实猜想一正确。
(1)该实验中,H2O2产生O2的化学方程式为_____ 。
(2)该“氧系茶垢清洁剂”除了清除茶垢外,还可杀菌消毒。原理是使用过程中产生的活性氧具有很强的氧化性,可以使细菌、病毒中的蛋白质_____ 。
【问题二】同样的产品价格不同,可能是因为产品的纯度不同等。测定样品的纯度(过碳酸钠的含量):
方案一:测定CO2质量
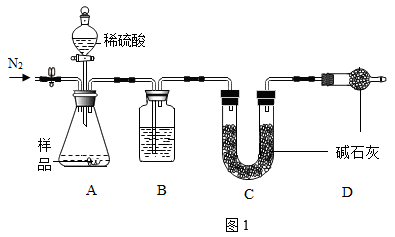
按图1取一定质量样品于锥形瓶中,向装置中通入一段时间N2,滴加足量稀硫酸。装置A中产生的气体经装置B干燥,进入装置C被吸收;反应结束后继续通入一段时间N2;称量装置C在反应前后的质量。(提示:碱石灰是NaOH和CaO的固体混合物)
(1)装置B中试剂的名称_____ 。
(2)装置D的作用_____ 。
(3)反应结束后继续通入N2的目的是_____ 。
方案二:测定O2的体积
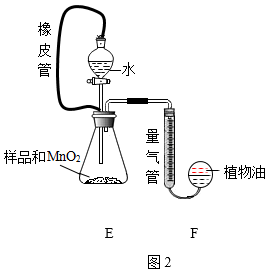
按图2取一定质量样品和MnO2于锥形瓶中,滴加适量水,利用装置F测定产生O2的体积。(提示:①读数时需等装置冷却至室温;②实验前后均需要调整量气管两边液面相平)
(1)从能量变化的角度考虑,H2O2在MnO2催化下分解的反应属于_____ 反应。
(2)若装置E中没有使用橡皮管,会导致测得的氧气体积偏大,原因是_____ ;本实验中,橡皮管还可以起到平衡压强,有利于液体顺利流下的作用。
方案三:测定沉淀质量
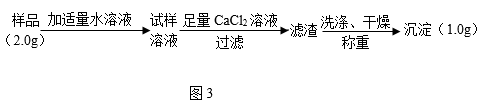
按图3将Na2CO3转化为CaCO3沉淀。
(1)加入“足量”CaCl2溶液的目的是_____ 。
(2)判断Na2CO3是否已完全转化为沉淀的方法_____ 。
(3)根据沉淀质量为1.0g,计算样品中Na2CO3的质量_____ g。
【总结提升】测定物质含量的一般方法如图4。
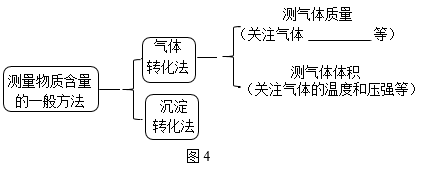
上述测量物质含量的方法中“测气体质量”时需关注的事项是_____ (答一条即可)。
资料:过碳酸钠具有Na2CO3与H2O2的双重性质,遇酸产生CO2,受热或遇水易分解;
【问题一】使用时,将产品倒入茶具中,加入60℃~70℃的热水,立即产生大量气泡。
探究该气泡成分:
提出猜想:猜想一:O2;猜想二:CO2;猜想三:……
实验验证:取少量该茶垢清洁剂于试管中,向其中加入适量60℃~70℃的热水,塞上带导管的橡皮塞,将生成的气体通入澄清石灰水,发现澄清石灰水
(1)该实验中,H2O2产生O2的化学方程式为
(2)该“氧系茶垢清洁剂”除了清除茶垢外,还可杀菌消毒。原理是使用过程中产生的活性氧具有很强的氧化性,可以使细菌、病毒中的蛋白质
【问题二】同样的产品价格不同,可能是因为产品的纯度不同等。测定样品的纯度(过碳酸钠的含量):
方案一:测定CO2质量
按图1取一定质量样品于锥形瓶中,向装置中通入一段时间N2,滴加足量稀硫酸。装置A中产生的气体经装置B干燥,进入装置C被吸收;反应结束后继续通入一段时间N2;称量装置C在反应前后的质量。(提示:碱石灰是NaOH和CaO的固体混合物)
(1)装置B中试剂的名称
(2)装置D的作用
(3)反应结束后继续通入N2的目的是


方案二:测定O2的体积
按图2取一定质量样品和MnO2于锥形瓶中,滴加适量水,利用装置F测定产生O2的体积。(提示:①读数时需等装置冷却至室温;②实验前后均需要调整量气管两边液面相平)
(1)从能量变化的角度考虑,H2O2在MnO2催化下分解的反应属于
(2)若装置E中没有使用橡皮管,会导致测得的氧气体积偏大,原因是
方案三:测定沉淀质量

按图3将Na2CO3转化为CaCO3沉淀。
(1)加入“足量”CaCl2溶液的目的是
(2)判断Na2CO3是否已完全转化为沉淀的方法
(3)根据沉淀质量为1.0g,计算样品中Na2CO3的质量
【总结提升】测定物质含量的一般方法如图4。

上述测量物质含量的方法中“测气体质量”时需关注的事项是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对黑色的氧化铜(CuO)产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
(1)上述实验应测量的“待测数据”是____ 。
(2)若实验②比实验①的“待测数据”更____ (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,说明黑色粉末的____ 在反应前后保持不变。
(4)再将该黑色粉末放入试管中,向其中倒入适量的双氧水,观察到有气泡产生,说明黑色粉末的____ 在反应前后保持不变。
【预期结论】
(5)氧化铜能作氯酸钾分解的催化剂,写出此反应的文字表达式____ 。
【评价设计】
(6)你认为小雨设计实验②和实验③对比的目的是____ 。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3 | 其它物质物质 | 待测数据 |
| ① | 1.2g | —— | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
(2)若实验②比实验①的“待测数据”更
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,说明黑色粉末的
(4)再将该黑色粉末放入试管中,向其中倒入适量的双氧水,观察到有气泡产生,说明黑色粉末的
【预期结论】
(5)氧化铜能作氯酸钾分解的催化剂,写出此反应的文字表达式
【评价设计】
(6)你认为小雨设计实验②和实验③对比的目的是
您最近一年使用:0次
【推荐2】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2 的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2 所需的时间。
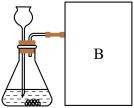
【进行实验】如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是______ 。
【实验记录】
【结 论】该探究过程得出的是______ 。
【反 思】H2O2在常温下分解缓慢,加入MnO2 或水泥块后反应明显加快,若要证明MnO2 和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的______ 和______ 是否改变。
【假设】H2O2生成O2 的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2 所需的时间。
【进行实验】如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是

【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2 | 5%H2O2 |
| 催化剂 | 1g水泥块 | 1gMnO2 |
| 时间 | 165秒 | 46秒 |
【反 思】H2O2在常温下分解缓慢,加入MnO2 或水泥块后反应明显加快,若要证明MnO2 和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】在学习“氧气的化学性质”过程中,小泽等同学进行了以下探究活动,请你一起参与。铁丝在氧气中燃烧
(1)实验时要用砂纸擦去铁丝表面的铁锈,该过程属于_________ 变化。(填“物理”或“化 学”)
(2)铁丝在氧气中燃烧的化学式表达式为______ 。
(3)小泽同学实验时,集气瓶炸裂了,请你帮助他分析一下可能的原因______ 。
(4)探究直径为 0.38mm 的铁丝燃烧是否需要纯净的氧气:
【实验内容】
取 0.38mm 的铁丝,分别在体积分数为 90%、70%、65%、60%、55%的氧气中进行实验, 实验现象如下表所示:
【实验结论】
就 0.38mm 铁丝而言,只要氧气浓度达到一定程度就可以燃烧,且氧气浓度越大,燃烧现象越_________ 。(填“剧烈”或“不剧烈”)。
【实验拓展】
小泽认为铁丝燃烧所需氧气最低浓度为 60%,你认为该结论是否合理,请说出理由?________ (填“合理”或“不合理”),理由:_________ 。
(1)实验时要用砂纸擦去铁丝表面的铁锈,该过程属于
(2)铁丝在氧气中燃烧的化学式表达式为
(3)小泽同学实验时,集气瓶炸裂了,请你帮助他分析一下可能的原因
(4)探究直径为 0.38mm 的铁丝燃烧是否需要纯净的氧气:
【实验内容】
取 0.38mm 的铁丝,分别在体积分数为 90%、70%、65%、60%、55%的氧气中进行实验, 实验现象如下表所示:
| O2 的体积分数 | 90% | 70% | 65% | 60% | 55% |
实验现象 | 燃烧剧烈、燃烧时间长,效果好 | 燃烧比 90% 弱,燃烧时间短,实验成功 | 燃烧比 70% 弱,燃烧时间比 70%短,实验成功 | 燃烧比 65% 弱,燃烧时间更短,实验成功 | 难以燃烧,只是发红 |
【实验结论】
就 0.38mm 铁丝而言,只要氧气浓度达到一定程度就可以燃烧,且氧气浓度越大,燃烧现象越
【实验拓展】
小泽认为铁丝燃烧所需氧气最低浓度为 60%,你认为该结论是否合理,请说出理由?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组对双氧水的分解速率受外界条件的影响进行探究。
【提出问题】双氧水的分解速率受哪些外界条件的影响?
【猜想与假设】双氧水的分解速率受催化剂、浓度、温度等影响。
【设计并实验】如图1组装装置。
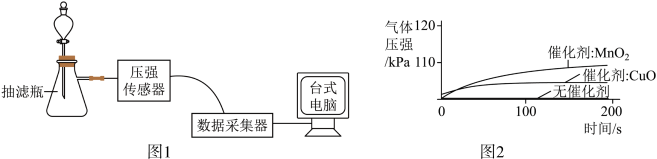
实验一:按如表添加物质,然后打开仪器a活塞,采集数据,得到如图所示的装置内压强-时间图像。
(1)图1装置还可用于实验室制________ 气体,写出反应的化学方程式 _________ 。
(2)从实验一得出的实验结论是__________ 。
实验二:按如表添加物质,然后打开仪器a活塞,采集数据,得到如图3所示的装置内压强一时间图像。

(3)实验二的探究目的是_________ 。
(4)从实验一中的③号瓶与实验二中的②号瓶比较,发现同为40s时装置内压强一时间图像有显著差异,其原因可能是_________ 。
(5)设计实验验证双氧水分解速率受温度的影响:________ 。
【提出问题】双氧水的分解速率受哪些外界条件的影响?
【猜想与假设】双氧水的分解速率受催化剂、浓度、温度等影响。
【设计并实验】如图1组装装置。

实验一:按如表添加物质,然后打开仪器a活塞,采集数据,得到如图所示的装置内压强-时间图像。
| 实验 | 抽滤瓶 | 抽法瓶中盛放物质 | 分液漏斗盛放物质 |
| 1 | ① | 无任何试剂 | 20mL4%的H2O2溶液 |
| 2 | ② | 0.2gMmO2粉末 | 20mL4%的H2O2溶液 |
| 3 | ③ | 0.2gCuO粉末 | 20mL4%的H2O2溶液 |
(1)图1装置还可用于实验室制
(2)从实验一得出的实验结论是
实验二:按如表添加物质,然后打开仪器a活塞,采集数据,得到如图3所示的装置内压强一时间图像。
| 实验 | 抽滤瓶 | 抽法瓶中盛放物质 | 分液漏斗盛放物质 |
| 1 | ① | 0.2gCuO粉末 | 20mL2%的H2O2溶液 |
| 2 | ② | 0.2gCuO粉末 | 20mL4%的H2O2溶液 |
| 3 | ③ | 0.2gCuO粉末 | 20mL6%的H2O2溶液 |

(3)实验二的探究目的是
(4)从实验一中的③号瓶与实验二中的②号瓶比较,发现同为40s时装置内压强一时间图像有显著差异,其原因可能是
(5)设计实验验证双氧水分解速率受温度的影响:
您最近一年使用:0次
【推荐2】二氧化锰是氯酸钾分解的催化剂。某兴趣小组发现,氧化铜(CuO)也能加快氯酸钾的分解,该实验小组进行了如下探究。
[提出猜想]除二氧化锰外,CuO也可作氯酸钾分解的催化剂。
[实验探究]按下表进行实验并获得相关数据。
[分析数据,得出结论]
(1)实验③中将5g氯酸钾、______ CuO放于试管中,加热,然后______ 。
(2)由实验①与实验③对比,证明猜想合理的依据是______ 。
(3)相同条件下对氯酸钾分解催化效果最好的是______ ,写出对应的符号表达式:______ ,该反应属于______ (填基本反应类型)。
[实验反思]
(4)若要确定CuO是该反应的催化剂,还要证明其在化学反应前后______ 不变。
(5)同种催化剂,质量多少可能影响氯酸钾分解的催化效果,还有哪些因素可能影响氯酸钾分解的催化效果?请说出一种你的猜想:______ 。
[提出猜想]除二氧化锰外,CuO也可作氯酸钾分解的催化剂。
[实验探究]按下表进行实验并获得相关数据。
| 实验编号 | 实验药品 | 分解温度/℃ |
| ① | 5g氯酸钾 | 580 |
| ② | 5g氯酸钾,1g二氧化锰 | 350 |
| ③ | 5g氯酸钾,______CuO | 370 |
(1)实验③中将5g氯酸钾、
(2)由实验①与实验③对比,证明猜想合理的依据是
(3)相同条件下对氯酸钾分解催化效果最好的是
[实验反思]
(4)若要确定CuO是该反应的催化剂,还要证明其在化学反应前后
(5)同种催化剂,质量多少可能影响氯酸钾分解的催化效果,还有哪些因素可能影响氯酸钾分解的催化效果?请说出一种你的猜想:
您最近一年使用:0次
【推荐3】研究表明许多金属氧化物对氯酸钾或过氧化氢分解有催化作用。
(1)分别用下列金属氧化物作催化剂,氯酸钾开始分解和剧烈分解时的温度如下表所示:
从节省能源角度看,若实验室无MnO2,可选用___________ ,原因是___________ 。用所选物质催化分解氯酸钾的符号表达式为___________ 。
(2)某小组欲比较CuO与MnO2催化分解过氧化氢的效率,进行如下实验。实验时间均以生成50mL气体为准,其他可能的影响因素忽略不计。
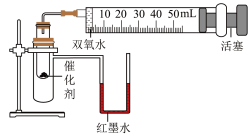
①实验2中x的数值是___________ 。
②表格中的“待测数据”是___________ 。
③实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U形管内右侧液面上升,原因是___________ 。
④结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是___________ 。
(1)分别用下列金属氧化物作催化剂,氯酸钾开始分解和剧烈分解时的温度如下表所示:
| 温度(℃) | Fe2O3 | Al2O3 | CuO | MgO |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
(2)某小组欲比较CuO与MnO2催化分解过氧化氢的效率,进行如下实验。实验时间均以生成50mL气体为准,其他可能的影响因素忽略不计。
| 实验序号 | 过氧化氢溶液 | 催化剂 | 待测数据 |
| 实验1 | 5mL4% | 粉末状MnO2 0.2g | a |
| 实验2 | 5mL4% | 粉末状CuO xg | b |

①实验2中x的数值是
②表格中的“待测数据”是
③实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据,实验过程中发现U形管内右侧液面上升,原因是
④结论:MnO2对过氧化氢分解的催化效果比CuO好,得出该结论的依据是
您最近一年使用:0次



