学习了二氧化锰对过氧化氢分解的催化作用后,某同学产生了两个疑问:(1)其它物质能作过氧化氢分解的催化剂吗?(2)催化剂参与化学反应吗?于是他进行了以下探究,结合实验过程,回答下列问题:
查资料得: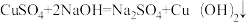 ,其中Cu(OH)2是蓝色沉淀。
,其中Cu(OH)2是蓝色沉淀。
结论:硫酸铜也可以作过氧化氢分解的催化剂,催化剂参与了化学反应。
(1)实验中试管a的作用是______ ,X=______ 。
(2)步骤②中的现象还有______ 。
(3)步骤④可以得出的结论有______。
(4)实验中能证明催化剂参与了化学反应的步骤是______ 。(填序号)
查资料得:
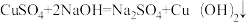 ,其中Cu(OH)2是蓝色沉淀。
,其中Cu(OH)2是蓝色沉淀。| 操作步骤 | 现象 | 结论 |
| ①在试管a中取硫酸铜固体1g,加入5mL蒸馏水,振荡 | 固体完全溶解,溶液为蓝色 | 硫酸铜固体溶于水 |
| ②在试管b中取XmL20%双氧水,伸入带火星木条 | 无明显现象 | 双氧水自然分解很慢 |
| ③在上述试管b中加入1g硫酸铜固体后,伸入带火星木条 | 溶液先变黄,最终变为与①中一样的蓝色溶液,______ | 硫酸铜能加快双氧水的分解 |
| ④分别向试管a、试管b中加入足量NaOH溶液,分离得到的沉淀并称量 | 均产生蓝色沉淀,分离后称量,质量相等 | ______ |
(1)实验中试管a的作用是
(2)步骤②中的现象还有
(3)步骤④可以得出的结论有______。
| A.硫酸铜加快了过氧化氢的分解 | B.硫酸铜的质量没有改变 |
| C.硫酸铜的化学性质没有改变 | D.硫酸铜参与了过氧化氢的分解 |
更新时间:2022-11-18 09:43:28
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某小组用如图所示装置探究影响H2O2分解反应速率的因素(部分装置略去)。
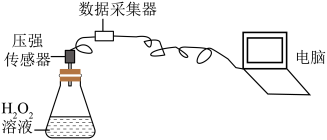
【实验方案】
Ⅰ.相同温度下,按下表进行实验,得到的数据如图 所示:
所示:
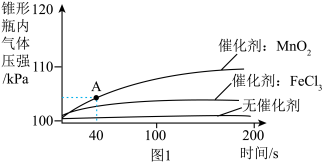
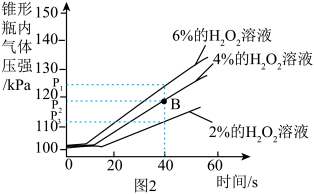
Ⅱ.某温度下,量取15mLH2O2溶液,加入0.2gMnO2粉末进行实验。仅改变H2O2溶液的浓度,得到的实验数据如图2。
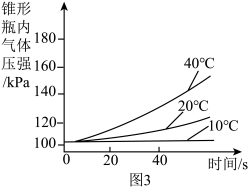
Ⅲ.量取15mL4%的H2O2溶液,加入0.2gMnO2粉末进行实验。仅改变反应温度,得到的实验数据如图3。
【解释与结论】
(1)③中,x=_______ 。
(2)对比①和②,目的是_______ 。
(3)依据图2分析,能证明H2O2溶液的浓度对H2O2分解反应速率有影响的依据是_______ 。
【反思与评价】
(4)请结合实验分析,图1、图2中4%的H2O2溶液与0.2gMnO2粉末混合后产生的气体压强明显不同(即图中A点与B点),可能的原因是_______ 。
(5)讨论后,同学们认为还可以研究_______ 对H2O2分解反应速率的影响。

【实验方案】
Ⅰ.相同温度下,按下表进行实验,得到的数据如图
 所示:
所示:| 实验编号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 催化剂 |
| ① | 4% | 15 | 无催化剂 |
| ② | 4% | 15 | 0.2gMnO2粉末 |
| ③ | 4% | 15 | xgFeCl3粉末 |

Ⅱ.某温度下,量取15mLH2O2溶液,加入0.2gMnO2粉末进行实验。仅改变H2O2溶液的浓度,得到的实验数据如图2。
Ⅲ.量取15mL4%的H2O2溶液,加入0.2gMnO2粉末进行实验。仅改变反应温度,得到的实验数据如图3。


【解释与结论】
(1)③中,x=
(2)对比①和②,目的是
(3)依据图2分析,能证明H2O2溶液的浓度对H2O2分解反应速率有影响的依据是
【反思与评价】
(4)请结合实验分析,图1、图2中4%的H2O2溶液与0.2gMnO2粉末混合后产生的气体压强明显不同(即图中A点与B点),可能的原因是
(5)讨论后,同学们认为还可以研究
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ.CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后_______
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
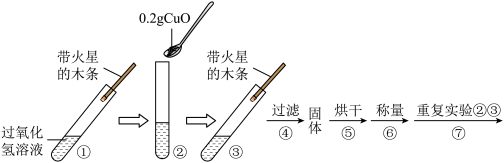
(1)填空:步骤②的现象是_______ ,带火星的木条复燃;步骤⑥的结果是_______ :
(2)步骤①的目的是_______ 。
(3)过氧化氢能被CuO催化分解放出O2的化学反应式为_______ 。
【猜想】Ⅰ.CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;
Ⅱ.CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ.CuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填空:步骤②的现象是
(2)步骤①的目的是
(3)过氧化氢能被CuO催化分解放出O2的化学反应式为
您最近一年使用:0次
【推荐3】学校化学兴趣小组知道二氧化锰能作过氧化氢分解的催化剂后,还想探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂。请你一起参与他们的探究过程,并填写下列空白。
【提出问题】A12O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】A12O3能作过氧化氢分解的催化剂。
【实验验证】
实验一,_____________ ,木条不复燃;结论,常温下过氧化氢溶液分解缓慢。
实验二,在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中,_____________ ,说明Al2O3,加快了过氧化氢的分解速率。
【实验结论】Al2O3能加快过氧化氢的分解速率,故A12O3能作过氧化氢分解的催化剂。
【讨论与反思】经过讨论,有的同学认为根据上述两个实验,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:探究____________
【实验步骤】
①准确称量Al2O3(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,_________ ,称量;
④对比反应前后Al2O3的质量。
【讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验探究____________ 。
【拓展反思1】影响化学反应的因素除催化剂外,还有哪些呢?在空气中加热铁丝,铁丝只能发生红热现象,不能燃烧:但在氧气里点燃细铁丝可发生____________ ,火星四射;带火星的木条在空气中不能燃烧,但在氧气里复燃。这说明反应物____________ 越大,反应速度越快。
【拓展反思2】碳在常温下不与氧气反应,点燃时能与氧气反应,这说明反应物 越高,反应速度越快。
【提出问题】A12O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】A12O3能作过氧化氢分解的催化剂。
【实验验证】
实验一,
实验二,在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中,
【实验结论】Al2O3能加快过氧化氢的分解速率,故A12O3能作过氧化氢分解的催化剂。
【讨论与反思】经过讨论,有的同学认为根据上述两个实验,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:探究
【实验步骤】
①准确称量Al2O3(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,
④对比反应前后Al2O3的质量。
【讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验探究
【拓展反思1】影响化学反应的因素除催化剂外,还有哪些呢?在空气中加热铁丝,铁丝只能发生红热现象,不能燃烧:但在氧气里点燃细铁丝可发生
【拓展反思2】碳在常温下不与氧气反应,点燃时能与氧气反应,这说明反应物 越高,反应速度越快。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】“曾青得铁化为铜”出自我国西汉刘安所著《淮南万毕术》。是现代湿法炼铜的先驱。表明我国很早就开始利用硫酸铜。同学们结合教材所学知识开始对硫酸铜进行如下项目研究。
【研究项目一】硫酸铜用途
(1)用硫酸铜和石灰乳混合可以配制农药“波尔多液”,反应的化学方程式为______ 。
(2)“波尔多液”不能用铁质容器存放,理由是____________ 。
【研究项目二】制备硫酸铜的原理
方案1: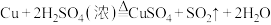
方案2: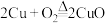

(3)化学产品制备要向着绿色、低碳、可持续的方向发展。请分析上述两个方案中,不符合这一方向的是方案1,理由是____________ 。
(4)查阅资料可知,方案3: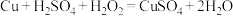
在老师指导下得知:制备硫酸铜过程中, 会发生分解反应,于是进行如下实验:
会发生分解反应,于是进行如下实验:
【发现问题】
上述方案3的实验现象中为什么开始气泡少,而后反应剧烈并出现大量气泡。是什么因素加快 分解?
分解?
【提出猜想】
(5)猜想一:生成的 猜想二:温度升高 猜想三:
猜想二:温度升高 猜想三:______ 。
【实验探究】
【实验分析】
(6)对比实验①②可得出的结论是____________ 。
(7)为了验证温度升高能加快 的分解,小红同学的方案是实验①③对比。小丽同学的方案是实验①④对比。你认为
的分解,小红同学的方案是实验①③对比。小丽同学的方案是实验①④对比。你认为______ 同学的方案更严谨,理由是______ 。
(8)通过对比实验①②③④,可得出的结论是______ 。
【研究项目三】探究 溶液中能加快
溶液中能加快 的分解的是哪种微观粒子。
的分解的是哪种微观粒子。
查阅资料: 溶液中含有、
溶液中含有、 ,
, 溶液中含有
溶液中含有 、
、 。
。
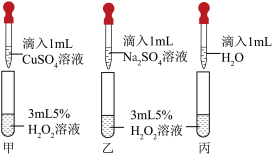
(9)同学们设计了如图所示的对比实验。若观察到______ (填实验现象),则说明 溶液中能加快
溶液中能加快 的分解的是
的分解的是 。
。
【研究项目一】硫酸铜用途
(1)用硫酸铜和石灰乳混合可以配制农药“波尔多液”,反应的化学方程式为
(2)“波尔多液”不能用铁质容器存放,理由是
【研究项目二】制备硫酸铜的原理
方案1:
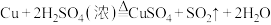
方案2:
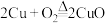

(3)化学产品制备要向着绿色、低碳、可持续的方向发展。请分析上述两个方案中,不符合这一方向的是方案1,理由是
(4)查阅资料可知,方案3:
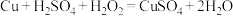
在老师指导下得知:制备硫酸铜过程中,
 会发生分解反应,于是进行如下实验:
会发生分解反应,于是进行如下实验:| 实验操作 | 实验现象 | 结论 |
| 将反应物装入试管中,观察 | 开始有少量气泡,而后反应剧烈,出现大量气泡,溶液呈蓝色,试管外壁发热。 | 气体是 |
| 将带火星的木条放在试管口 | 木条复燃 |
【发现问题】
上述方案3的实验现象中为什么开始气泡少,而后反应剧烈并出现大量气泡。是什么因素加快
 分解?
分解?【提出猜想】
(5)猜想一:生成的
 猜想二:温度升高 猜想三:
猜想二:温度升高 猜想三:【实验探究】
| 序号 | ① | ② | ③ | ④ |
| 实验操作 | 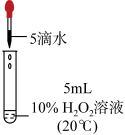 | 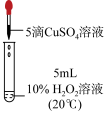 | 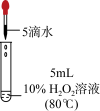 | 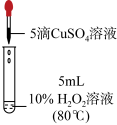 |
| 现象 | 无明显现象 | 出现气泡 | 出现气泡 | 快速出现气泡 |
(6)对比实验①②可得出的结论是
(7)为了验证温度升高能加快
 的分解,小红同学的方案是实验①③对比。小丽同学的方案是实验①④对比。你认为
的分解,小红同学的方案是实验①③对比。小丽同学的方案是实验①④对比。你认为(8)通过对比实验①②③④,可得出的结论是
【研究项目三】探究
 溶液中能加快
溶液中能加快 的分解的是哪种微观粒子。
的分解的是哪种微观粒子。查阅资料:
 溶液中含有、
溶液中含有、 ,
, 溶液中含有
溶液中含有 、
、 。
。(9)同学们设计了如图所示的对比实验。若观察到
 溶液中能加快
溶液中能加快 的分解的是
的分解的是 。
。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变。
Ⅱ、CuO参与反应产生O2 ,反应前后质量和化学性质发生了改变。
Ⅲ、CuO是反应的催化剂,反应前后________________ 。
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
(2)步骤①的目的是_____________________ 。
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__________ 。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为_____________________ 。
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变。
Ⅱ、CuO参与反应产生O2 ,反应前后质量和化学性质发生了改变。
Ⅲ、CuO是反应的催化剂,反应前后
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃。 | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立。 |
(2)步骤①的目的是
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】如下图为初中化学教材中探究二氧化锰在过氧化氢分解中的催化作用。请你参与探究活动并回答下列问题:(已知:过氧化氢在常温下可以分解产生氧气)
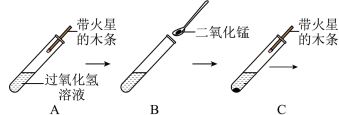
(1)图A试管中盛有5mL5%的过氧化氢溶液,将带火星的木条伸入试管内,没有观察到明显现象,原因是_______ 。
(2)如图B,在试管中加入少量二氧化锰,并将带火星的木条伸入试管内,如图C,观察到的现象是_______ ,写出该反应的文字(或符号)表达式_______ 。
(3)待图C试管中无现象时,向其中再次添加过氧化氢溶液,并把带火星的木条伸入试管内,观察现象,重复该操作多次,均观察到相同的现象,说明_______ 。如果用精密的天平称量反应前后二氧化锰的质量,发现_______ 。
【拓展探究】兴趣小组用按图1所示装置进行如下实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。
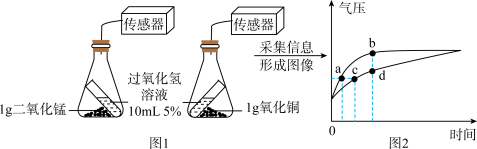
(4)对比分析图2中的_______ 两点(填字母符号),可知化学反应速率与催化剂的种类有关。
(5)请从催化剂的角度解释,在实验过程中,上述3个反应虽然化学反应速率不同,但完全反应后两个装置内压强相同的原因是_______ 。

(1)图A试管中盛有5mL5%的过氧化氢溶液,将带火星的木条伸入试管内,没有观察到明显现象,原因是
(2)如图B,在试管中加入少量二氧化锰,并将带火星的木条伸入试管内,如图C,观察到的现象是
(3)待图C试管中无现象时,向其中再次添加过氧化氢溶液,并把带火星的木条伸入试管内,观察现象,重复该操作多次,均观察到相同的现象,说明
【拓展探究】兴趣小组用按图1所示装置进行如下实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。

(4)对比分析图2中的
(5)请从催化剂的角度解释,在实验过程中,上述3个反应虽然化学反应速率不同,但完全反应后两个装置内压强相同的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】碘是人体生长发育必需的微量元素,加碘食盐主要有两种,添加KI(碘化钾)或KIO3。
(1)食盐中加入碘酸钾的目的是补充微量元素碘,它的主要作用是预防______ 。
【实验探究一】加碘食盐中含碘钾盐的成分是什么?
作出猜想:猜想1:KI;
猜想2:KIO3;
猜想3:KI和KIO3的混合物
查阅资料:
①KIO3与KI在酸性条件下能发生反应生成碘(I2),淀粉溶液遇I2变蓝色;
②KI能与AgNO3溶液反应,生成不溶于水的黄色AgI沉淀,但是KIO3与AgNO3溶液混合,无明显现象。
③I2有毒,不能服用
(2)小组同学根据资料进行讨论后,认为上述猜想______ 不正确,理由是______ 。
(3)实验验证:为验证其他猜想,小组同学设计了如下实验,请填写表格中空白处。
实验结论:根据上述实验推理,加碘食盐中含碘钾盐是KIO3。
【实验探究二】
(4)为什么做菜在起锅时,才加入碘盐呢?
查阅资料:碘酸钾受热易分解产生碘化钾和氧气。反应的化学方程式是______ 。
KI中仍含有碘元素,为什么生成KI就会降低碘效?
查阅资料:KI是白色固体,在空气中与O2、CO2、H2O中的两种或三种物质反应生成单质I2而泛黄变质。光照会加速它的变质,不利于人体吸收。
(5)实验探究:研究小组开展以下实验。请将现象补充完整。
【交流反思】
(6)讨论后大家认为以上实验方案有所欠缺。甲同学做了补充实验,该实验密封的试管中除了KI固体外,还有______ ,数日后观察无明显现象,证明以上结论正确。
(1)食盐中加入碘酸钾的目的是补充微量元素碘,它的主要作用是预防
【实验探究一】加碘食盐中含碘钾盐的成分是什么?
作出猜想:猜想1:KI;
猜想2:KIO3;
猜想3:KI和KIO3的混合物
查阅资料:
①KIO3与KI在酸性条件下能发生反应生成碘(I2),淀粉溶液遇I2变蓝色;
②KI能与AgNO3溶液反应,生成不溶于水的黄色AgI沉淀,但是KIO3与AgNO3溶液混合,无明显现象。
③I2有毒,不能服用
(2)小组同学根据资料进行讨论后,认为上述猜想
(3)实验验证:为验证其他猜想,小组同学设计了如下实验,请填写表格中空白处。
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量加碘食盐于试管中,加水溶解, 再向试管中滴加AgNO3溶液 | 猜想1不成立 | |
| 实验二 | 另取少量加碘食盐于试管中,加水溶解, 先向试管中滴加稀硫酸酸化的KI溶液, 再滴入 | 溶液有无色变成蓝色 | 猜想2成立 |
【实验探究二】
(4)为什么做菜在起锅时,才加入碘盐呢?
查阅资料:碘酸钾受热易分解产生碘化钾和氧气。反应的化学方程式是
KI中仍含有碘元素,为什么生成KI就会降低碘效?
查阅资料:KI是白色固体,在空气中与O2、CO2、H2O中的两种或三种物质反应生成单质I2而泛黄变质。光照会加速它的变质,不利于人体吸收。
(5)实验探究:研究小组开展以下实验。请将现象补充完整。
| 实验操作 | 现象 | |
| 如图所示,在燃烧匙中加入KI 固体,然后分别放置在①②③ 号试管中,数日后观察现象。 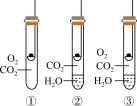 | KI固体在空气中与O2。 CO2、H2O共同作用而 变质导致碘效降低 |
【交流反思】
(6)讨论后大家认为以上实验方案有所欠缺。甲同学做了补充实验,该实验密封的试管中除了KI固体外,还有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】纯水的导电能力很弱,电解水时常在水中加入一些氢氧化钠增强导电性。为研究影响电解水反应速率的因素,某课外活动小组进行了实验探究,数据记录如下表(直流电,电压:12V)
请回答问题:
(1)电解水反应的文字表达式为_____ ;
(2)该小组研究的影响电解水反应速率的因素是_____ 和溶液浓度。
(3)本实验通过比较_____ 确定电解水速率的快慢。
(4)比较实验A和C,可得到的结论是_____ ;
(5)分析实验A、B、C的数据,实验D的电解时间“X”可能是_____ ;
A 35.4 B 37.8 C 50.2 D 55.6
(6)理论上,电解水产生氢气、氧气的体积比为2:1,但实验结果比理论值大,可能的原因是_____ (答一点即可)。
| 实验编号 | 温度(℃) | NaOH溶液浓度(%) | H2体积 (mL) | O2体积 (mL) | 电解时间(s) |
| A | 20 | 2% | 20 | 9.8 | 54.0 |
| B | 20 | 5% | 20 | 9.8 | 36.2 |
| C | 30 | 2% | 20 | 9.6 | 46.2 |
| D | 30 | 5% | 20 | 9.7 | X |
请回答问题:
(1)电解水反应的文字表达式为
(2)该小组研究的影响电解水反应速率的因素是
(3)本实验通过比较
(4)比较实验A和C,可得到的结论是
(5)分析实验A、B、C的数据,实验D的电解时间“X”可能是
A 35.4 B 37.8 C 50.2 D 55.6
(6)理论上,电解水产生氢气、氧气的体积比为2:1,但实验结果比理论值大,可能的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】维生素C(简写Vc)易溶于水,易被氧化。人体缺乏Vc可能引发多种疾病。水果和蔬菜中含有丰富的Vc。某研究性学习小组对Vc进行探究。
探究一:测定饮料中Vc的含量。
【查阅资料】Vc能与高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有1 mL等浓度高锰酸钾稀溶液的四支试管中逐滴滴加果味饮料、苹果汁、梨汁和梨汁,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
【实验结论】分析数据可知,Vc含量最高的是_________ ,含量为_____ (各液体密度上的差别和每一滴的体积差别忽略不计)。
探究二:蔬菜放置时间的长短对其Vc的含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案______ 。
【实验结论】按上述方案进行实验,根据_____ 这一结果,可知蔬菜放置时间的长短对其Vc的含量有影响。
【实验反思】化学实验需要控制变量。下列情况不会影响到测定结果的是______ 。
A.每次实验所用的果汁颜色不同
B.量取的被测物质的体积不同
C.试管的大小不同
D.没有用同一规格的胶头滴管滴加
探究一:测定饮料中Vc的含量。
【查阅资料】Vc能与高锰酸钾反应,使紫色的高锰酸钾溶液褪色。
【设计方案】分别向盛有1 mL等浓度高锰酸钾稀溶液的四支试管中逐滴滴加果味饮料、苹果汁、梨汁和梨汁,边滴边振荡,直至高锰酸钾溶液褪色。
【实验数据】
| 果味饮料 | 苹果汁 | 梨汁 | 0.04%的Vc溶液 | |
| 滴加的滴数 | 40 | 10 | 20 | 5 |
【实验结论】分析数据可知,Vc含量最高的是
探究二:蔬菜放置时间的长短对其Vc的含量是否有影响。
【设计方案】请你用新鲜的黄瓜、放置一周的黄瓜、高锰酸钾稀溶液和必要的仪器设计实验方案
【实验结论】按上述方案进行实验,根据
【实验反思】化学实验需要控制变量。下列情况不会影响到测定结果的是
A.每次实验所用的果汁颜色不同
B.量取的被测物质的体积不同
C.试管的大小不同
D.没有用同一规格的胶头滴管滴加
您最近一年使用:0次



