在实验室里,某化学实验小组利用下图所示的装置进行模拟炼铁实验原理。

(1)A处玻璃管内所发生反应的化学方程式是______ ;
(2)B处可观察到的现象是______ ;C处酒精灯的作用是______ 。
(3)已知该实验小组称取50g含有杂质的黑色样品装入直玻璃管中,通入足量的CO后充分反应后,待装置冷却,称得直玻璃管中剩余固体的质量为46.8g,其中杂质不参与反应。试计算原黑色样品中Fe3O4的质量分数。

(1)A处玻璃管内所发生反应的化学方程式是
(2)B处可观察到的现象是
(3)已知该实验小组称取50g含有杂质的黑色样品装入直玻璃管中,通入足量的CO后充分反应后,待装置冷却,称得直玻璃管中剩余固体的质量为46.8g,其中杂质不参与反应。试计算原黑色样品中Fe3O4的质量分数。
更新时间:2022-11-18 20:49:04
|
相似题推荐
综合应用题
|
较难
(0.4)
解题方法
【推荐1】某厂采用臭氧氧化—钙法吸收工艺对锅炉烟气(含N2、空气、NO、SO2等)进行同时脱硫(SO2)脱硝(NOx)处理,减少了设备建设用地,下图为主要吸收装置——鼓泡反应器。请回答:
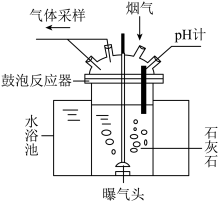
(1)NO和O3反应产物除生成NO2外,还生成能使带火星木条复燃的气体,反应的化学方程式为____ ,属于 ____ 反应(填基本反应类型)。
(2)鼓泡反应器中SO2和石灰水反应生成CaSO3和水,反应的化学方程式____ 。
(3)鼓泡反应器放在水浴槽中,控制温度35℃,水浴加热的优点是____ 。曝气头为半球形,作用是 ____ 。
(4)下图是同时脱硫(SO2)脱硝(NOx)与单独脱硫、脱硝去除率的对比图。

①分析图像,你认为同时脱硫脱硝在工业生产中的优势是____ 、 ____ 。
②左图中,50min后SO2去除率明显降低的原因可能是____ 。
(5)计算单独脱硫时,1吨质量分数为0.15%的石灰水理论上可吸收SO2气体的质量是___ 克?(精确到小数点后一位)

(1)NO和O3反应产物除生成NO2外,还生成能使带火星木条复燃的气体,反应的化学方程式为
(2)鼓泡反应器中SO2和石灰水反应生成CaSO3和水,反应的化学方程式
(3)鼓泡反应器放在水浴槽中,控制温度35℃,水浴加热的优点是
(4)下图是同时脱硫(SO2)脱硝(NOx)与单独脱硫、脱硝去除率的对比图。

①分析图像,你认为同时脱硫脱硝在工业生产中的优势是
②左图中,50min后SO2去除率明显降低的原因可能是
(5)计算单独脱硫时,1吨质量分数为0.15%的石灰水理论上可吸收SO2气体的质量是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】实验是科学探究的重要手段,气体的制取及合理利用使人类生活向环境友好方向发展。
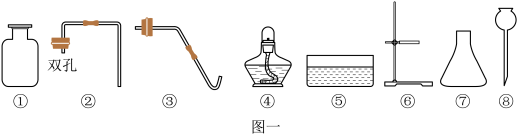
(1)利用图一仪器可以实验室制取二氧化碳,你选择的仪器是____ (填序号),反应原理是______ (用化学方程式表示),若将仪器⑧换成分液漏斗,则装置具备的优点是_______ 。
(2)实验室若用固体制取氧气,除利用上述仪器外,还需补充的一种仪器是_______ (填名称),其反应的化学方程式为_______ ,氧气可用排水法收集,利用了氧气_______ 的性质。
(3)为测定某石灰石样品中碳酸钙的含量,小明同学取了6g石灰石样品与足量的稀盐酸反应,得到2.2g的二氧化碳气体,请计算该石灰石样品中含有多少克碳酸钙?

(1)利用图一仪器可以实验室制取二氧化碳,你选择的仪器是
(2)实验室若用固体制取氧气,除利用上述仪器外,还需补充的一种仪器是
(3)为测定某石灰石样品中碳酸钙的含量,小明同学取了6g石灰石样品与足量的稀盐酸反应,得到2.2g的二氧化碳气体,请计算该石灰石样品中含有多少克碳酸钙?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
【推荐3】利用海水吸收含硫烟气中的SO2并生产石膏(主要成分为CaSO4·2H2O)的主要物质转化关系如下:___________ 。
(2)反应釜中,石灰石在加入前,将其粉碎的目的是___________ 。
(3)现取40.8g石膏进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。
①石膏开始分解的温度是___________ ,CaSO4·2H2O受热分解的方程式为___________ 。
②计算40.8g该石膏样品中含有CaSO4·2H2O的质量___________ 。(写出计算过程)
③1350-1500℃时,CaSO4继续分解生成氧化钙、二氧化硫和氧气,最终剩余的17.6g固体中含有CaO的质量为___________ 。
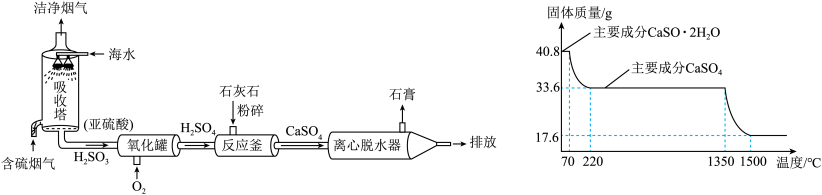
(2)反应釜中,石灰石在加入前,将其粉碎的目的是
(3)现取40.8g石膏进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。
①石膏开始分解的温度是
②计算40.8g该石膏样品中含有CaSO4·2H2O的质量
③1350-1500℃时,CaSO4继续分解生成氧化钙、二氧化硫和氧气,最终剩余的17.6g固体中含有CaO的质量为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】“科技梦”助推“中国梦”,嫦娥探月、北斗组网、天和升空、蛟龙潜海、高铁纵横,都离不开化学。
(1)嫦娥五号返回器携带 1731g月球土壤成功着落。
①因为 N2的化学性质______ (填“活泼”或“稳定"),故被用于保存月球土壤。
②嫦娥探月重要目的是寻找新能源 He-3,其原子的相对原子质量为3,则 He-3 原子核内中子数为_______ 。
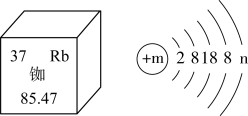
(2)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则n 的值为为______ 。
(3)“天和核心舱”由长征五号 B 遥二运载火箭发射升空,火箭采用液氢、液氧和煤油作为推进剂,利用液氢作燃料的优点是_______ ,生产煤油的原料是_______ 。
(4)蛟龙号耐压球壳使用了钛合金,下图是以钛酸亚铁(FeTiO3)为原料制取钛(Ti)的部分流程图。

①步骤 I 中反应时要先将钛铁矿和焦炭粉碎,目的是_____ 。
②物质 X 为一种有毒气体,反应 II 合成甲醇(CH3OH)时,按照绿色化学的原则,应调节原料中X 和 H2的分子个数比为_______ 。
③反应 III 中分出 TiCl4的蒸馏法是利用物质的______ 不同。
④反应 IV 需在氩气(Ar)环境下进行,Ar 的作用是_______ 。
(5)制造高铁使用了许多金属材料,现烧杯中有铜和氧化铜的混合物 12.8 克,加入一定量的稀硫酸,当稀硫酸全部反应完时,烧杯中所得溶液的质量为 108 克,剩余固体质量为 4.8 克。计算所用稀硫酸的溶质质量分数(写出计算过程)。
(1)嫦娥五号返回器携带 1731g月球土壤成功着落。
①因为 N2的化学性质
②嫦娥探月重要目的是寻找新能源 He-3,其原子的相对原子质量为3,则 He-3 原子核内中子数为
(2)北斗导航卫星系统用铷原子钟提供精确时间。铷元素在元素周期表中的相关信息及原子结构示意图如图,则n 的值为为

(3)“天和核心舱”由长征五号 B 遥二运载火箭发射升空,火箭采用液氢、液氧和煤油作为推进剂,利用液氢作燃料的优点是
(4)蛟龙号耐压球壳使用了钛合金,下图是以钛酸亚铁(FeTiO3)为原料制取钛(Ti)的部分流程图。

①步骤 I 中反应时要先将钛铁矿和焦炭粉碎,目的是
②物质 X 为一种有毒气体,反应 II 合成甲醇(CH3OH)时,按照绿色化学的原则,应调节原料中X 和 H2的分子个数比为
③反应 III 中分出 TiCl4的蒸馏法是利用物质的
④反应 IV 需在氩气(Ar)环境下进行,Ar 的作用是
(5)制造高铁使用了许多金属材料,现烧杯中有铜和氧化铜的混合物 12.8 克,加入一定量的稀硫酸,当稀硫酸全部反应完时,烧杯中所得溶液的质量为 108 克,剩余固体质量为 4.8 克。计算所用稀硫酸的溶质质量分数(写出计算过程)。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl,其它成分不考虑。请回答下列问题:
(1)味精中至少含有__________ (填数字)种元素。
(2)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是_________(填字母)。
(3)下图是配制过程,正确的操作顺序为___________(填字母) 。
(4)为测定NaCl在味精中的质量分数,进行如下实验:
①向所配制的50g溶液中加入AgNO3溶液充分反应,检验沉淀是否完全的方法是:静置后,在上层清液中加入___________ (填化学式)溶液,观察是否有沉淀生成。
②在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中,谷氨酸钠的质量分数_________ (填“偏大”、“偏小”或“无影响”),所测定的味精中NaCI的质量分数______________ (填“偏大”、“偏小”或“无影响”)。
③向所配制的50g溶液中加入足量的AgNO3溶液充分反应后,将沉淀_________ 、洗涤、干燥,精确测定(假定实验过程中沉淀无损耗)沉淀质量为2.87 g,则该味精中NaCl的质量分数为_________ 。(计算结果精确到0.1% )
(1)味精中至少含有
(2)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是_________(填字母)。
| A.5mL | B.10 mL | C.50 mL | D.100 mL |
(3)下图是配制过程,正确的操作顺序为___________(填字母) 。
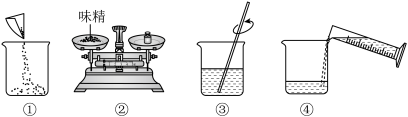
| A.①②③④ | B.②①④③ | C.②④①③ |
(4)为测定NaCl在味精中的质量分数,进行如下实验:
①向所配制的50g溶液中加入AgNO3溶液充分反应,检验沉淀是否完全的方法是:静置后,在上层清液中加入
②在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中,谷氨酸钠的质量分数
③向所配制的50g溶液中加入足量的AgNO3溶液充分反应后,将沉淀
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】金属材料在日常生活中的应用十分广泛,某化学兴趣小组对金属的相关知识进行了探究。
(1)该小组同学要用如图装置做一氧化碳还原氧化铁的实验并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。
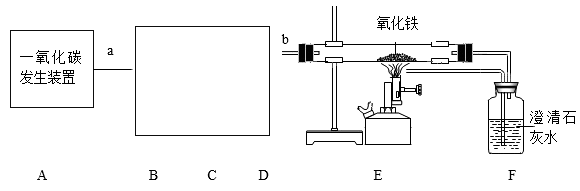
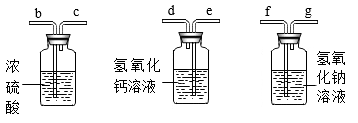
①请将上列装置接入到B、C、D位置中,装置中导管接口从左到右的连接顺序为:a→____
②F装置的作用是_______________________
③写出E装置中发生反应的化学方程式________________________
④实验开始时,使纯净的一氧化碳气体进入E装置一段时间后,再点燃E处酒精喷灯加热的目的是______________________________
(2)某同学将一定量的锌粉加入到AgNO3、Cu(NO3)2、A1(NO3)3的混合溶液中,充分反应后过滤,发现滤液为无色,向滤渣中滴加稀盐酸,没有气泡产生。
①根据现象判断滤渣的成分为____________
②写出将锌粉加入混合溶液中发生反应的化学方程式(任写一个)__________
③反应后溶液质量与原溶液质量相比有可能保持不变,请解释原因__________
(3)为了测定某黄铜样品(铜锌合金)中铜的质量分数,称取10g样品放入烧杯中,加入100g稀硫酸,二者恰好完反应,反应后烧杯中剩余物质的总质量为109.9g,请计算该样品中铜的质量分数__________
(1)该小组同学要用如图装置做一氧化碳还原氧化铁的实验并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。


①请将上列装置接入到B、C、D位置中,装置中导管接口从左到右的连接顺序为:a→
②F装置的作用是
③写出E装置中发生反应的化学方程式
④实验开始时,使纯净的一氧化碳气体进入E装置一段时间后,再点燃E处酒精喷灯加热的目的是
(2)某同学将一定量的锌粉加入到AgNO3、Cu(NO3)2、A1(NO3)3的混合溶液中,充分反应后过滤,发现滤液为无色,向滤渣中滴加稀盐酸,没有气泡产生。
①根据现象判断滤渣的成分为
②写出将锌粉加入混合溶液中发生反应的化学方程式(任写一个)
③反应后溶液质量与原溶液质量相比有可能保持不变,请解释原因
(3)为了测定某黄铜样品(铜锌合金)中铜的质量分数,称取10g样品放入烧杯中,加入100g稀硫酸,二者恰好完反应,反应后烧杯中剩余物质的总质量为109.9g,请计算该样品中铜的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去)
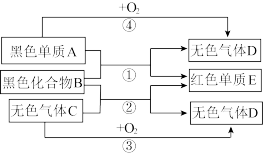
(1)在①②③④中,属于置换反应的是_____________ (填序号)。
(2)反应②的化学方程式是___________ 。
(3)已知H:也具有还原性,现有混合气体由H2、CO和CO2三种气体中一种或几种组成。为验证该混合气体的成分,科学研究小组的同学经过讨论,设计了如图所示的实验方案。
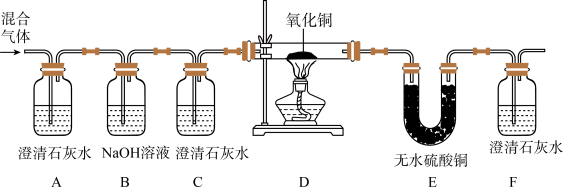
根据方案回答下列问题:
①实验中三处澄清石灰水的作用:A_________ ;C__________ ;F________ 。
②仅根据D装置中黑色粉末变红这一现象能否证明混合气体中一定存在CO?请判断并说明理由:_____________ 。
②小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论___________ (填“是”或“否”)可靠?若可靠,请说明理由;若不可靠,请对实验装置提出改进意见:_____________ 。

(1)在①②③④中,属于置换反应的是
(2)反应②的化学方程式是
(3)已知H:也具有还原性,现有混合气体由H2、CO和CO2三种气体中一种或几种组成。为验证该混合气体的成分,科学研究小组的同学经过讨论,设计了如图所示的实验方案。

根据方案回答下列问题:
①实验中三处澄清石灰水的作用:A
②仅根据D装置中黑色粉末变红这一现象能否证明混合气体中一定存在CO?请判断并说明理由:
②小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】用某含有CO2、水蒸气的还原性气体(可能含有CO、H2中的一种或两种)经过如下图的装置来确定其成分及C装置中FexOy的化学式。(已知:无水硫酸铜粉末遇水变蓝)
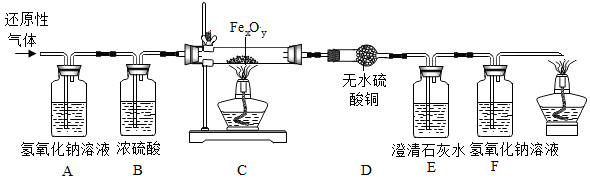
(1)B装置的作用是_______ ,D装置的作用是_______ ;
(2)实验过程中观察到D中无明显变化,E中澄清石灰水变浑浊,则还原性气体是____ ,当C中的FexOy,完全反应后,测得E和F的总重量增加3.52g,C中剩余固体质量为3.36g,则FexOy的化学式为_______ 。若没有A装置,则测得的x和y的比值将_______ (“偏大”、“偏小”或“不变”)。

(1)B装置的作用是
(2)实验过程中观察到D中无明显变化,E中澄清石灰水变浑浊,则还原性气体是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】铜及其化合物在生产、生活中都有广泛的应用。
一、铜的冶炼
资料一:考古工作者从安阳的商代铸铜遗址中,发现当时冶炼铜的主要矿物原料是孔雀石[主要成分是碱式碳酸铜Cu2(OH)2CO3],主要燃料是木炭,冶炼温度估计在1000℃左右。
资料二:西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”。“曾青”可能是硫酸铜一类的物质,将孔雀石溶于硫酸中得此溶液,当把铁粉投入此溶液中即可得铜。
(1)关于“曾青”和孔雀石的说法中,正确的是___ 。
A 前者属于盐,后者的主要成分是碱 B 前者属于酸,后者的主要成分是碱
C 前者和后者的主要成分都属于氧化物 D 前者和后者的主要成分都属于盐
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有__ 。
①Cu2(OH)2CO3 2CuO+CO2↑+H2O ②2CuO+C
2CuO+CO2↑+H2O ②2CuO+C 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C 2CO
2CO
A ①② B ①③ C ①②③ D ①②③④
(3)已知有元素化合价升高和降低的反应属于氧化还原反应。在(2)的四个反应中,不属于四种基本反应类型的有(填序号,下同)____ ,不属于氧化还原反应的有 ____ 。
(4)资料二中,假设溶解孔雀石的酸是稀硫酸,写出用此方法冶炼铜的化学方程式:___ , ___ 。
二、铜及其化合物的应用
(5)碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等。碱式碳酸铜由Na2CO3•10H2O与CuSO4•5H2O反应制备,原理:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2Na2SO4+CO2↑。称取14.0gCuSO4•5H2O、16.0gNa2CO3•10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“嗞嗞”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含SO42﹣为止,取出沉淀,风干,得到蓝绿色晶体。
①混合物发生反应时有“嗞嗞”声的原因是___ 。
②撤离热源的目的是___ 。
组成测定:
有同学查阅资料发现用Cu(OH)2•CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2•nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如下图所示,通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。
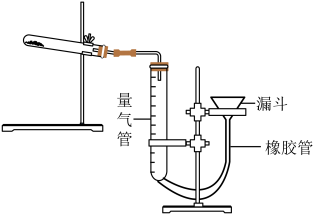
③三次平行实验测定结果如下表,则该样品中m:n=___ ,若量气管中所盛液体是水,则该测定值比理论值 ___ (填“偏大”、“偏小”或“不变”)。(已知该状况下,二氧化碳密度为1.964g/L)
一、铜的冶炼
资料一:考古工作者从安阳的商代铸铜遗址中,发现当时冶炼铜的主要矿物原料是孔雀石[主要成分是碱式碳酸铜Cu2(OH)2CO3],主要燃料是木炭,冶炼温度估计在1000℃左右。
资料二:西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”。“曾青”可能是硫酸铜一类的物质,将孔雀石溶于硫酸中得此溶液,当把铁粉投入此溶液中即可得铜。
(1)关于“曾青”和孔雀石的说法中,正确的是
A 前者属于盐,后者的主要成分是碱 B 前者属于酸,后者的主要成分是碱
C 前者和后者的主要成分都属于氧化物 D 前者和后者的主要成分都属于盐
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有
①Cu2(OH)2CO3
 2CuO+CO2↑+H2O ②2CuO+C
2CuO+CO2↑+H2O ②2CuO+C 2Cu+CO2↑
2Cu+CO2↑③CuO+CO
 Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C 2CO
2COA ①② B ①③ C ①②③ D ①②③④
(3)已知有元素化合价升高和降低的反应属于氧化还原反应。在(2)的四个反应中,不属于四种基本反应类型的有(填序号,下同)
(4)资料二中,假设溶解孔雀石的酸是稀硫酸,写出用此方法冶炼铜的化学方程式:
二、铜及其化合物的应用
(5)碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等。碱式碳酸铜由Na2CO3•10H2O与CuSO4•5H2O反应制备,原理:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2Na2SO4+CO2↑。称取14.0gCuSO4•5H2O、16.0gNa2CO3•10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“嗞嗞”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含SO42﹣为止,取出沉淀,风干,得到蓝绿色晶体。
①混合物发生反应时有“嗞嗞”声的原因是
②撤离热源的目的是
组成测定:
有同学查阅资料发现用Cu(OH)2•CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2•nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如下图所示,通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。

③三次平行实验测定结果如下表,则该样品中m:n=
| 实验序号 | 样品质量/g | CO2体积/mL (已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
您最近一年使用:0次




