某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素(实验装置如图1所示,夹持仪器已略去)
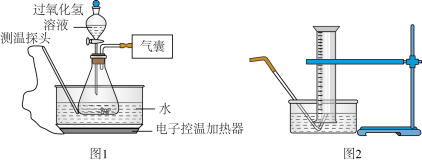
【猜想与假设】影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂种类。
【实验记录】同学们进行6组实验,实验记录如表:
【解释与结论】
(1)实验②中应加入过氧化氢溶液的体积x是_______ mL。
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定____ 来比较过氧化氢的分解速率。
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是_______ (填序号)。
(4)通过实验①、②、④可得出的结论是_______ 。
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是_______ (答一点)。
(6)某同学改用如图2所示装置代替气囊完成实验②,正确的实验操作顺序是_______ 。
a.将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b.开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c.开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒

【猜想与假设】影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂种类。
【实验记录】同学们进行6组实验,实验记录如表:
| 实验序号 | ① | ② | ③ | ④ | ⑤ | 6 |
| 过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
| 过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
| 水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
| 锥形瓶中的物质 | _______ | _______ | _______ | _______ | 0.5gNaCl | 0.5gFeCl3 |
| 60min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(1)实验②中应加入过氧化氢溶液的体积x是
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是
(4)通过实验①、②、④可得出的结论是
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是
(6)某同学改用如图2所示装置代替气囊完成实验②,正确的实验操作顺序是
a.将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b.开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c.开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒
22-23九年级上·河北廊坊·期中 查看更多[5]
河北省廊坊市第六中学2022-2023学年九年级上学期期中化学试题北京市一零一教育集团2022-2023学年九年级下学期3月化学练习河北省张家口市桥西区2022-2023学年九年级上学期期中化学试题安徽省滁州市定远县吴圩片2022-2023学年九年级上学期期中化学试题(已下线)第一次月考卷(长沙专用)-2023-2024学年九年级化学上册同步测试优选卷
更新时间:2022-11-19 17:27:37
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验,在相同温度下,比较两组实验产生O2的快慢
Ⅰ.将3.0g 10%过氧化氢溶液与1.0g MnO2均匀混合 ;Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
①为了Ⅰ与Ⅱ中对比x的值应为__________ .
②写出实验II发生反应的化学方程式_____________________________ 。
(2)探究影响双氧水分解速度的某种因素.实验数据记录如下(三组实验所用的MnO2质量相同)
①通过实验a与b对比可知,化学反应快慢与_______ 有关.
②通过对比实验__ 与实验________ 可知,反应物浓度大,反应速率快.
③除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是____ 。
(1)为探究催化剂的种类对双氧水分解速度的影响,甲设计以下对比实验,在相同温度下,比较两组实验产生O2的快慢
Ⅰ.将3.0g 10%过氧化氢溶液与1.0g MnO2均匀混合 ;Ⅱ.将x g10% H2O2溶液与1.0g CuO均匀混合
①为了Ⅰ与Ⅱ中对比x的值应为
②写出实验II发生反应的化学方程式
(2)探究影响双氧水分解速度的某种因素.实验数据记录如下(三组实验所用的MnO2质量相同)
| 实验 | 温度 | 药品 | 氧气体积/ml | 反应所需时间/s | |
| a | 20℃ | 5% H2O2 | 0 | ||
| b | 20℃ | 5% H2O2 | MnO2 | 125 | 20 |
| c | 40℃ | 5% H2O2 | MnO2 | 125 | 18 |
| d | 20℃ | 30% H2O2 | MnO2 | 125 | 5 |
①通过实验a与b对比可知,化学反应快慢与
②通过对比实验
③除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】化学反应条件的控制是实验的灵魂”.某探究小组发现若反应过快,产生的气体不易及时收集,为探究影响过氧化氢溶液分解快慢的因素,于是进行了如下探究:
【提出问题】过氧化氢溶液分解快慢与哪些因素有关呢?
【猜想与假设】猜想一:可能与过氧化氢的质量分数有关;
猜想二:可能与____ 有关;
猜想三:可能与是否用催化剂有关.
【设计并实验】该探究小组用不同质量分数的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧气体积和反应所需时间,记录数据如表.
【收集证据】要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是_____ (选填“实验序号”).由实验③和④对比可知,化学反应速率与温度的关系是:________ .
【解释与结论】
(1)通过探究,了解控制过氧化氢分解快慢的方法.请写出过氧化氢溶液在二氧化锰的催化作用下生成氧气的文字表达式为:_____________ .
(2)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量_________ .(填“减小”、“增大”或“不变”)
【提出问题】过氧化氢溶液分解快慢与哪些因素有关呢?
【猜想与假设】猜想一:可能与过氧化氢的质量分数有关;
猜想二:可能与
猜想三:可能与是否用催化剂有关.
【设计并实验】该探究小组用不同质量分数的过氧化氢溶液在不同温度时进行四次实验.记录所生成的氧气体积和反应所需时间,记录数据如表.
| 实验 序号 | 过氧化氢的 质量分数 | 过氧化氢溶液 体积(mL) | 温度 | 二氧化锰 的用量/g | 收集氧气 的体积/ml | 反应所需 的时间/s |
| ① | 5% | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15% | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30% | 5 | 35 | 2 | 49.21 | |
| ④ | 30% | 5 | 55 | 2 | 10.76 |
【收集证据】要比较不同质量分数的过氧化氢溶液对反应快慢的影响,应选择的实验编号组合是
【解释与结论】
(1)通过探究,了解控制过氧化氢分解快慢的方法.请写出过氧化氢溶液在二氧化锰的催化作用下生成氧气的文字表达式为:
(2)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,所产生氧气的总质量
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气。请你写出上述化学反应的文字表达式:_____
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验_____ 与实验④对比,证明猜想合理。
(2)实验所用的三种金属氧化物,催化效果最好的是_____ 。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
(1)由实验
(2)实验所用的三种金属氧化物,催化效果最好的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组对中和反应进行探究。
【问题提出】怎样证明NaOH溶液与稀盐酸能发生化学反应?

【查阅资料】可从三个方面设计实验证明:
一是设计实验证明反应物的消失;
二是设计实验证明有新物质生成;
三是设计实验证明化学反应有能量变化。
【实验探究】
(1)方案一:在NaOH溶液中滴入几滴酚酞后再滴加盐酸,当观察到___________ 时,即可确定二者发生了化学反应。其中和反应方程式为___________ 。但有同学认为顔色变化可能是盐酸与NaOH溶液反应,也可能是盐酸和酚酞反应了,请设计实验加以证明___________ 。
方案二:往NaOH溶液滴加盐酸的过程中,用pH计不断测量溶液的酸碱度,当pH<7即可确定二者发生了化学反应。实验测得其图像如图1。

(2)a点表示溶液中的溶质是___________ (写名称),将该溶液蒸发结晶后得到固体是___________ (填“纯净物”或“混合物”)
(3)滴加盐酸的过程中,强调“pH<7时”而不是“pH减小”作为判断二者发生化学反应的理由是___________ 。
方案三:NaOH溶液与稀盐酸反应放热,若混合前后温度有变化,则证明发生了化学反应。某同学将不同溶质质量分数的盐酸和NaOH溶液各10mL混合(注:所用溶液溶质质量分数很小,密度均相等),用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表)
(4)表中x约为___________ 。
(5)某同学在没有使用温度计的情况下,通过图2所示装置完成了实验(烧瓶内装氢氧化钠溶液,分液漏斗装盐酸,U形管装红墨水)。则该同学根据U形管装红墨水液面左低右高的现象判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是___________ 。
(6)如图3对上述过程采用微观模型加以认识,NaOH溶液和盐酸反应的微观实质是___________ 。
【问题提出】怎样证明NaOH溶液与稀盐酸能发生化学反应?

【查阅资料】可从三个方面设计实验证明:
一是设计实验证明反应物的消失;
二是设计实验证明有新物质生成;
三是设计实验证明化学反应有能量变化。
【实验探究】
(1)方案一:在NaOH溶液中滴入几滴酚酞后再滴加盐酸,当观察到
方案二:往NaOH溶液滴加盐酸的过程中,用pH计不断测量溶液的酸碱度,当pH<7即可确定二者发生了化学反应。实验测得其图像如图1。

(2)a点表示溶液中的溶质是
(3)滴加盐酸的过程中,强调“pH<7时”而不是“pH减小”作为判断二者发生化学反应的理由是
方案三:NaOH溶液与稀盐酸反应放热,若混合前后温度有变化,则证明发生了化学反应。某同学将不同溶质质量分数的盐酸和NaOH溶液各10mL混合(注:所用溶液溶质质量分数很小,密度均相等),用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表)
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
(5)某同学在没有使用温度计的情况下,通过图2所示装置完成了实验(烧瓶内装氢氧化钠溶液,分液漏斗装盐酸,U形管装红墨水)。则该同学根据U形管装红墨水液面左低右高的现象判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是
(6)如图3对上述过程采用微观模型加以认识,NaOH溶液和盐酸反应的微观实质是
您最近一年使用:0次
【推荐2】人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现:①过氧化氢酶是一种生物催化剂,在高温条件下容易失去活性;②FeCl3也能催化过氧化氢分解。为比较过氧化氢酶和FeCl3催化效率的高低,该同学在28℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:____ ;
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2;
②往1号试管内加入3mL浓度为5%的过氧化氢溶液,并滴入2滴适宜浓度的FeCl3溶液;往2号试管内____ ;
③观察并记录现象:2号试管内产生气泡比1号试管快。
(5)得出结论:在28℃环境下,____ 的催化效率高,猜想正确。
(6)在以上探究的基础上,该同学又完成了“探究温度对过氧化氢酶和FeCl3催化效率的影响”实验。实验结果如图所示:

结合以上实验结果分析,曲线乙表示____ 的催化效率随温度的变化,温度约为___ ℃时催化效果最好。
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2;
②往1号试管内加入3mL浓度为5%的过氧化氢溶液,并滴入2滴适宜浓度的FeCl3溶液;往2号试管内
③观察并记录现象:2号试管内产生气泡比1号试管快。
(5)得出结论:在28℃环境下,
(6)在以上探究的基础上,该同学又完成了“探究温度对过氧化氢酶和FeCl3催化效率的影响”实验。实验结果如图所示:

结合以上实验结果分析,曲线乙表示
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】ZB是常用的阻燃剂。已知:
Ⅰ.可用硼酸( )与ZnO、
)与ZnO、 合成ZB,ZB的组成会受温度等合成条件的影响。
合成ZB,ZB的组成会受温度等合成条件的影响。
Ⅱ.ZB受热,先释放出水;当温度高于350℃,生成ZnO和 固体;继续升温到400℃以上,
固体;继续升温到400℃以上, 熔化为玻璃态物质。
熔化为玻璃态物质。
(1)ZB能起阻燃作用的原因是______ (写一种)。
(2)为研究温度对合成的ZB组成的影响,研究小组在不同温度下制取ZB。实验如下:
x、y分别为______ 和______ 。
(3)为检测102℃时合成的ZB含水的质量分数,某同学利用如图装置(夹持仪器已略)进行实验。实验时,____________ 。
②需要称量获得的数据有:ZB样品的质量、______ 的质量。
(4)为评估102℃时合成的ZB的阻燃性能,做木材粉末灼烧残重实验:某温度下,灼烧质量相同的两份干燥的木材粉末(一份经ZB处理)30 min,测量残留固体质量;调整温度,重复实验,得到木材粉末灼烧后固体残留率(W)随温度变化关系如下图。 ;残留固体质量已扣除ZB的残余质量)
;残留固体质量已扣除ZB的残余质量)
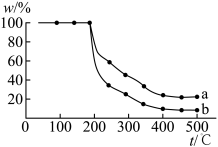
①低于200℃时,两份木材粉末质量均保持不变的原因是____________ 。
②图中曲线______ (填“a”或“b”)对应的木材粉末是经ZB处理的,判断的理由是____________ 。
Ⅰ.可用硼酸(
 )与ZnO、
)与ZnO、 合成ZB,ZB的组成会受温度等合成条件的影响。
合成ZB,ZB的组成会受温度等合成条件的影响。Ⅱ.ZB受热,先释放出水;当温度高于350℃,生成ZnO和
 固体;继续升温到400℃以上,
固体;继续升温到400℃以上, 熔化为玻璃态物质。
熔化为玻璃态物质。(1)ZB能起阻燃作用的原因是
(2)为研究温度对合成的ZB组成的影响,研究小组在不同温度下制取ZB。实验如下:
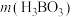 /g /g | 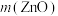 /g /g |  /mL /mL | t/℃ | |
| 实验 1 | 28 | 10 | 100 | 94 |
| 实验 2 | x | 10 | 100 | 98 |
| 实验 3 | 28 | y | 100 | 102 |
(3)为检测102℃时合成的ZB含水的质量分数,某同学利用如图装置(夹持仪器已略)进行实验。实验时,
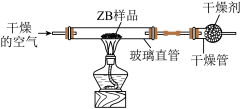
②需要称量获得的数据有:ZB样品的质量、
(4)为评估102℃时合成的ZB的阻燃性能,做木材粉末灼烧残重实验:某温度下,灼烧质量相同的两份干燥的木材粉末(一份经ZB处理)30 min,测量残留固体质量;调整温度,重复实验,得到木材粉末灼烧后固体残留率(W)随温度变化关系如下图。
 ;残留固体质量已扣除ZB的残余质量)
;残留固体质量已扣除ZB的残余质量)①低于200℃时,两份木材粉末质量均保持不变的原因是
②图中曲线
您最近一年使用:0次



