已知: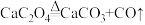 ,
,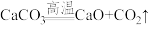 ,草酸钙【CaC2O4】比碳酸钙受热易分解。将12.8gCaC2O4固体加热一段时间后剩余7.8g固体。下列说法正确的是
,草酸钙【CaC2O4】比碳酸钙受热易分解。将12.8gCaC2O4固体加热一段时间后剩余7.8g固体。下列说法正确的是
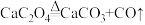 ,
,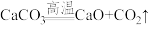 ,草酸钙【CaC2O4】比碳酸钙受热易分解。将12.8gCaC2O4固体加热一段时间后剩余7.8g固体。下列说法正确的是
,草酸钙【CaC2O4】比碳酸钙受热易分解。将12.8gCaC2O4固体加热一段时间后剩余7.8g固体。下列说法正确的是| A.剩余固体为纯净物 |
| B.剩余固体中含有钙元素的质量为2.0g |
| C.将剩余固体溶于过量的稀盐酸,产生4.4gCO2 |
| D.将加热产生的气体全部通入足量澄清石灰水中,生成5.0g固体 |
22-23九年级上·江苏镇江·阶段练习 查看更多[7]
江苏省镇江市江苏科技大学附属中学2022-2023学年九年级上学期12月月考化学试题2023分层教学_沪教版_第四单元_课题3 化学方程式的书写与应用 课时2_能力题(已审)(已下线)第13讲 化学方程式-【暑假轻松学】2023年新九年级暑假预习课(人教版)四川省泸州市泸县第一中学2022-2023学年九年级上学期第一次教学质量诊断(一诊)化学试题(已下线)课题3 利用化学方程式的简单计算 第2课时(分层练习)-2023-2024学年九年级化学上册同步精品课堂(人教版)(已下线)第3节 化学方程式的书写与应用(第2课时)(分层练习)-2023-2024学年九年级化学上册同步精品课堂(沪教版)2024年福建省永春市第一中学自主招生模拟化学试卷三
更新时间:2022-12-18 10:36:58
|
相似题推荐
选择题-单选题
|
困难
(0.15)
【推荐1】将铜粉和铁粉的混合物10g放入烧杯中,向烧杯中不断缓慢加入质量分数为20%的FeCl3溶液,测得烧杯中剩余固体的质量与加入FeCl3溶液质量的关系如图所示。下列选项正确的是
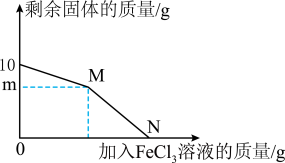
【小资料】铁和铜都能与FeCl3溶液发生反应,反应的化学方程式分别为:①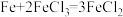 ;②
;②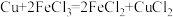

【小资料】铁和铜都能与FeCl3溶液发生反应,反应的化学方程式分别为:①
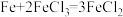 ;②
;②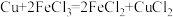
| A.Cu与FeCl3的反应属于置换反应 |
| B.混合物中铜粉的质量为(10-m)g |
| C.M点溶液中含有的阳离子为Fe3+、Fe2+、Cu2+ |
| D.若N点溶液中铁元素与铜元素质量比为115:28,则m为5.6 |
您最近一年使用:0次
选择题-单选题
|
困难
(0.15)
【推荐2】有NaHCO3与NaCl的混合物20.0g,加热一段时间,得剩余固体16.9g。向剩余固体中加入足量稀盐酸,并将该反应生成的气体通入澄清石灰水中,得到白色固体15.0g,下列说法正确的是( )
| A.NaHCO3加热生成CO2的质量为3.1g |
| B.剩余固体为Na2CO3和NaCl的混合物 |
| C.反应后,所得溶液中NaCl的质量为11.7g |
| D.原混合物中NaHCO3与NaCl的质量比为63:37 |
您最近一年使用:0次
选择题-单选题
|
困难
(0.15)
名校
解题方法
【推荐1】欲测定某碳酸钠样品中碳酸钠的含量,取 40g 该样品 (杂质不溶于水也不与酸反应) ,向其中加入 200g稀盐酸,恰好完全反应后,过滤,得到滤液 212.4g ,则该碳酸钠样品中含碳酸钠的质量分数是
| A.29.9% | B.53% | C.66.5% | D.80% |
您最近一年使用:0次
选择题-单选题
|
困难
(0.15)
解题方法
【推荐2】mgCaCO3煅烧一段时间,冷却,称得剩金固体的质量为17.8g,向剩金固体中加入足能的稀盐酸,充分反应,将所得溶液蒸干,得到22.2gCaCl2,下列说法不正确的是
| A.m=20 |
| B.剩余固体中CaCO3、CaO的质量比为75:14 |
| C.室温下,若将17.8g固体加96.3g水充分溶解后过滤,所得溶液浓度为3.7% |
| D.燃烧前后的固体分别与等浓度的稀盐酸反应,两者消耗稀盐酸的质量相等 |
您最近一年使用:0次
【推荐3】如图所示图1为一氧化碳还原氧化铜的实验,图2为碳还原氧化铜的实验,其中澄清石灰水足量,说法正确的有∶
①两个实验中都可观察到黑色固体变红,澄清石灰水变浑浊;
②两个实验都可以根石灰水不冒气泡的现象判断反应已经结束
③两个实验均应防止石灰水倒吸
④两个实验发生的反应中,C、CO都得到氧,发生还原反应;
⑤两个实验的相关反应中,C、Cu、O三种元素的化合价都发生改变;
⑥两个实验中固体减少的质量均为产生气体的质量
⑦两个实验中铜元素在固体中的质量分数逐渐变大;
⑧图1中,若取氧化铜样品质量为m,充分反应后,玻璃管内的固体质量减少了n,则样品中氧化铜的质量分数为 ×100%(杂质不参加反应),澄清石灰水增加的质量为
×100%(杂质不参加反应),澄清石灰水增加的质量为  。
。

①两个实验中都可观察到黑色固体变红,澄清石灰水变浑浊;
②两个实验都可以根石灰水不冒气泡的现象判断反应已经结束
③两个实验均应防止石灰水倒吸
④两个实验发生的反应中,C、CO都得到氧,发生还原反应;
⑤两个实验的相关反应中,C、Cu、O三种元素的化合价都发生改变;
⑥两个实验中固体减少的质量均为产生气体的质量
⑦两个实验中铜元素在固体中的质量分数逐渐变大;
⑧图1中,若取氧化铜样品质量为m,充分反应后,玻璃管内的固体质量减少了n,则样品中氧化铜的质量分数为
 ×100%(杂质不参加反应),澄清石灰水增加的质量为
×100%(杂质不参加反应),澄清石灰水增加的质量为  。
。| A.2个 | B.3 个 | C.4个 | D.5个 |
您最近一年使用:0次
选择题-单选题
|
困难
(0.15)
【推荐1】将22.2gCu2(OH)2CO3放在密闭容器内高温加热一段时间后,冷却,测得剩余固体的质量为15.2g。在剩余固体里加入100.0g稀硫酸恰好完全反应,过滤得红色金属。已知:Cu2O+H2SO4 =Cu+CuSO4+H2O,下列说法正确的是
| A.15.2g剩余固体是纯净物 | B.过程中生成CO2和H2O的质量和为7.0g |
| C.残留红色金属质量为12.8g | D.稀硫酸的溶质质量分数为14.7% |
您最近一年使用:0次
选择题-单选题
|
困难
(0.15)
【推荐2】已知:Mg(OH)2 MgO+H2O,CaCO3
MgO+H2O,CaCO3 CaO+CO2↑某水垢为Mg(OH)2、CaCO3的混合物。某兴趣小组称取25.8g此水垢,加热,剩余固体的质量随加热时间的变化如图所示。
CaO+CO2↑某水垢为Mg(OH)2、CaCO3的混合物。某兴趣小组称取25.8g此水垢,加热,剩余固体的质量随加热时间的变化如图所示。
 MgO+H2O,CaCO3
MgO+H2O,CaCO3 CaO+CO2↑某水垢为Mg(OH)2、CaCO3的混合物。某兴趣小组称取25.8g此水垢,加热,剩余固体的质量随加热时间的变化如图所示。
CaO+CO2↑某水垢为Mg(OH)2、CaCO3的混合物。某兴趣小组称取25.8g此水垢,加热,剩余固体的质量随加热时间的变化如图所示。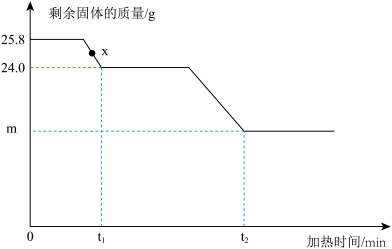
| A.x点对应固体成分为MgO、Mg(OH)2和CaCO3 |
| B.图中m=15.2 |
| C.水垢中Mg(OH)2与CaCO3的质量比为29:100 |
| D.若剩余固体中钙元素的质量分数为40%,则剩余固体的成分是MgO和CaCO3 |
您最近一年使用:0次

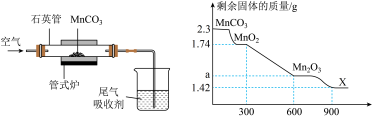
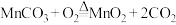 。已知焙烧过程中产生的气体不含锰元素,且石英管内固体的质量与管式炉温度的关系如图。下列说法正确的是
。已知焙烧过程中产生的气体不含锰元素,且石英管内固体的质量与管式炉温度的关系如图。下列说法正确的是