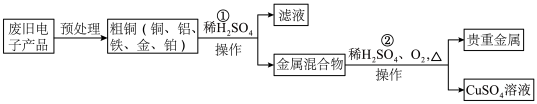
从某含铜、金(Au)和锌(Zn)废金属中回收Au并制备硫酸铜晶体(CuSO4·5H2O)的流程如下:(资料:铜的金属活动性比金强)
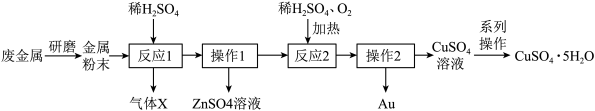
(1)将废旧金属研磨成粉末的目的是___________ 。
(2)X化学式为___________ 。
(3)操作:1和2中用到的玻璃仪器有:___________ 烧杯、玻璃棒等:
(4)反应2的化学方程式为:___________ 。

(1)将废旧金属研磨成粉末的目的是
(2)X化学式为
(3)操作:1和2中用到的玻璃仪器有:
(4)反应2的化学方程式为:
更新时间:2022-12-18 10:36:58
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】北京时间5月15日天问一号探测器成功着陆于火星乌托邦原南部预选着落区,我国首次火星探测任务着陆火星取得成功,这是我国航天事业发展的又一具有里程碑意义的进展。火星的橘红色外表是因为地表被赤铁矿覆盖,大气成分二氧化碳占96%。铁红(Fe2O3)是一种红棕色难溶于水的粉末,广泛应用于制造油漆、油墨、橡胶等。利用赤铁矿(主要成分Fe2O3)制备铁红的一种工艺如图:
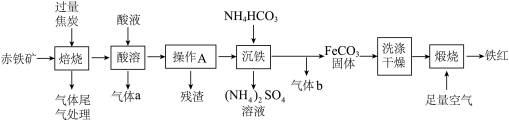
(1)“焙烧”过程中,铁元素的化合价___________ (填“升高”“降低”或“不变”)。
(2)“酸溶”过程中加入酸的名称是___________ ,气体a是___________ (填化学式)。
(3)“操作A”的名称是___________ ,需要用到的铁制仪器为___________ 。
(4)“沉铁”过程,产生的气体是___________ 。
(5)在流程中,可以回收利用的一种物质是___________ ,该物质主要使用在农业生产当中。
(6)以上流程中释放的二氧化碳,引起的气候变化问题是___________ ;中国承诺在2030年前实现“碳达峰”,2060年前实现“碳中和”的目标。抵消CO2的排放量路径一:可以通过植树造林、节能减排等形式,路径二:可以通过捕集、利用和封存CO2.如利用废气中的CO2与流程中的气体a在一定条件下制取甲醇(CH3OH)。根据质量守恒定律,写出CO2制取甲醇的化学方程式:___________ 。

(1)“焙烧”过程中,铁元素的化合价
(2)“酸溶”过程中加入酸的名称是
(3)“操作A”的名称是
(4)“沉铁”过程,产生的气体是
(5)在流程中,可以回收利用的一种物质是
(6)以上流程中释放的二氧化碳,引起的气候变化问题是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐2】根据题意完成化学反应方程式
(1)氢气在氧气中燃烧________
(2)铜和硝酸汞溶液反应________
(3)酒精在空气中完全燃烧________
(4)实验室用过氧化氢溶液和二氧化锰制取氧气________
(1)氢气在氧气中燃烧
(2)铜和硝酸汞溶液反应
(3)酒精在空气中完全燃烧
(4)实验室用过氧化氢溶液和二氧化锰制取氧气
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某样品是由铁粉和氧化铜粉末均匀混合而成,将该样品等质量分为两份,进行以下实验回收铜,若每一步都充分反应,得到的固体2是两种金属的混合物。
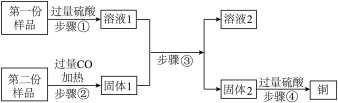
(1)步骤①中观察到的实验现象为_______ 。溶液1和溶液2中都含有的溶质是_______ (填物质的名称)。
(2)步骤②在下图所示的装置(夹持仪器已省略)中进行
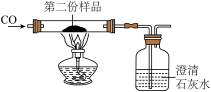
点燃酒精灯前,先要通一段时间CO,目的是_______ 。请写出硬质玻璃管中发生反应的化学方程式_______ 。用该装置做实验的不足之处是_______ 。
(3)根据上述实验流程,能得出样品中铁和氧化铜的物质的量大小有怎样的关系?____ 请说明理由。_______ 。

(1)步骤①中观察到的实验现象为
(2)步骤②在下图所示的装置(夹持仪器已省略)中进行

点燃酒精灯前,先要通一段时间CO,目的是
(3)根据上述实验流程,能得出样品中铁和氧化铜的物质的量大小有怎样的关系?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】取等质量、相同形状的铁片、镁片、锌片,分别与足量的等体积、等溶质质量分数的稀硫酸反应,用传感器测得反应温度随时间变化曲线如图所示。
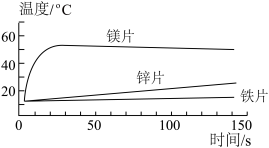
(1)根据曲线可以得到什么结论?_________
(2)完全反应后,三种溶液的质量由大到小的顺序是什么?(直接用加入到稀硫酸中的各金属表示)___________

(1)根据曲线可以得到什么结论?
(2)完全反应后,三种溶液的质量由大到小的顺序是什么?(直接用加入到稀硫酸中的各金属表示)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】Na2SO4是制造纸张、药品、染料稀释剂等的重要原料。某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图所示。
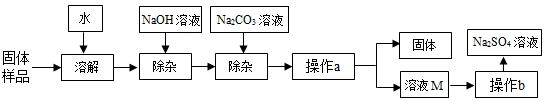
(1)操作a的名称是_____ 。
(2)加入NaOH溶液可除去的是_____ ,其反应的化学方程式为: _____ 。若添加的NaOH溶液和Na2CO3溶液过量,可加入适量 _____ (填“稀盐酸”或“稀硫酸”)除去。

(1)操作a的名称是
(2)加入NaOH溶液可除去的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】高纯碳酸钙广泛应用于精密电子陶瓷、医药等。实验室以优质石灰石(含少量SiO2)制备高纯碳酸钙工艺流程如图所示:
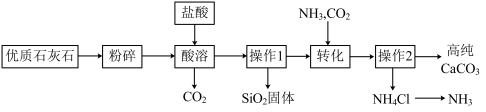
请回答下列问题:
(1)“操作1”的名称是_______ ;
(2)“粉碎”步骤中的目的是______ ;
(3)“转化”中有水参加反应,反应的化学方程式为_______ ;
(4)工艺流程中可以循环使用的物质是__________ 。

请回答下列问题:
(1)“操作1”的名称是
(2)“粉碎”步骤中的目的是
(3)“转化”中有水参加反应,反应的化学方程式为
(4)工艺流程中可以循环使用的物质是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】绿矾晶体是重要的化工原料。某工厂取硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)回收制取绿矾晶体(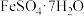 ),主要流程如图所示。根据所学知识填空。
),主要流程如图所示。根据所学知识填空。
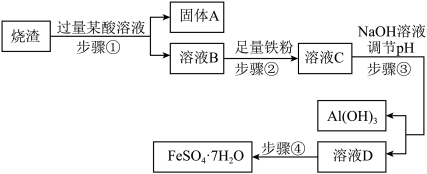
已知:
①铁与硫酸铁溶液能发生如下反应:Fe+Fe2(SO4)3=3FeSO4;
②Al3+在溶液pH为4.2时开始沉淀,在溶液pH为5.37时完全沉淀;Fe2+在溶液pH为8时开始沉淀。
(1)步骤①操作的名称是_______ 。
(2)步骤①中加入某酸溶液后,Fe2O3消失的化学方程式为______ 。
(3)步骤②加入铁粉后可观察到的现象是______ 。
(4)步骤③加入氢氧化钠调节溶液pH为5.37,发生的化学方程式为_______ 。
(5)步骤④结晶后的母液中还存在的金属离子有______ 。
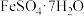 ),主要流程如图所示。根据所学知识填空。
),主要流程如图所示。根据所学知识填空。
已知:
①铁与硫酸铁溶液能发生如下反应:Fe+Fe2(SO4)3=3FeSO4;
②Al3+在溶液pH为4.2时开始沉淀,在溶液pH为5.37时完全沉淀;Fe2+在溶液pH为8时开始沉淀。
(1)步骤①操作的名称是
(2)步骤①中加入某酸溶液后,Fe2O3消失的化学方程式为
(3)步骤②加入铁粉后可观察到的现象是
(4)步骤③加入氢氧化钠调节溶液pH为5.37,发生的化学方程式为
(5)步骤④结晶后的母液中还存在的金属离子有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某品牌平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2等物质)。以此粉末为原料进行资源回收,其工艺流程如下:
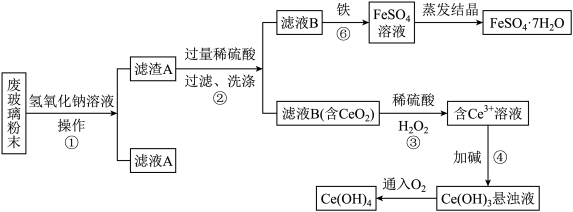
已知:2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3溶于水。
(1)第①步操作的名称是_______ ;
(2)第②步加入过量稀硫酸的目的是_______ ;
(3)滤液B中的阳离子有_______ (填离子符号);
(4)若第④步加的碱为NaOH,写出该反应的化学方程式_______ 。

已知:2NaOH+SiO2=Na2SiO3+H2O,Na2SiO3溶于水。
(1)第①步操作的名称是
(2)第②步加入过量稀硫酸的目的是
(3)滤液B中的阳离子有
(4)若第④步加的碱为NaOH,写出该反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋中蕴含丰富的资源。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是______ (填字母序号);
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是______ 。
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:
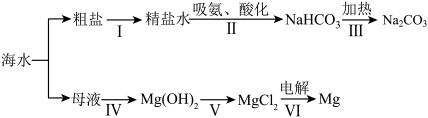
①1925年我国化学家______ 创立了联合制碱法,促进了世界制碱技术的发展。
②步骤I粗盐形成精盐水的过程中需去除泥沙。除去泥沙需经过溶解、过滤、蒸发三个步骤,均要用到玻璃棒,其中玻璃棒在蒸发中的作用是______ 。
③步骤I粗盐形成精盐水的过程中还要除去MgCl2、CaCl2、Na2SO4杂质。可依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,并在滤液中加入适量稀盐酸形成精盐水。加入稀盐酸的目的______ 。
④步骤Ⅱ中吸氨的目的是______ 。
⑤其第Ⅲ步反应的化学方程式为______ 。
⑥在工业生产中为了减低成本,步骤IV中所加试剂最好选择的是______ 。
⑦步骤第Ⅵ步反应的化学方程式为______ 。
(1)海水淡化
①海水淡化是解决淡水资源不足的重要方法,下列方法中,可以使海水淡化的是
A.过滤 B.吸附 C.沉降 D.蒸馏
②用化学方法区分蒸馏水和海水可采用的试剂是
(2)利用海水制取纯碱和金属镁的流程如图所示,试回答问题:

①1925年我国化学家
②步骤I粗盐形成精盐水的过程中需去除泥沙。除去泥沙需经过溶解、过滤、蒸发三个步骤,均要用到玻璃棒,其中玻璃棒在蒸发中的作用是
③步骤I粗盐形成精盐水的过程中还要除去MgCl2、CaCl2、Na2SO4杂质。可依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,并在滤液中加入适量稀盐酸形成精盐水。加入稀盐酸的目的
④步骤Ⅱ中吸氨的目的是
⑤其第Ⅲ步反应的化学方程式为
⑥在工业生产中为了减低成本,步骤IV中所加试剂最好选择的是
⑦步骤第Ⅵ步反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
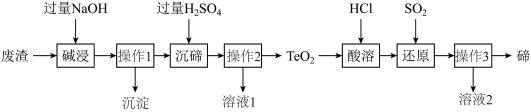
【推荐3】碲(Te)广泛用于彩色玻璃和陶瓷工艺。用某工业废渣((主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如图:_________________ (答一点即可)。
(2)TeO2与CO2化学性质相似,写出“碱浸”时发生反应的化学方程式______________ 。
(3)溶液1中一定有的金属阳离子是______ (填离子符号)。
(4)上述工艺流程中设计“废渣→……→TeO2”的目的是__________ 。
(5)“还原”时,在TeCl4溶液中通入SO2,该反应的化学方程式是TeCl4+2SO2+4H2O=Te+4HCl+2________ 。
(6)操作3要用蒸馏水对产品进行洗涤,具体做法:取少量最后一次洗涤后的滤出液于试管中,滴入AgNO3溶液或BaCl2溶液,观察到____________ 现象,则说明产品已洗涤干净。
(2)TeO2与CO2化学性质相似,写出“碱浸”时发生反应的化学方程式
(3)溶液1中一定有的金属阳离子是
(4)上述工艺流程中设计“废渣→……→TeO2”的目的是
(5)“还原”时,在TeCl4溶液中通入SO2,该反应的化学方程式是TeCl4+2SO2+4H2O=Te+4HCl+2
(6)操作3要用蒸馏水对产品进行洗涤,具体做法:取少量最后一次洗涤后的滤出液于试管中,滴入AgNO3溶液或BaCl2溶液,观察到
您最近一年使用:0次