人类的生活、生产离不开金属材料。大自然向人类提供了丰富的金属矿物资源,人类每年提取较大的金属依次是铁、铝、铜。
(1)在金属活动性顺序中铁没有铝活泼,但铝具有很好抗腐蚀性原因是_______ 。
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的_______ 共同作用的结果。
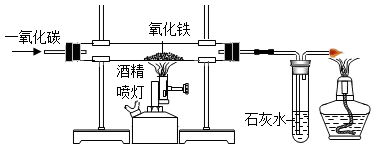
(3)下图是实验室模拟工业炼铁的装置图。该装置中一共发生的化学反应有_______ 个,酒精灯的作用是_______ ,炼铁的原理_______ (写化学方程式)。
(4)将锌粉放入含有Mg(NO3)2、Cu(NO3)2、AgNO3三种溶质的混合溶液中,充分反应后过滤。以下是对固体或滤液成分的探究。
①若向反应后所得固体上滴加盐酸有气泡产生,则该固体含有的金属有哪些?____
②猜想:滤液中的溶质为Mg(NO3)2、Zn(NO3)2、AgNO3,请分析猜想不合理原因是什么?____
(5)黄铜是铜锌合金,为测定某黄铜(铜锌合金)样品中铜的含量,取10g样品放在烧杯中,然后向其中逐渐加入稀硫酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀硫酸的质量为14g,反应后烧杯中物质总质量为23.8g。请计算样品中铜的质量分数。
(1)在金属活动性顺序中铁没有铝活泼,但铝具有很好抗腐蚀性原因是
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的
(3)下图是实验室模拟工业炼铁的装置图。该装置中一共发生的化学反应有

(4)将锌粉放入含有Mg(NO3)2、Cu(NO3)2、AgNO3三种溶质的混合溶液中,充分反应后过滤。以下是对固体或滤液成分的探究。
①若向反应后所得固体上滴加盐酸有气泡产生,则该固体含有的金属有哪些?
②猜想:滤液中的溶质为Mg(NO3)2、Zn(NO3)2、AgNO3,请分析猜想不合理原因是什么?
(5)黄铜是铜锌合金,为测定某黄铜(铜锌合金)样品中铜的含量,取10g样品放在烧杯中,然后向其中逐渐加入稀硫酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀硫酸的质量为14g,反应后烧杯中物质总质量为23.8g。请计算样品中铜的质量分数。
更新时间:2023-01-04 16:31:20
|
相似题推荐
综合应用题
|
较难
(0.4)
【推荐1】(1)我们已经学习了氢氧化钠的性质,知道这种固体要密封保存,原因有:①___________________ ;②________________ 。
兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
【对固体猜想】
猜想I:全部是NaOH;猜想II:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物
【实验和推断】
(2)为进一步确定成分,进行了以下探究:
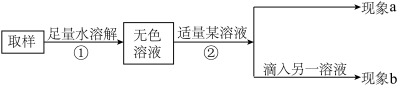
填写以下实验报告:
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想Ⅲ成立,理由是:
a、Na2CO3溶液呈碱性; b、__________________________________________________ 。
(3)兴趣小组按下图实验测定部分变质的NaOH固体中Na2CO3的质量分数。
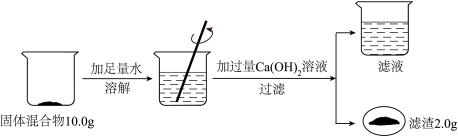
①根据题中信息______ (填“能”或“不能”)计算Ca(OH)2溶液的质量分数。
②通过计算,固体混合物中Na2CO3的质量分数是__________________ 。
兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
【对固体猜想】
猜想I:全部是NaOH;猜想II:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物
【实验和推断】
(2)为进一步确定成分,进行了以下探究:

填写以下实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步:用试管取约2mL该无色溶液,滴入适量澄清石灰水。 | 现象a:溶液变浑浊。 | 化学方程式:① |
| 第二步:静置,取上层清液于另一试管中,滴入无色酚酞溶液。 | 现象b:② | 证明含有NaOH,猜想Ⅲ成立,是NaOH和Na2CO3混合物 |
a、Na2CO3溶液呈碱性; b、
(3)兴趣小组按下图实验测定部分变质的NaOH固体中Na2CO3的质量分数。

①根据题中信息
②通过计算,固体混合物中Na2CO3的质量分数是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】化学是以实验为基础的科学,实验是进行科学探究的重要方式。
(1)下列实验仪器中,不能用来加热的是_________ ;
A.试管 B.量筒 C.烧杯 D.锥形瓶
(2)下图是教材中的探究实验。
A. 电解水
电解水
B. 硫在纯氧中燃烧
硫在纯氧中燃烧
C. 二氧化碳的性质
二氧化碳的性质
①A图装置可进行电解水实验,该实验得出的主要结论是_________ 。
②B图装置中集气瓶底部水的作用是_________ 。
③C图所示实验现象为_________ ,说明二氧化碳的化学性质为 _________ 。
(3)实验室用如图装置制取二氧化碳。
A. B.
B.
①A装置中长颈漏斗的下端管口必须插入液面以下,原因是_____
②请在B图方框中画出收集CO2的装置(只画出导管和集气瓶)_______
③写出实验室检验CO2的化学方程式____________
(4)选用上图装置制取二氧化碳,若用2.5g大理石与足量的稀盐酸完全反应(杂质不反应),可产生二氧化碳0.88g,则大理石中杂质的质量分数是_________ 。
(1)下列实验仪器中,不能用来加热的是
A.试管 B.量筒 C.烧杯 D.锥形瓶
(2)下图是教材中的探究实验。
A.
 电解水
电解水B.
 硫在纯氧中燃烧
硫在纯氧中燃烧C.
 二氧化碳的性质
二氧化碳的性质①A图装置可进行电解水实验,该实验得出的主要结论是
②B图装置中集气瓶底部水的作用是
③C图所示实验现象为
(3)实验室用如图装置制取二氧化碳。
A.
 B.
B.
①A装置中长颈漏斗的下端管口必须插入液面以下,原因是
②请在B图方框中画出收集CO2的装置(只画出导管和集气瓶)
③写出实验室检验CO2的化学方程式
(4)选用上图装置制取二氧化碳,若用2.5g大理石与足量的稀盐酸完全反应(杂质不反应),可产生二氧化碳0.88g,则大理石中杂质的质量分数是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】在实验室里,利用下图实验装置制取有关气体。

(1)图中仪器 a 的名称是______ 。
(2)实验室用 A 装置制备氧气,应选择的药品是______ 。(填数字序号)
①氯酸钾和二氧化锰 ②过氧化氢溶液和二氧化锰
(3)实验室用大理石和稀盐酸反应制取二氧化碳,反应的化学方程式是_______ 。B、C、D装置均可用作制取二氧化碳的发生装置,D装置与B、C装置相比,其突出优点是______ 。若选择 H 装置采用排空气法收集二氧化碳,验满的方法是__________ 。
(4)现取 25g 大理石样品于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如下图所示。

回答:①在实验时可将大理石适当粉碎,这样做的目的是_________ 。
②反应生成的 CO2的质量为多少_______ ?(请写出完整的计算过程)

(1)图中仪器 a 的名称是
(2)实验室用 A 装置制备氧气,应选择的药品是
①氯酸钾和二氧化锰 ②过氧化氢溶液和二氧化锰
(3)实验室用大理石和稀盐酸反应制取二氧化碳,反应的化学方程式是
(4)现取 25g 大理石样品于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如下图所示。

回答:①在实验时可将大理石适当粉碎,这样做的目的是
②反应生成的 CO2的质量为多少
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】为了除去二氧化碳中的少量氧气,并探究二氧化碳的性质,某同学设计了如图所示这套装置。
【拓展与思考】
(1)从步骤②开始E中液面开始下降的原因:_____
(2)有同学认为该装置需要添加尾气处理理装置,你认为是否需要并说明理由:_____ 。
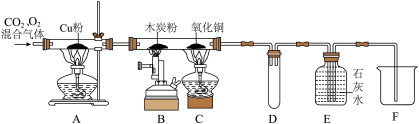 实验步骤 | 实验现象 | 现象分析 |
| ①点燃A处酒精灯,缓缓通入混合气体 | A中硬质玻璃管内固体 | A硬质玻璃管中铜粉的作用是 |
| ②点燃B中酒精喷灯 | B中木炭粉减少,E中石灰水混浊,液面下降。 | B硬质玻璃管中发生反应的化学方程式是 |
| ③点燃C中酒精灯 | C中现象 | C硬质玻璃管中发生反应的化 学方程式是 |
| ④停止通入混合气体,并用止水夹夹紧进气口,熄灭A,B,C处的酒精灯和酒精喷灯 | D装置的作用是 |
(1)从步骤②开始E中液面开始下降的原因:
(2)有同学认为该装置需要添加尾气处理理装置,你认为是否需要并说明理由:
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】金属是现代生活、工业生产以及科学研究中应用极为普遍的一类材料。

(1)台灯是在光线不足时常用照明用具。如右图所示台灯,铜质插头是利用了金属铜的_____ 性,灯管后面的反光片为铝箔。铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为 _____ 。
(2)在铁制品表面喷漆不仅美观,而且能防止铁制品表面与_____ 接触而生锈。
(3)将锌片投入到下列盐溶液后,能使溶液质量减轻的是_____ (填字母)。
A 氯化镁 B 氯化铜 C 硝酸汞 D 硝酸铝
(4)下列说法中不正确的是 _____ (填字母)。
A 生铁比钢的含碳量高
B 将钢针淬火后可以做钓鱼钩
C 焊锡的熔点比锡的熔点低
D 相同质量的钠、镁、铝三种金属,所含的原子最多的是钠
(5)将一定量的金属 (
( 的金属活动性比钠弱)加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤液中的溶质种类最多含
的金属活动性比钠弱)加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤液中的溶质种类最多含 _____ 种。
(6)将 铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成
铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成 二氧化碳,则这种铁的氧化物的化学式是
二氧化碳,则这种铁的氧化物的化学式是 _____ 。

(1)台灯是在光线不足时常用照明用具。如右图所示台灯,铜质插头是利用了金属铜的
(2)在铁制品表面喷漆不仅美观,而且能防止铁制品表面与
(3)将锌片投入到下列盐溶液后,能使溶液质量减轻的是
A 氯化镁 B 氯化铜 C 硝酸汞 D 硝酸铝
(4)下列说法中
A 生铁比钢的含碳量高
B 将钢针淬火后可以做钓鱼钩
C 焊锡的熔点比锡的熔点低
D 相同质量的钠、镁、铝三种金属,所含的原子最多的是钠
(5)将一定量的金属
 (
( 的金属活动性比钠弱)加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤液中的溶质种类最多含
的金属活动性比钠弱)加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤液中的溶质种类最多含 (6)将
 铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成
铁的某种氧化物在高温下与足量的一氧化碳充分反应,生成 二氧化碳,则这种铁的氧化物的化学式是
二氧化碳,则这种铁的氧化物的化学式是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】金属及其制品是现代生活中不可缺少的材料和工具。
(1)金属铝具有良好的防腐蚀性,原因是(用化学方程式表示)_______________________
(2)铁锅作炊具主要利用铁的_________ 性;使用铁锅炒菜、做饭有利于人体健康,主要是增加了膳食中的铁______ (选填“元素”、“原子”、“分子”),可以预防__________________ 病。
(3)对铁质零件进行“发蓝”处理后,其表面会形成致密氧化膜,从而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是可有效防止铁与_______________ 接触而生锈。
②发蓝过程的化学方程式如下:36Fe+4NaNO2+9NaNO3+26H2O=12X+13NaOH+13NH3 ↑,
式中X的化学式为________________ ,为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现_________ 色物质,由此可知“发蓝”处理效果不好,因为____________ (用化学方程式表示)。
(4)工业上常用CO还原赤铁矿冶炼金属铁,写出反应的化学方程式________________ 。
(5)火药起源于唐朝。为使烟火产生耀眼的白光,可在其火药中加入_____ (填一种金属名称)。
(6)现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用。2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有__________ (填序号)。
①硬度大 ②密度小 ③易导电 ④耐腐蚀
(7)导线不用纯铜制作而选用黄铜(铜锌合金),主要是因为黄铜__________________ 。
(8)①钛是一种贵重金属,具有熔点高、密度小、抗腐蚀性强(常温下不与酸、碱反应)、与人体相容性好等优良性能。据此判断,下列有关金属钛的用途不切实际的是____________ (填序号)。a.作保险丝 b.制造航天飞机 c.制造炊具 d.作人造骨头
②由钒钛磁铁矿提取金属钛的主要工艺过程如下:

写出最后两步反应的化学方程式:
Ⅰ.在高温下TiO2与C 混合后通入Cl2反应除生成TiCl4外还生成一种可燃性气体。
____________________________________________________
Ⅱ.TiCl4在高温下与足量Mg反应置换生成金属Ti。_______________________________________
上述生产过程中得到的金属钛中混有少量金属杂质,可加入______________ 除去(写名称)
(1)金属铝具有良好的防腐蚀性,原因是(用化学方程式表示)
(2)铁锅作炊具主要利用铁的
(3)对铁质零件进行“发蓝”处理后,其表面会形成致密氧化膜,从而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是可有效防止铁与
②发蓝过程的化学方程式如下:36Fe+4NaNO2+9NaNO3+26H2O=12X+13NaOH+13NH3 ↑,
式中X的化学式为
(4)工业上常用CO还原赤铁矿冶炼金属铁,写出反应的化学方程式
(5)火药起源于唐朝。为使烟火产生耀眼的白光,可在其火药中加入
(6)现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用。2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有
①硬度大 ②密度小 ③易导电 ④耐腐蚀
(7)导线不用纯铜制作而选用黄铜(铜锌合金),主要是因为黄铜
(8)①钛是一种贵重金属,具有熔点高、密度小、抗腐蚀性强(常温下不与酸、碱反应)、与人体相容性好等优良性能。据此判断,下列有关金属钛的用途不切实际的是
②由钒钛磁铁矿提取金属钛的主要工艺过程如下:

写出最后两步反应的化学方程式:
Ⅰ.在高温下TiO2与C 混合后通入Cl2反应除生成TiCl4外还生成一种可燃性气体。
Ⅱ.TiCl4在高温下与足量Mg反应置换生成金属Ti。
上述生产过程中得到的金属钛中混有少量金属杂质,可加入
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】金属材料在人类的生产和生活中有着广泛的应用。
(1)生铁和钢都是铁的合金,两者性能不同的原因是_________ 。
(2)我国航母螺旋桨由铜合金制造,与纯铜相比,铜合金的硬度更_____ (选填“大”或“小”)。
(3)某兴趣小组为探究铝、铜、银三种金属的活动性顺序,设计了如图所示的方案:

①I中发生反应的化学方程式为_________ 。
②通过以上实验,_________ (选填“能”或“不能”)得出三种金属的活动性的强弱。
(4)金属钛被称为铁和铝之后崛起的“第三种金属”,它是航海、化工、医疗上不可缺少的材料。工业上用钛铁矿(主要成分为FeTiO3)制备金属钛的一种工艺流程如图所示:

①操作I的名称是_________ 。
②向钛铁矿中加入的稀盐酸须过量,目的是_________ 。
③高温条件下,TiO2固体、单质碳和通入的C12发生反应的化学方程式为_________ 。
(5)高铁的高速运行离不开铁轨,建造铁轨所需要的钢铁通常用还原铁矿石的方法制得。工业上用赤铁矿石(主要成分为Fe2O3)与一氧化碳反应来炼铁。若制得5.6t铁,理论上需要含氧化铁80%的赤铁矿石多少吨?
(1)生铁和钢都是铁的合金,两者性能不同的原因是
(2)我国航母螺旋桨由铜合金制造,与纯铜相比,铜合金的硬度更
(3)某兴趣小组为探究铝、铜、银三种金属的活动性顺序,设计了如图所示的方案:

①I中发生反应的化学方程式为
②通过以上实验,
(4)金属钛被称为铁和铝之后崛起的“第三种金属”,它是航海、化工、医疗上不可缺少的材料。工业上用钛铁矿(主要成分为FeTiO3)制备金属钛的一种工艺流程如图所示:

①操作I的名称是
②向钛铁矿中加入的稀盐酸须过量,目的是
③高温条件下,TiO2固体、单质碳和通入的C12发生反应的化学方程式为
(5)高铁的高速运行离不开铁轨,建造铁轨所需要的钢铁通常用还原铁矿石的方法制得。工业上用赤铁矿石(主要成分为Fe2O3)与一氧化碳反应来炼铁。若制得5.6t铁,理论上需要含氧化铁80%的赤铁矿石多少吨?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是________ (填序号)。

(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行 的是________ 。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与__________ 和__________ 发生反应;用于铁栏杆外层防止其生锈的涂料中的“银粉”大多是金属________ 的粉末。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有________ ;滤液B中一定没有的金属离子是________ 。
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨________ 。?(结果精确到0.1 t)
(1)下列生活用品中,主要利用金属导热性的是

(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】金属材料在生产、生活中使用广泛。
(1)用生铁制成铁锅是利用了其良好的______ 性;生铁比纯铁硬度大,其原因是______ 。
(2)在Cu(NO3)2、AgNO3和Zn(NO3)2的混合溶液中加入一定量的镁粉,充分反应后过滤,可得到滤渣和滤液。
①写出反应过程中一定发生的化学反应方程式:______ 。
②反应后得到滤液质量一定小于原混合溶液的质量,请分析原因:______ 。
③若取6.5g反应后所得的滤渣,向其中加入足量的稀盐酸,得到0.2g氢气,则滤渣的组成可能是______ 。
A.银、铜、锌 B.银、铜、镁 C.银、铜、锌、镁
(3)利用如图装置进行模拟冶铁的实验,并检验该反应的气体产物。已知由A装置制取的一氧化碳气体中混有少量二氧化碳和水蒸气。

①要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接______ 、______ 接______ 、______ 接______ 、______ 接______ 、______ 接i。
②D装置在冷却过程中,应该如何防止其中的黑色粉末与空气接触而变为红色______ 。
(4)100t含Fe2O380%的赤铁矿石理论上能炼出含杂质4%的生铁的质量是多少?(保留一位小数)
(1)用生铁制成铁锅是利用了其良好的
(2)在Cu(NO3)2、AgNO3和Zn(NO3)2的混合溶液中加入一定量的镁粉,充分反应后过滤,可得到滤渣和滤液。
①写出反应过程中一定发生的化学反应方程式:
②反应后得到滤液质量一定小于原混合溶液的质量,请分析原因:
③若取6.5g反应后所得的滤渣,向其中加入足量的稀盐酸,得到0.2g氢气,则滤渣的组成可能是
A.银、铜、锌 B.银、铜、镁 C.银、铜、锌、镁
(3)利用如图装置进行模拟冶铁的实验,并检验该反应的气体产物。已知由A装置制取的一氧化碳气体中混有少量二氧化碳和水蒸气。

①要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接
②D装置在冷却过程中,应该如何防止其中的黑色粉末与空气接触而变为红色
(4)100t含Fe2O380%的赤铁矿石理论上能炼出含杂质4%的生铁的质量是多少?(保留一位小数)
您最近一年使用:0次
【推荐1】化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)某化学兴趣小组的同学利用如图所示的微型装置进行探究实验。已知:W形管的容积为300mL;红磷的着火点是240℃、白磷的着火点是40℃。

①向W形管中放入过量的红磷和白磷,塞好橡胶塞,关闭弹簧夹,然后将其放入80℃的热水中,观察到
红磷不燃烧而白磷燃烧。请写出白磷(用P表示)燃烧的化学方程式:_______ ;由此可说明燃烧需要的条件之一是_______ 。
②待实验①中白磷熄灭,装置冷却至室温后,打开弹簧夹,最终可观察到量筒中的水剩余约_______ mL。
(2)实验室可利用如图所示装置制取纯净、干燥的CO,然后用CO还原赤铁矿井测定赤铁矿中氧化铁的质量分数。已知:一氧化碳发生装置中的反应为

 ,赤铁矿中的杂质不参加反应。
,赤铁矿中的杂质不参加反应。

①B装置的硬质玻璃管中可观察到什么现象?____ 。
②要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接_______ 、_______ 接_______ 、_______ 接_______ 、_______ 接g。
③D装置中碱石灰的作用是什么?____ 。
④请设计实验,检验实验后C装置的溶液中溶质的成分____ 。(简要写出实验步骤、现象和结论)
⑤实验前称量赤铁矿的质量为10g,通入足量的一氧化碳完全反应后,D装置中盛有NaOH溶液的试剂瓶的总质量增加了6.6g,求该赤铁矿中氧化铁的质量分数____ 。
(1)某化学兴趣小组的同学利用如图所示的微型装置进行探究实验。已知:W形管的容积为300mL;红磷的着火点是240℃、白磷的着火点是40℃。

①向W形管中放入过量的红磷和白磷,塞好橡胶塞,关闭弹簧夹,然后将其放入80℃的热水中,观察到
红磷不燃烧而白磷燃烧。请写出白磷(用P表示)燃烧的化学方程式:
②待实验①中白磷熄灭,装置冷却至室温后,打开弹簧夹,最终可观察到量筒中的水剩余约
(2)实验室可利用如图所示装置制取纯净、干燥的CO,然后用CO还原赤铁矿井测定赤铁矿中氧化铁的质量分数。已知:一氧化碳发生装置中的反应为


 ,赤铁矿中的杂质不参加反应。
,赤铁矿中的杂质不参加反应。
①B装置的硬质玻璃管中可观察到什么现象?
②要达到实验目的,装置中导管接口从左到右的连接顺序为:一氧化碳发生装置接
③D装置中碱石灰的作用是什么?
④请设计实验,检验实验后C装置的溶液中溶质的成分
⑤实验前称量赤铁矿的质量为10g,通入足量的一氧化碳完全反应后,D装置中盛有NaOH溶液的试剂瓶的总质量增加了6.6g,求该赤铁矿中氧化铁的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】金属及合金有广泛的用途。
(1)铝的原子结构示意图为_______ 。下列有关铝的叙述正确的是_______ 。(填序号)
①铝元素在周期表中位于第三周期;②铝原子在化学反应中易得电子;③铝元素是地壳中含量最高的元素;④金属铝化学性质活泼却较耐腐蚀。
(2)要证明Cu、Zn、Ag三种金属的活动性顺序,除了金属单质外,还至少需要一种溶液,用该溶液进行实验时发生反应的化学方程式为_______ 。
(3)向硝酸镁和硝酸银的混合溶液中加入一定量锌粉和铜粉的混合物,充分反应后过滤,观察到滤液为无色,请回答:
①要进一步确认此时所得滤渣的成分,请设计实验方案____ 。
②请分析并解释滤液的质量与反应前溶液的质量相比如何变化_____ 。
(4)某化学小组用如图徽型装置进行模拟冶铁的实验。(已知甲处反应生成CO)

①乙处玻璃管中观察到的现象是_______ 。
②丁装置的作用是什么?____ 。
(5)若将10g赤铁矿样品用CO还原,充分反应后剩余固体的质量为7.6g,请利用化学方程式计算该赤铁矿样品中氧化铁的质量分数。(杂质不参加反应)
(1)铝的原子结构示意图为
①铝元素在周期表中位于第三周期;②铝原子在化学反应中易得电子;③铝元素是地壳中含量最高的元素;④金属铝化学性质活泼却较耐腐蚀。
(2)要证明Cu、Zn、Ag三种金属的活动性顺序,除了金属单质外,还至少需要一种溶液,用该溶液进行实验时发生反应的化学方程式为
(3)向硝酸镁和硝酸银的混合溶液中加入一定量锌粉和铜粉的混合物,充分反应后过滤,观察到滤液为无色,请回答:
①要进一步确认此时所得滤渣的成分,请设计实验方案
②请分析并解释滤液的质量与反应前溶液的质量相比如何变化
(4)某化学小组用如图徽型装置进行模拟冶铁的实验。(已知甲处反应生成CO)

①乙处玻璃管中观察到的现象是
②丁装置的作用是什么?
(5)若将10g赤铁矿样品用CO还原,充分反应后剩余固体的质量为7.6g,请利用化学方程式计算该赤铁矿样品中氧化铁的质量分数。(杂质不参加反应)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】金属材料在人类发展的历史长河中起着非常重要的作用。
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的______ (填“高”或“低”)。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:
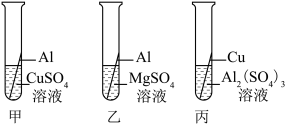
①实验甲中铝丝会出现的现象是______ ,该反应的化学方程式为______ 。
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是______ (填字母代号)。
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
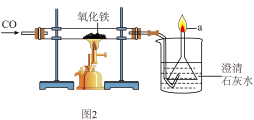
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式______ 。
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?______ 。
③a处尾气被点燃,写出反应的化学方程式______ 。
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?______ (反应方程式: )
)
(1)我国探月工程嫦娥五号探测器用到了铝合金材料。一般情况下,铝合金的强度和硬度比纯铝的
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序、某同学设计了如图1所示三个实验:


①实验甲中铝丝会出现的现象是
②另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是
A.乙、丙都可以省去B.乙、丙都不能省去
C.丙可以省去,乙不能省D.乙可以省去,丙不能省
(3)钢铁是使用最多的金属材料。某化学小组利用如图2所示装置模拟工业炼铁的实验。
①写出玻璃长管中发生反应的化学方程式
②检验CO还原Fe2O3反应的气体生成物的实验现象是什么?
③a处尾气被点燃,写出反应的化学方程式
(4)高铁的快速发展方便了人们的出行。工业上可利用铝粉和Fe2O3在高温下发生置换反应制得铁来焊接钢轨。用13.5kg铝粉可制取铁的质量是多少?
 )
)
您最近一年使用:0次



