过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末.在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:___________________________ ,发生的反应方程式是:__________________________ .
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为______________________________ ;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.
猜想3:_____________
方案3:
(1)区分水和过氧化氢的实验方法是:
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究.
提出问题:什么导致溶液先变红再褪色?
猜想与假设:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”.
实验与结论:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1﹣2滴酚酞试液,变红后, | 溶液依然为红色 |
讨论交流:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分.
猜想3:
方案3:
| 实验步骤 | 实验现象 | 实验结论 |
2012·安徽·中考模拟 查看更多[3]
更新时间:2016-11-28 11:40:45
|
相似题推荐
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐1】H2O2溶液俗称双氧水,在生活、生产和实验研究中均有广泛应用。现有一瓶已开启过一段时间的H2O2溶液,标签内容见图-1。

【配制溶液】配制浓度约为5%的过氧化氢溶液
(1)用这种溶质质量分数为30%的H2O2溶液,与H2O以1:5的体积比混合后,所得溶液的溶质质量分数为______ 。(结果精确到0.1%)
【测定浓度】H2O2溶液的浓度可以采用酸化的KMnO4溶液来标定,主要的反应方程式为: 。
。
(2)取20mL配得的H2O2溶液(密度近似为1.0g/mL)加入少量稀H2SO4,不断滴入一定浓度的KMnO4标准液(每1000mL溶液中含KMnO415.8g),边滴边振荡,直到溶液刚好呈浅红色为止(可认为KMnO4和H2O2恰好完全反应),测得该H2O2溶液的溶质质量分数为1.5%。计算:标定中滴入KMnO4标准液多少毫升?(结果精确到0.1mL)
(3)配得溶液的浓度和标定浓度直偏差的原因是______ 。
【拓展研究】
(4)以图-2所示装置进行实验I~IV,研究影响H2O2分解的因素,每组实验做3次,内容见表格。(室温为20℃,氧气浓度传感器初始读数为21%,水浴时间均为5分钟。)
①实验I试管中产生的气泡是溶解在水中的空气,说明气体的溶解性受________ 影响。
②实验I的目的是________ 。
③通过以上实验,得出加快H2O2分解的原因是________ 。
④实验V:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2%H2SO4溶液的试管中(见图-3)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。
(5)仅通过实验V,得出“Cu也能加快H2O2分解”的证据是否充足?请做出判断,并说明理由:______ 。

【配制溶液】配制浓度约为5%的过氧化氢溶液
(1)用这种溶质质量分数为30%的H2O2溶液,与H2O以1:5的体积比混合后,所得溶液的溶质质量分数为
【测定浓度】H2O2溶液的浓度可以采用酸化的KMnO4溶液来标定,主要的反应方程式为:
 。
。(2)取20mL配得的H2O2溶液(密度近似为1.0g/mL)加入少量稀H2SO4,不断滴入一定浓度的KMnO4标准液(每1000mL溶液中含KMnO415.8g),边滴边振荡,直到溶液刚好呈浅红色为止(可认为KMnO4和H2O2恰好完全反应),测得该H2O2溶液的溶质质量分数为1.5%。计算:标定中滴入KMnO4标准液多少毫升?(结果精确到0.1mL)
(3)配得溶液的浓度和标定浓度直偏差的原因是
【拓展研究】
(4)以图-2所示装置进行实验I~IV,研究影响H2O2分解的因素,每组实验做3次,内容见表格。(室温为20℃,氧气浓度传感器初始读数为21%,水浴时间均为5分钟。)
| 实验编号 | 具支试管内的试剂 | 水浴温度 | 试管内现象 | 传感器3次读数(%) |
| I | 10mL蒸馏水 1mL2%H2SO4溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 极少量气泡 | 21,21,21 | ||
| II | 10mL30%H2O2溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 极少量气泡 | 24,23,24 | ||
| III | 10mL30%H2O2溶液 1mL2%H2SO4溶液 | 20℃ | 无气泡 | 21,21,21 |
| 40℃ | 少量气泡 | 27,28,28 | ||
| IV | 10mL30%H2O2溶液 1mL2%CuSO4溶液 | 20℃ | 少量气泡 | 35,34,33 |
| 40℃ | 大量气泡 | 69,70,69 |
②实验I的目的是
③通过以上实验,得出加快H2O2分解的原因是
④实验V:将光亮的粗铜丝灼烧后,迅速伸入盛有10mL30%H2O2溶液和1mL2%H2SO4溶液的试管中(见图-3)。溶液中立即产生大量气泡,该气体能使带火星的木条复燃。
(5)仅通过实验V,得出“Cu也能加快H2O2分解”的证据是否充足?请做出判断,并说明理由:
您最近一年使用:0次
【推荐2】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0 g KClO3与1.0 g MnO2均匀混合加热。
Ⅱ.将x g KClO3与1.0 g CuO均匀混合加热。
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是____________________ ;Ⅱ中x的值应为 ________ 。
(2)乙探究了影响双氧水分解速度的某种因素。反应的化学方程式为________________ ,有关实验数据记录如下:
本实验中,测量O2质量应用了图的装置。根据实验装置实验所依据的原理是 _______________ 。

实验结论:在相同条件下,______ ,双氧水分解得越快。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0 g KClO3与1.0 g MnO2均匀混合加热。
Ⅱ.将x g KClO3与1.0 g CuO均匀混合加热。
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是
(2)乙探究了影响双氧水分解速度的某种因素。反应的化学方程式为
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2质量 | |
| Ⅰ | 50.0 g | 1% | 0.1 g | 0.013 mg |
| Ⅱ | 50.0 g | 2% | 0.1 g | 0.023 mg |
| Ⅲ | 50.0 g | 4% | 0.1 g | 0.044 mg |

实验结论:在相同条件下,
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】为探究过氧化氢的分解反应,同学们进行了以下实验。
【查阅资料】过氧化氢分解放热。当氧气低于一定浓度时,可燃物无法燃烧。
【进行实验】
初步探究:探究影响过氧化氢分解速率的因素
继续探究:重复烧杯1、3、4实验,并分别伸入带火星木条,如下图所示。
【结论与解释】
(1)写出烧杯1中反应的化学方程式_______ 。
(2)为证明MnO2和CuSO4能加快过氧化氢的分解速率,应增加的对比实验是_______ (填具体操作)。
(3)能证明过氧化氢溶液浓度影响其分解速率的实验是_____ (填烧杯的数字序号)。
(4)烧杯内出现大量白雾的原因是_______ 。
【反思与评价】
(5)烧杯4中木条熄灭的原因可能是_______ 。
(6)实验室若用双氧水制取氧气来完成木炭燃烧的实验,应选择的试剂是_______ (填字母序号)。
A5%过氧化氢溶液 B10%过氧化氢溶液
C20%过氧化氢溶液 D二氧化锰
【查阅资料】过氧化氢分解放热。当氧气低于一定浓度时,可燃物无法燃烧。
【进行实验】
初步探究:探究影响过氧化氢分解速率的因素
| 序号 | 烧杯1 | 烧杯2 | 烧杯3 | 烧杯4 |
| 实验操作 |  | 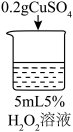 | 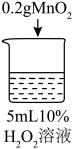 | 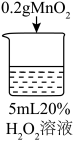 |
| 实验现象 | 立即冒大量气泡,烧杯内有 少量白雾出现。 | 5分钟后,有比较大量的气泡冒出。 | 立即冒大量气泡,烧杯内有白雾。 | 立即冒大量气泡,烧杯内有大量白雾。 |
继续探究:重复烧杯1、3、4实验,并分别伸入带火星木条,如下图所示。
| 实验方案 | 序号 | 实验现象 |
 | 烧杯1 | 木条复燃,燃烧很旺 |
| 烧杯3 | 木条复燃,之后火焰变微弱 | |
| 烧杯4 | 木条复燃,之后立即熄灭 |
【结论与解释】
(1)写出烧杯1中反应的化学方程式
(2)为证明MnO2和CuSO4能加快过氧化氢的分解速率,应增加的对比实验是
(3)能证明过氧化氢溶液浓度影响其分解速率的实验是
(4)烧杯内出现大量白雾的原因是
【反思与评价】
(5)烧杯4中木条熄灭的原因可能是
(6)实验室若用双氧水制取氧气来完成木炭燃烧的实验,应选择的试剂是
A5%过氧化氢溶液 B10%过氧化氢溶液
C20%过氧化氢溶液 D二氧化锰
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】(16分,每空2分)某化学兴趣小组做了如图所示的实验。

(1)实验中,观察到试管①③中共同的明显现象是_______ ,试管②中没有明显现象。试管①中发生反应的化学方程式为_______ 。
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】
(2)某化学兴趣小组取少量实验后试管②中的溶液,分别加入a、b两支试管中,向a试管中滴入酚酞溶液,观察到_______ 现象,证明了稀盐酸和氢氧化钠溶液一定发生了化学反应,为进一步探究试管②反应后溶液中溶质成分,可以向试管b中加入下列物质中的________ (填序号)。
①Zn ②AgNO3③Mg ④Na2CO3
(3)化学兴趣小组利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和测定结果如图所示:

①该实验中乙溶液是______ 。
②加入甲溶液6mL时,烧瓶中的溶液溶质成分为______ (填化学式)。
③根据该实验测定结果,判断发生化学反应的依据是_______ ,此反应的化学方程式为______ 。

(1)实验中,观察到试管①③中共同的明显现象是
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】
(2)某化学兴趣小组取少量实验后试管②中的溶液,分别加入a、b两支试管中,向a试管中滴入酚酞溶液,观察到
①Zn ②AgNO3③Mg ④Na2CO3
(3)化学兴趣小组利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和测定结果如图所示:

①该实验中乙溶液是
②加入甲溶液6mL时,烧瓶中的溶液溶质成分为
③根据该实验测定结果,判断发生化学反应的依据是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】食盐、苏打、食醋和生石灰是生活中常见的物质,某化学实验小组进行了如下实验探究。
【活动1】
(1)选用上述物质中的______ 做食品干燥剂(填化学式)。
【活动2】化学实验小组通过如图1所示的两组实验(其中A、B一组,C、D一组)鉴别氯化钠溶液和碳酸钠溶液:______ 。
【活动3】实验小组将试管B和试管D反应后的上层清液倒在烧杯中,发现有白色沉淀生成如图2,实验小组对烧杯内上层废液的成分产生了探究兴趣。
【提出问题】废液中含有哪些溶质?
【查阅资料】①常温下醋酸盐可溶于水
②
【猜想与假设】
(3)猜想①:CH3COONa、NaOH
猜想②:CH3COONa、NaOH、Na2CO3
猜想③:______
【进行实验】
(4)取废液少许于试管中,再向其中加入足量的氯化钡溶液,实验现象为______ 。
【得出结论】猜想②正确。
【反思交流】
(5)实验小组利用活动2结束后试管A中的废液除去某水垢(主要成分为氢氧化镁),其反应属于______ 反应(填基本反应类型)。
(6)实验小组想确定活动2试管C中是否发生了化学反应,现将活动2结束后试管C的溶液分成两等份。第一份溶液中加入过量的纯碱溶液得到a克沉淀,第二份溶液中加入过量硝酸镁溶液得到b克沉淀,当m= =
=______ (用b表示并化简)时说明进行活动2时C试管内没有发生化学反应。
【活动1】
(1)选用上述物质中的
【活动2】化学实验小组通过如图1所示的两组实验(其中A、B一组,C、D一组)鉴别氯化钠溶液和碳酸钠溶液:

【活动3】实验小组将试管B和试管D反应后的上层清液倒在烧杯中,发现有白色沉淀生成如图2,实验小组对烧杯内上层废液的成分产生了探究兴趣。
【提出问题】废液中含有哪些溶质?
【查阅资料】①常温下醋酸盐可溶于水
②

【猜想与假设】
(3)猜想①:CH3COONa、NaOH
猜想②:CH3COONa、NaOH、Na2CO3
猜想③:
【进行实验】
(4)取废液少许于试管中,再向其中加入足量的氯化钡溶液,实验现象为
【得出结论】猜想②正确。
【反思交流】
(5)实验小组利用活动2结束后试管A中的废液除去某水垢(主要成分为氢氧化镁),其反应属于
(6)实验小组想确定活动2试管C中是否发生了化学反应,现将活动2结束后试管C的溶液分成两等份。第一份溶液中加入过量的纯碱溶液得到a克沉淀,第二份溶液中加入过量硝酸镁溶液得到b克沉淀,当m=
 =
=
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】氮化镁( )是工业上常用的脱硫剂。通常条件下为黄绿色粉末,极易与水反应。
)是工业上常用的脱硫剂。通常条件下为黄绿色粉末,极易与水反应。
I、氮化镁的制备
下面是某同学利用空气中含有大量 的事实,用以下装置设计了一种制备氮化镁的方案(夹持装置略去):
的事实,用以下装置设计了一种制备氮化镁的方案(夹持装置略去):
【反应原理】 还原
还原 粉用于除去空气中的氧气。
粉用于除去空气中的氧气。

(1)按气流由左到右的方向,上述装置合理的连接顺序为______ (填接口字母)。
(2)装置D的作用为______ 。
II、定性分析产物
(3)
II、定量测定氮化镁纯度
为了测定 样品中
样品中 的纯度,某同学设计了如图装置(样品中的杂质不与水反应,夹持装置已略去)。
的纯度,某同学设计了如图装置(样品中的杂质不与水反应,夹持装置已略去)。
(4)装置C中球形干燥管的作用是______ 。
(5)组装好实验装置后,首先应检验装置气密性,再加入实验药品,打开K1,关闭K2,打开分液漏斗活塞,加入水,至不再产生气体。打开所有止水夹后通入氮气一段时间,测量装置______ (填“B”“C”或“D”)反应前后的质量变化为bg,通入氮气的目的是______ 。

(6) 的纯度是
的纯度是______ (用含a,b的式子表示)。
(7)若去掉装置D,则导致测定结果______ (填“偏高”“偏低”或“无影响”)。
 )是工业上常用的脱硫剂。通常条件下为黄绿色粉末,极易与水反应。
)是工业上常用的脱硫剂。通常条件下为黄绿色粉末,极易与水反应。I、氮化镁的制备
下面是某同学利用空气中含有大量
 的事实,用以下装置设计了一种制备氮化镁的方案(夹持装置略去):
的事实,用以下装置设计了一种制备氮化镁的方案(夹持装置略去):【反应原理】
 还原
还原 粉用于除去空气中的氧气。
粉用于除去空气中的氧气。
(1)按气流由左到右的方向,上述装置合理的连接顺序为
(2)装置D的作用为
II、定性分析产物
(3)
| 操作步骤 | 实验现象 | 解释原因 |
| 取少量产品于试管中,加足量蒸馏水溶解 | 试管底部有固体不溶物,有刺激性气味的气体产生 | 反应的化学方程式为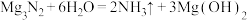 |
| 弃去上层清液,加入足量稀盐酸 | 观察到固体全部溶解,且有气泡冒出,放出热量 | 冒出的原因为 |
II、定量测定氮化镁纯度
为了测定
 样品中
样品中 的纯度,某同学设计了如图装置(样品中的杂质不与水反应,夹持装置已略去)。
的纯度,某同学设计了如图装置(样品中的杂质不与水反应,夹持装置已略去)。(4)装置C中球形干燥管的作用是
(5)组装好实验装置后,首先应检验装置气密性,再加入实验药品,打开K1,关闭K2,打开分液漏斗活塞,加入水,至不再产生气体。打开所有止水夹后通入氮气一段时间,测量装置

(6)
 的纯度是
的纯度是(7)若去掉装置D,则导致测定结果
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐1】实验台有一瓶标签受到腐蚀(如图所示)的无色溶液,实验员说该溶液只含一种溶质。化学兴趣小组的同学对该溶液作了如下探究:

【提出猜想】猜想Ⅰ:是NaOH溶液
猜想Ⅱ:是Na2CO3溶液
【进行实验】兴趣小组的同学取少量该溶液于试管中,按下图所示操作进行实验:

(已知白色沉淀M不溶于稀硝酸)
(1)通过操作①,兴趣小组的同学确认该溶液呈碱性,则X溶液是______________ 。
(2)综合分析操作②和操作③实验过程中产生的现象,你认为操作②发生反应的化学方程式是___________ ;Y溶液中的溶质是______________ (填化学式),由此你认为______________ (选填“猜想Ⅰ”或“猜想Ⅱ”)正确。
【反思交流】(3)大家认为该溶液还可能是_______________ 。
(4)操作③实验过程中,溶液由无色变为红色的原因是_____________ ,有关反应的化学方程式是_____________ 。

【提出猜想】猜想Ⅰ:是NaOH溶液
猜想Ⅱ:是Na2CO3溶液
【进行实验】兴趣小组的同学取少量该溶液于试管中,按下图所示操作进行实验:

(已知白色沉淀M不溶于稀硝酸)
(1)通过操作①,兴趣小组的同学确认该溶液呈碱性,则X溶液是
(2)综合分析操作②和操作③实验过程中产生的现象,你认为操作②发生反应的化学方程式是
【反思交流】(3)大家认为该溶液还可能是
(4)操作③实验过程中,溶液由无色变为红色的原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学小组围绕“碳酸钠的性质”展开探究,请你参与。
(1)【活动与探究】
实验Ⅳ反应的化学方程式为_____ 。
实验结束后,小组同学将四个实验所得澄清溶液倒入同一废液缸中,发现废液无色。
(2)【提出问题】
经讨论,小组同学一致认为废液中一定含有的离子是_____ (填离子符号)。废液中还含有哪些离子呢?(酚酞除外)
(3)【猜想与假设】猜想一:H+;猜想二:Ca2+;猜想三:_____ 。
(4)【实验探究】
甲同学取少许废液于试管中,向其中滴加紫色石蕊溶液,观察到紫色石蕊溶液变红,于是认为猜想一成立。大家一致认为甲同学的实验结论_____ (填“正确”或“不正确”)。同学们继续选取其它试剂进行实验,最终确定废液中含有三种阳离子、一种阴离子,从而得出实验结论。
(5)【反思与归纳】
通过上述探究可知:当溶液中可能存在的离子不止一种时,需要选择合适的试剂证明_____ ,才能得出实验结论。
(1)【活动与探究】
| 实验 | I | Ⅱ | Ⅲ | Ⅳ |
| 实验操作 | 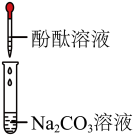 | 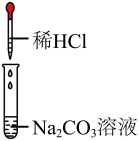 | 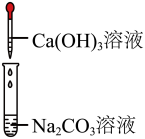 | 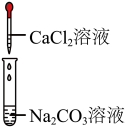 |
| 实验现象 | 溶液中出现气泡 | 溶液中产生白色沉淀 | 溶液中产生白色沉淀 |
实验结束后,小组同学将四个实验所得澄清溶液倒入同一废液缸中,发现废液无色。
(2)【提出问题】
经讨论,小组同学一致认为废液中一定含有的离子是
(3)【猜想与假设】猜想一:H+;猜想二:Ca2+;猜想三:
(4)【实验探究】
甲同学取少许废液于试管中,向其中滴加紫色石蕊溶液,观察到紫色石蕊溶液变红,于是认为猜想一成立。大家一致认为甲同学的实验结论
(5)【反思与归纳】
通过上述探究可知:当溶液中可能存在的离子不止一种时,需要选择合适的试剂证明
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】化学小组的同学用下图所示装置进行如下实验,实验前K1、K2、K3均为关闭状态。

(1)实验1中,可以观察到的现象是__________ 。
(2)实验2中,步骤①中所发生反应的化学方程式为____________________ 。
(3)实验2中,请解释步骤③产生气泡的原因为____________________ 。

| 步骤 内容 | 实验步骤 |
| 实验1 | B、C中分别盛有无色酚酞试液,打开K1,从分液漏斗中加入浓氨水,关闭K1,然后打开K2、K3。 |
| 实验2 | A中盛满CO2,B中盛有氢氧化钙溶液,C中盛有稀盐酸。 ①打开K1,从分液漏斗慢慢放入适量的氢氧化钠溶液,关闭K1。 ②一段时间后打开K2,观察到有A中有沉淀产生时,迅速关闭K2。 ③再打开K3,观察到A中有气泡产生。 |
(2)实验2中,步骤①中所发生反应的化学方程式为
(3)实验2中,请解释步骤③产生气泡的原因为
您最近一年使用:0次



