阅读下面科普短文。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,比如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维。使其易于被消化吸收。
你知道吗?深受人们喜爱的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入人胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中病菌进行了检测,结果如下表所示。
表﹣人体胃液pH情况分析
胃酸过多会对胃黏膜产生侵蚀作用,并使人感觉反酸或胃灼热。治疗胃酸过多的药主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应;二是抗酸药,能直接与胃酸反应。常服用的抗酸药的药物有碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。
胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。
依据文章内容,回答下列问题。
(1)关于文中提到的几种药物,属于氧化物的是_____ (填化学式)。
(2)燕麦中的铁粉遇到胃酸发生的化学反应,生成_____ 价铁离子。
(3)适量使用碳酸钙可以治疗胃酸过多,同时还可以补钙。反应方程式_____ 。
(4)胃溃疡患者适合服用的抗酸药是_____ (从文中挑选一)。
(5)下列说法正确的是 (填字母序号)。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,比如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维。使其易于被消化吸收。
你知道吗?深受人们喜爱的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入人胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中病菌进行了检测,结果如下表所示。
表﹣人体胃液pH情况分析
| 分组 | 胃液的pH | 受检患者人数 | 胃液中检出病菌的 人数及比列 |
| A | ≤2.0 | 7 | 0(0.0%) |
| B | 2.0﹣4.0 | 13 | 3(23.1%) |
| C | 4.0﹣6.0 | 26 | 17(65.4%) |
| D | >6.0 | 53 | 45(84.9%) |
胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。
依据文章内容,回答下列问题。
(1)关于文中提到的几种药物,属于氧化物的是
(2)燕麦中的铁粉遇到胃酸发生的化学反应,生成
(3)适量使用碳酸钙可以治疗胃酸过多,同时还可以补钙。反应方程式
(4)胃溃疡患者适合服用的抗酸药是
(5)下列说法正确的是 (填字母序号)。
| A.在使用抗酸药时不是越多越好 |
| B.胃液pH越小越有利于病菌生存 |
| C.氢氧化铝、氢氧化镁属于抗酸药物 |
更新时间:2023-01-31 14:07:28
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】A~H都是初中化学中的常见物质,它们之间的转化关系如图所示.A是天然气的主要成分,E是一种常见的食品干燥剂.请回答:
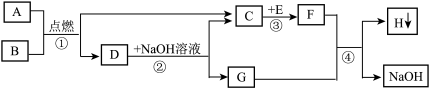
(1)物质C的化学式________ ; (2)反应③的基本反应类型是___________ ;
(3)写出有关反应的化学方程式:
②______________________ ,
④________________________ .

(1)物质C的化学式
(3)写出有关反应的化学方程式:
②
④
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】下图是汽车尾气转换器发生反应的微观过程。

图中单质是______ ,化学方程式为______ ,生成物的质量比为______ 。

图中单质是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~F分别是初中常见的六种物质,其中A是赤铁矿的主要成分,C是胃酸的主要成分,D是可溶性银盐,E为无色溶液,它们之间的关系如图所示。其中“—”表示相连的两种物质之间可以发生反应,用“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。

请回答下列问题:
(1)写出物质E的化学式_______ 。
(2)写出物质C的一种用途______ 。
(3)物质A转化为B的实验现象为_______ 。
(4)D与F的反应属于基本反应类型中的______ 。

请回答下列问题:
(1)写出物质E的化学式
(2)写出物质C的一种用途
(3)物质A转化为B的实验现象为
(4)D与F的反应属于基本反应类型中的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】物质是多样的,利用物质的转化创造物质,利用一定的方法分离物质,是化学重要研究思路和方法,请分析以下两个化学工艺流程回答问题。
(1)海水是宝贵的自然资源,从海水中提取食盐的主要过程如图。___________ 。
②蒸发池中,水蒸发属于___________ (填“物理”或“化学”)变化。
(2)硼(B)是制造火箭耐热合金的原料,它是一种既不与酸反应也不溶入水的物质。工业上用镁还原法生产硼,其主要工艺流程如图。___________ 。
②在还原炉中加热发生反应的化学方程式为___________ 其基本反应类型为___________ 。
③酸煮罐中,加入盐酸的目的是___________ 。(用化学方程式表示)
(1)海水是宝贵的自然资源,从海水中提取食盐的主要过程如图。

②蒸发池中,水蒸发属于
(2)硼(B)是制造火箭耐热合金的原料,它是一种既不与酸反应也不溶入水的物质。工业上用镁还原法生产硼,其主要工艺流程如图。

②在还原炉中加热发生反应的化学方程式为
③酸煮罐中,加入盐酸的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学与生活紧密相关,随着化学的发展,极大促进了人民大众的生活质量,请结合生活常识回答下列问题:
(1)有机高分子材料充斥于我们的生活,请用化学方法判定羊毛衫的真假______________________________ 。
(2)某化工厂有大量的酸性废水,为将其处理到中性之后再排放,请从下列物质中选择你认为的最适宜的物质_______ 。
a.氢氧化钠 b.氢氧化钙 c.氧化钙 d.碳酸钙
(1)有机高分子材料充斥于我们的生活,请用化学方法判定羊毛衫的真假
(2)某化工厂有大量的酸性废水,为将其处理到中性之后再排放,请从下列物质中选择你认为的最适宜的物质
a.氢氧化钠 b.氢氧化钙 c.氧化钙 d.碳酸钙
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A~G 是初中化学常见的不同物质,它们的相互转化关系如下图所示。其中 A、B、C、E 均为气体,G 是大理石的主要成分。请回答下列问题:

(1)物质 G 的化学式为______ 。
(2)物质 C 的一种用途为______ 。
(3)反应④的化学反应方程式是______ 。
(4)写出反应⑤的基本反应类型是:______ 反应。

(1)物质 G 的化学式为
(2)物质 C 的一种用途为
(3)反应④的化学反应方程式是
(4)写出反应⑤的基本反应类型是:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】A、B、C、D均含有同一种金属元素,它们的转化关系如图(部分物质和反应条件已略去)。

(1)若A是单质,D为蓝色不溶于水的固体。则D的化学式为__________ ,由C转化为A的化学方程式为____________ 。
(2)若A属于氧化物,C常用做建筑材料。则A转化为B的过程会__________ (填“放出”或“吸收”)热量,B的一种用途是____________ ,D转化为C的化学方程式为____________ 。

(1)若A是单质,D为蓝色不溶于水的固体。则D的化学式为
(2)若A属于氧化物,C常用做建筑材料。则A转化为B的过程会
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】孔雀石是冶炼金属铜的主要原料,其主要成分是 [可看成是
[可看成是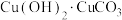 ],还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应)。下图为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。
],还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应)。下图为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。 与盐酸反应生成氧化铜、水和一种气体;
与盐酸反应生成氧化铜、水和一种气体;
b.铁能与氯化铁溶液反应,反应方程式为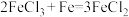 ;
;
c.氢氧化亚铁易被氧气氧化,反应方程式为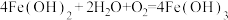 ;
;
回答下列问题:
(1)实验室在获取NaCl晶体的操作Y中,使用的仪器有:铁架台、蒸发皿、酒精灯、_________ ;
(2)盐酸与 反应的化学方程式:
反应的化学方程式:_______________________________ ;
(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有_________ 个;
(4)滤液Ⅱ的溶质的化学式为__________________ ;
(5)在洗涤、干燥获取铜粉时,判断洗涤完全的方法是______________________________ 。
 [可看成是
[可看成是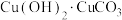 ],还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应)。下图为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。
],还含少量氧化铁和二氧化硅(不溶于水,也不与酸反应)。下图为“湿法炼铜”并制备其它副产品氯化钠和铁红(氧化铁)的工业流程。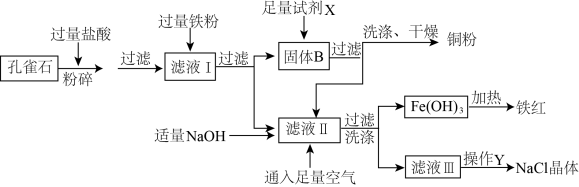
 与盐酸反应生成氧化铜、水和一种气体;
与盐酸反应生成氧化铜、水和一种气体;b.铁能与氯化铁溶液反应,反应方程式为
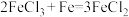 ;
;c.氢氧化亚铁易被氧气氧化,反应方程式为
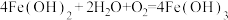 ;
;回答下列问题:
(1)实验室在获取NaCl晶体的操作Y中,使用的仪器有:铁架台、蒸发皿、酒精灯、
(2)盐酸与
 反应的化学方程式:
反应的化学方程式:(3)在滤液Ⅰ中加入过量铁粉,搅拌至充分反应,其中发生的置换反应有
(4)滤液Ⅱ的溶质的化学式为
(5)在洗涤、干燥获取铜粉时,判断洗涤完全的方法是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用该矿石制备氢氧化镁的流程图如图:

已知:
Ⅰ.SiO2不溶于水也不溶于盐酸。
Ⅱ.部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表:
(1)操作a的名称是______ ,沉淀B是______ 。
(2)图中步骤②控制pH的范围为______ ≤pH<9.l。
(3)溶液C中所含的溶质除HCl外,还有______ 。
(4)写出图中步骤②发生反应的一个化学方程式:______ 。

已知:
Ⅰ.SiO2不溶于水也不溶于盐酸。
Ⅱ.部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀pH | 3.2 | 6.7 | 11.1 |
(2)图中步骤②控制pH的范围为
(3)溶液C中所含的溶质除HCl外,还有
(4)写出图中步骤②发生反应的一个化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】小石同学为探究实验室制取二氧化碳后废液的成分,做了如下实验:
某废酸液中主要含有H2SO4和FeSO4,研究人员用CaCO3消耗部分酸,再加入廉价的电石渣(主要成分为CaO),经一系列操作可得到磁性铁(Fe3O4)。具体流程如图所示:

已知在90℃下向沉淀中加入氯酸钠时所发生的主要反应为: ;
;
(1)“沉铁”过程中发生复分解反应其化学方程式为_______ 。
(2)“沉铁”后,溶液的pH对磁性铁产率的影响如下表。
根据表格分析,欲获得较高的产率,最适宜的pH为__ ,pH较低时产率较低的主要原因是__ 。
(3)“水洗”时,为检验滤渣是否洗涤干净,可向最后一次洗涤液中滴加_______。
某废酸液中主要含有H2SO4和FeSO4,研究人员用CaCO3消耗部分酸,再加入廉价的电石渣(主要成分为CaO),经一系列操作可得到磁性铁(Fe3O4)。具体流程如图所示:

已知在90℃下向沉淀中加入氯酸钠时所发生的主要反应为:
 ;
;
(1)“沉铁”过程中发生复分解反应其化学方程式为
(2)“沉铁”后,溶液的pH对磁性铁产率的影响如下表。
| 溶液的pH | 6.0 | 6.5 | 7.0 | 7.5 | 8.0 | 9.0 |
| 产率(%) | 43.9 | 50.6 | 86.2 | 93.0 | 92.3 | 91.6 |
(3)“水洗”时,为检验滤渣是否洗涤干净,可向最后一次洗涤液中滴加_______。
| A.稀盐酸 | B.氢氧化钠溶液 | C.硝酸银溶液 |
您最近一年使用:0次

 。
。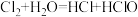 ,溴单质(Br2)和氯气性质高度相似,写出溴单质与水反应的化学方程式
,溴单质(Br2)和氯气性质高度相似,写出溴单质与水反应的化学方程式


