过氧乙酸消毒剂具有很强的杀菌能力。如图为某瓶过氧乙酸消毒剂的标签,该消毒剂由过氧乙酸、水和过氧化氢组成,其中某物质的质量分数是指该物质的质量与样品总质量之比的百分数。请完成下列问题:

(1)该瓶消毒剂属于______ (填“纯净物”或“混合物”)。
(2)过氧乙酸的相对分子质量为______ 。
(3)过氧化氢中氢、氧元素的质量比为______ (填最简整数比)。
(4)水中氢元素的质量分数为______ (结果保留到1%)。
(5)求这瓶过氧乙酸消毒剂中含碳元素的质量(写出计算过程,结果精确到0.1g)。

(1)该瓶消毒剂属于
(2)过氧乙酸的相对分子质量为
(3)过氧化氢中氢、氧元素的质量比为
(4)水中氢元素的质量分数为
(5)求这瓶过氧乙酸消毒剂中含碳元素的质量(写出计算过程,结果精确到0.1g)。
更新时间:2023-02-18 17:13:13
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】下图是某生理盐水的标签,根据标签给出的数据回答下列问题。

(1)生理盐水属于
(2)在氯化钠中,钠元素与氯元素的质量比为
(3)假设生理盐水的密度为1.0g/cm3,则这瓶生理盐水的溶质质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】“追梦”学小组通过查阅资料得知,工业上可利用二氧化碳生产尿素CO(NH2)2,既实现二氧化碳的转化,又获得化工产品。请回答以下问题:
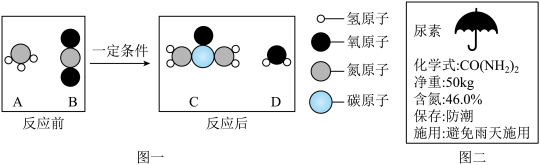
(1)工业上用氨气和二氧化碳在一定条件下反应生产尿素【CO(NH2)2】,该反应的微观示意图如图一、你能获得关于化学变化的信息有(各写一条):
宏观方面______ :微观方面______ 。
(2)计算尿素中碳元素和氮元素的质量比是______
(3)计算尿素中氮元素的质量分数______ (写出计算步骤,计算结果保留到0.1%)。
(4)尿素是一种常用的化肥,图二是尿素包装袋上的部分说明,请判断该化肥是______ (选填“纯净物”或“混合物”)。

(1)工业上用氨气和二氧化碳在一定条件下反应生产尿素【CO(NH2)2】,该反应的微观示意图如图一、你能获得关于化学变化的信息有(各写一条):
宏观方面
(2)计算尿素中碳元素和氮元素的质量比是
(3)计算尿素中氮元素的质量分数
(4)尿素是一种常用的化肥,图二是尿素包装袋上的部分说明,请判断该化肥是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】金属涂层光纤是在光纤的表面涂布Cu-Al合金层的光纤。为测定金属涂层光纤材料Cu-Al合金中铝的质量分数,进行如图所示实验(假设不含其他杂质):

(1)该金属涂层光纤材料是_______(填纯净物或混合物);
(2)往烧杯样品中加入100g稀硫酸并用玻璃棒搅拌,搅拌的目的是________,恰好完全反应后过滤,过滤时需要用到的玻璃仪器有 ;
(3)反应后所得溶液中溶质的质量分数(写出计算过程,结果精确至0.1%);
(4)硫酸铝是一种很有效的软体动物杀虫剂,用上述实验后所得溶液可配制溶质质量分数为16.3%的硫酸铝溶液 g。

(1)该金属涂层光纤材料是_______(填纯净物或混合物);
(2)往烧杯样品中加入100g稀硫酸并用玻璃棒搅拌,搅拌的目的是________,恰好完全反应后过滤,过滤时需要用到的玻璃仪器有 ;
(3)反应后所得溶液中溶质的质量分数(写出计算过程,结果精确至0.1%);
(4)硫酸铝是一种很有效的软体动物杀虫剂,用上述实验后所得溶液可配制溶质质量分数为16.3%的硫酸铝溶液 g。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】新装修的房间甲醛含量较高,是众多疾病的主要诱因。已知甲醛的化学式为CH2O,请回答下列问题(不需写计算过程):
(1)一个甲醛分子由 个原子构成
(2)甲醛中C、H、O三种元素的质量比为
(3)甲醛分子的相对分子质量为
(4)甲醛中碳元素的质量分数为
(1)一个甲醛分子由 个原子构成
(2)甲醛中C、H、O三种元素的质量比为
(3)甲醛分子的相对分子质量为
(4)甲醛中碳元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】“第八届国际侏罗纪大会”于2010年8月在我市射洪县龙凤峡召开。射洪龙凤峡以保存科研价值巨大的侏罗纪硅化木化石群著称,被国土资源部命名为“硅化木国家级地质公园”。硅化木也称木化石,是数亿年前的树木因种种原因被埋入地下后经过石化作用形成了木化石。因为所含的二氧化硅(SiO2)成分多,所以常常称为硅化木。计算(不要求写出计算过程):
(1)二氧化硅的相对分子质量_____ ;
(2)二氧化硅中硅、氧元素质量比为_____ 。
(1)二氧化硅的相对分子质量
(2)二氧化硅中硅、氧元素质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】阿司匹林可以缓解轻度或中度疼痛,化学式为C9H8O4,完成下列问题:
(1)阿司匹林由_____种元素组成,其中C、H、O元素原子个数比为_____;
(2)阿司匹林的摩尔质量为_____;
(3)阿司匹林中氧元素的质量分数为_____(列式计算,精确到0.1%)。
(4)0.25mol C9H8O4分子中约含有_____个氧原子(用科学记数法表示)。
(5)0.5mol C9H8O4的氢原子与_____g水中的氢原子个数相同。
(1)阿司匹林由_____种元素组成,其中C、H、O元素原子个数比为_____;
(2)阿司匹林的摩尔质量为_____;
(3)阿司匹林中氧元素的质量分数为_____(列式计算,精确到0.1%)。
(4)0.25mol C9H8O4分子中约含有_____个氧原子(用科学记数法表示)。
(5)0.5mol C9H8O4的氢原子与_____g水中的氢原子个数相同。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】钙是维持维持人体正常功能所必需的元素,有时需要服用补钙剂满足人体需求。如图分别为两种补钙剂说明书的一部分。

请根据提示中的信息回答下列问题:
(1)葡萄糖酸钙(C12H22O14Ca)的化学式量是_________;
(2)碳酸钙(化学式为CaCO3)中钙元素的质量分数为______;
(3)每片金钙尔奇中含碳酸钙的质量为________mg;
(4)按照金钙尔奇说明书每日的补钙量,若改服用葡萄糖酸钙片,一日3次,一次应服用几片?___________。

请根据提示中的信息回答下列问题:
(1)葡萄糖酸钙(C12H22O14Ca)的化学式量是_________;
(2)碳酸钙(化学式为CaCO3)中钙元素的质量分数为______;
(3)每片金钙尔奇中含碳酸钙的质量为________mg;
(4)按照金钙尔奇说明书每日的补钙量,若改服用葡萄糖酸钙片,一日3次,一次应服用几片?___________。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】尿素[化学式CO(NH2)2]是一种重要的氮肥,在土壤中不残留有害物质,长期施用没有不良影响。硝铵(化学式NH4NO3)也是一种常用的氮肥。
(1)尿素分子中碳、氢、氧、氮的原子个数比为_____________
(2)尿素的含氮量_____________硝铵的含氮量;(填“>”“<”或“=”)
(3)计算多少质量的硝铵中含有30g氮元素__________(算结果精确到0.1)。
(4)计算多少质量的尿素与80g硝铵中的含氮量相当__________?
(1)尿素分子中碳、氢、氧、氮的原子个数比为_____________
(2)尿素的含氮量_____________硝铵的含氮量;(填“>”“<”或“=”)
(3)计算多少质量的硝铵中含有30g氮元素__________(算结果精确到0.1)。
(4)计算多少质量的尿素与80g硝铵中的含氮量相当__________?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某钙片的标签如下,且知此钙片成分中只有碳酸钙(CaCO3)含有钙元素。
(1)钙片标签含钙量标明每片含钙0.75g,这里的“钙”是指______(填字母)。
(2)碳酸钙的相对分子质量为______ 。
(3)其中Ca、C、O元素的原子个数比是______ ;Ca、C、O元素质量比为______ (填最简整数比)。
(4)通过计算说明此标签中的含钙量是否合理?
(5)如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片。请计算每天他需补充碳酸钙多少克?
执行标准:GH1413—00每瓶50片,净重40g 主要成分:碳酸钙含钙量:每片含钙0.75g(中外合资xx公司出品 |
| A.分子 | B.原子 | C.元素 | D.离子 |
(3)其中Ca、C、O元素的原子个数比是
(4)通过计算说明此标签中的含钙量是否合理?
(5)如果一个青少年每天需补钙0.8克,其中0.6克来自于牛奶,其余服用钙片。请计算每天他需补充碳酸钙多少克?
您最近一年使用:0次




