乙炔是重要的有机工业原材料,常温下为气态物质,下图是化工厂生产乙炔的工艺流程简图。(图中1370K,2100-2500K表示热力学温度,是相关反应的条件)请读图回答:
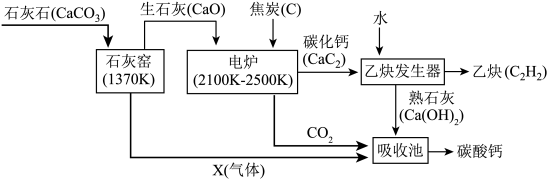
(1)写出上图X气体的名称:________ 。
(2)根据上图信息,写出电炉内发生的反应:_________ 。(化学方程式)
(3)根据上图信息,写出乙炔发生器内发生的反应:_________ 。(化学方程式)
(4)常温常压下,乙烯(C2H4)是一种无色,有苹果香味的气体:乙烯不仅是重要的工业基础原材料,也是常见的水果催熟剂。工业上可以用乙炔在一定条件下与氢气反应合成乙烯,请写出该变化的反应方程式:_______ 。
(5)写出本工艺流程循环使用的物质:_________ 。(化学式)

(1)写出上图X气体的名称:
(2)根据上图信息,写出电炉内发生的反应:
(3)根据上图信息,写出乙炔发生器内发生的反应:
(4)常温常压下,乙烯(C2H4)是一种无色,有苹果香味的气体:乙烯不仅是重要的工业基础原材料,也是常见的水果催熟剂。工业上可以用乙炔在一定条件下与氢气反应合成乙烯,请写出该变化的反应方程式:
(5)写出本工艺流程循环使用的物质:
2023·四川德阳·一模 查看更多[3]
(已下线)非选择专练12 工业流程(25题)-2023年中考化学总复习高频考点必刷题(苏州专用)四川省德阳市中江县2022-2023学年九年级上学期期末化学试题2023年四川省德阳市中江县中考一模化学试题
更新时间:2023-02-23 20:55:56
|
相似题推荐
【推荐1】利用“三角模型”来构建物质间的转化关系,如下图所示(“→”表示能一步实现的物质转化方向,部分反应物、生成物及反应条件均已略去)。
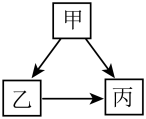
Ⅰ.从元素组成的角度构建
(1)甲、乙、丙均含碳元素,丙为 ,甲、乙均为盐,则甲转化为丙的化学方程式为
,甲、乙均为盐,则甲转化为丙的化学方程式为______ 。
(2)甲、乙、丙均含钠元素,丙为碱,则乙为______ 。
Ⅱ.从物质类别的角度构建
(3)甲、乙、丙均为金属单质,则三者的金属活动性由强到弱的顺序为______ ,图中有关反应的基本类型为______ 。
(4)甲、乙、丙均为氧化物,若甲为氧化铁,固态乙俗称干冰,写出甲→丙的反应中可能观察到的实验现象:______ 。甲→乙的化学方程式:______ 。
(5)甲、乙、丙均为酸,若丙为硝酸,则乙为______ ,甲转化为丙的化学方程式为______ 。
(6)下列“三角模型”正确的是______ (填序号)。写出“盐三角”中转化①涉及的化学方程式:______ 。
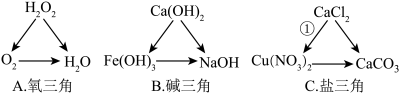

Ⅰ.从元素组成的角度构建
(1)甲、乙、丙均含碳元素,丙为
 ,甲、乙均为盐,则甲转化为丙的化学方程式为
,甲、乙均为盐,则甲转化为丙的化学方程式为(2)甲、乙、丙均含钠元素,丙为碱,则乙为
Ⅱ.从物质类别的角度构建
(3)甲、乙、丙均为金属单质,则三者的金属活动性由强到弱的顺序为
(4)甲、乙、丙均为氧化物,若甲为氧化铁,固态乙俗称干冰,写出甲→丙的反应中可能观察到的实验现象:
(5)甲、乙、丙均为酸,若丙为硝酸,则乙为
(6)下列“三角模型”正确的是

您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】已知A为黑色粉末,B为无色气体且和C的组成元素相同,D为红色固体。A、B、C、D、E五种物质之间的转化关系如下图所示。请回答:

(1)B的化学式为______ 。
(2)写出E的一种用途______ 。
(3)A与B反应的现象是______ 。
(4)反应②的化学方程式为______ 。

(1)B的化学式为
(2)写出E的一种用途
(3)A与B反应的现象是
(4)反应②的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】多角度认识物质,能帮助我们更全面了解物质世界。以氧气和二氧化碳为例,回答下列问
(1)认识物质的性质。
如图所示,将高低两个燃着的蜡烛放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到的实验现象是______ ;该实验说明CO2具有的性质是______ 。

(2)辩证地认识物质。
功过相对论。以二氧化碳的“功”、“过”事实分析。“功”:为工业生产和植物的光合作用提供丰富的原料;“过”:使全球气候变暖导致海平面上升等。植物光合作用的化学方程式为:6CO2+6H2O 6O2+X,则X的化学式是
6O2+X,则X的化学式是_____________ ;为了降低大气中二氧化碳含量过多所导致的危害,需要将二氧化碳吸收并加以利用,利用二氧化碳的成功范例是:在高温、高压下,以二氧化碳和氨气(NH3)为原料合成尿素[CO(NH2)2],同时有水生成,该反应的化学方程式是_________ 。
(1)认识物质的性质。
如图所示,将高低两个燃着的蜡烛放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到的实验现象是

(2)辩证地认识物质。
功过相对论。以二氧化碳的“功”、“过”事实分析。“功”:为工业生产和植物的光合作用提供丰富的原料;“过”:使全球气候变暖导致海平面上升等。植物光合作用的化学方程式为:6CO2+6H2O
 6O2+X,则X的化学式是
6O2+X,则X的化学式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】生产、生活中蕴含着丰富的化学知识。
(1)开水壶用久后,水壶内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2],可利用厨房内常用的一种调味品______ 来清除。
(2)我们中学生在生活中如何减少“白色污染”,请回答一点:______ 。
(3)用碳素墨水书写的文件、档案年深日久不褪色的原因是______ 。
(1)开水壶用久后,水壶内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2],可利用厨房内常用的一种调味品
(2)我们中学生在生活中如何减少“白色污染”,请回答一点:
(3)用碳素墨水书写的文件、档案年深日久不褪色的原因是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】A一H是初中化学常见的物质,其中A为发酵粉的主要成分之一,B是常用调味品,E、F的俗称分别为熟石灰、纯碱。它们之间的相互转化关系如图:

(1)写出构成物质B的粒子符号_____ 。
(2)在物质的分类中,A属于_____ (填“酸”、“碱”、“盐”)。
(3)图中反应②的化学方程式为_____ 。
(4)图中反应④的化学方程式为_____ 。

(1)写出构成物质B的粒子符号
(2)在物质的分类中,A属于
(3)图中反应②的化学方程式为
(4)图中反应④的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】我国已探明的页岩气储量31.6万亿立方米,储量世界第一、页岩气中含有CH4、CO2、H2S等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的CO2和H2S。
Ⅰ.CO2的处理:
(1)CO2和CH4一定条件下重整可制合成气(主要成分为CO、H2),请写出其发生反应的化学方程式:_______ 。
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2转化率随温度的变化如图2所示。

①结合图2,260°C时生成主要产物所发生反应的化学方程式为_______ 。
②温度高于320°C,CO2的转化率下降的原因是_______ 。
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生反应如图3。
(3)Fe2O3脱硫剂的脱硫和再生过程可以描述为_______ 。
(4)400°C条件下,氧气浓度较大时,氧气会将部分FeS氧化成 或
或 ,出现脱硫剂再生时质量
,出现脱硫剂再生时质量_______ (填“增大”或“减小”),且所得再生脱硫剂脱硫效果差,因此脱硫剂再生时需控制_______ 。
(5)脱硫剂再生时可以用水汽代替O2.700°C条件下用水汽代替O2再生时,生成 、
、 和
和 ,
, 也可作脱硫剂 写出水汽作用条件下脱硫剂再生反应的化学方程式:
也可作脱硫剂 写出水汽作用条件下脱硫剂再生反应的化学方程式:_______ 。
Ⅰ.CO2的处理:
(1)CO2和CH4一定条件下重整可制合成气(主要成分为CO、H2),请写出其发生反应的化学方程式:
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2转化率随温度的变化如图2所示。

①结合图2,260°C时生成主要产物所发生反应的化学方程式为
②温度高于320°C,CO2的转化率下降的原因是
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生反应如图3。
(3)Fe2O3脱硫剂的脱硫和再生过程可以描述为
(4)400°C条件下,氧气浓度较大时,氧气会将部分FeS氧化成
 或
或 ,出现脱硫剂再生时质量
,出现脱硫剂再生时质量(5)脱硫剂再生时可以用水汽代替O2.700°C条件下用水汽代替O2再生时,生成
 、
、 和
和 ,
, 也可作脱硫剂 写出水汽作用条件下脱硫剂再生反应的化学方程式:
也可作脱硫剂 写出水汽作用条件下脱硫剂再生反应的化学方程式:
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下列短文,回答相关问题。
氢能的生产与储存
氢能作为21世纪人类可持续发展的清洁可再生能源,更是实现“碳中和”和“碳达峰”的最有效途径之一。
一、氢气的生产
目前,常见的氢气制备方法除了电解水制氢法以外,还有如下几种方法:
①光催化制氢。如在二氧化钛微粒催化下利用光能分解水得到氢气和氧气。
②生物质发酵制氢。利用厌氧菌发酵水解淀粉和纤维素得到葡萄糖,在酶的作用下进一步转化为氢气。
③利用化石能源制氢。常用水蒸气改质法和部分氧化法。
水蒸气改质法是利用水蒸气和碳氢化合物反应制造氢气。
部分氧化法是使碳氢化合物与氧气催化反应生成氢气。例如,甲烷部分氧化法的制氢工艺如下所示。
目前的储氢方法主要是高压气态存储和低温液态储氢,两种储氢方法存在一定的安全隐患。因此,目前人们在重点研究固态储氢。Mg-Y-Ni储氢合金是我国科学家研究的一种新型储氢材料。其吸收和释放氢气的效率如下图所示。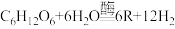 ,R的化学式是
,R的化学式是______ 。
(2)部分氧化法中,CO转化时与高温水蒸气反应的化学方程式是______ 。去除二氧化碳时采用加压、降温的方法得到气态H2和液态CO2。原理是利用CO2与H2的______ 不同。
(3)甲、乙、丙、丁四种材料中储氢性能最好的是______ ,原因是______ 。
氢能的生产与储存
氢能作为21世纪人类可持续发展的清洁可再生能源,更是实现“碳中和”和“碳达峰”的最有效途径之一。
一、氢气的生产
目前,常见的氢气制备方法除了电解水制氢法以外,还有如下几种方法:
①光催化制氢。如在二氧化钛微粒催化下利用光能分解水得到氢气和氧气。
②生物质发酵制氢。利用厌氧菌发酵水解淀粉和纤维素得到葡萄糖,在酶的作用下进一步转化为氢气。
③利用化石能源制氢。常用水蒸气改质法和部分氧化法。
水蒸气改质法是利用水蒸气和碳氢化合物反应制造氢气。
部分氧化法是使碳氢化合物与氧气催化反应生成氢气。例如,甲烷部分氧化法的制氢工艺如下所示。

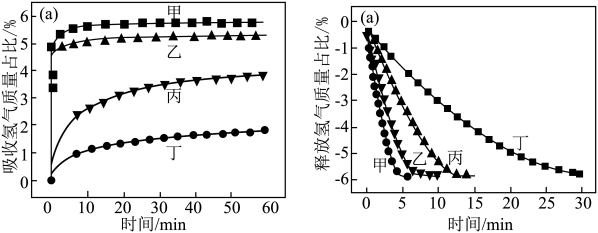
目前的储氢方法主要是高压气态存储和低温液态储氢,两种储氢方法存在一定的安全隐患。因此,目前人们在重点研究固态储氢。Mg-Y-Ni储氢合金是我国科学家研究的一种新型储氢材料。其吸收和释放氢气的效率如下图所示。
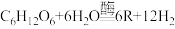 ,R的化学式是
,R的化学式是(2)部分氧化法中,CO转化时与高温水蒸气反应的化学方程式是
(3)甲、乙、丙、丁四种材料中储氢性能最好的是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】阅读下列短文,回答相关问题。
氢能
氢能是一种理想的清洁能源,其制取和储存是科学研究的重要方向。
制氢的技术有多种,其中煤气化制氢约占56%、天然气重整制氢约占21%,电解水制氢约占1%。此外,在一定温度下,利用Fe-Mo/C作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中Mo与Fe最佳质量比的实验结果如图1,氢气产率越高,说明催化剂效果越好。
近几年,制氢的工艺也有进展。我国科学家发明了一种用稀土元素铈(Ce)的氧化物为催化剂将甲烷中的氢转化为氢气的工艺,反应原理如图2所示。
目前,我国已经成为世界最大的制氢国。随着低耗能制氢及高效储氢问题的解决,氢能终将在各领域实现大规模的应用。_______ (选填“可再生”或“不可再生”)能源。
(2)对比图1中的曲线,得到的实验结论是____________ 。
(3)图2中反应器Ⅱ内发生的化学方程式为___________ 。
(4)图3中“储氢”消耗的氢气质量________ (选填“>”、“=”或“<”)“释氢”产生的氢气质量。
(5)下列说法中不正确的是________ (填序号)。
a.目前制氢的原料主要来源于化石燃料
b.裂解乙醇(C2H5OH)制氢指将乙醇分解成H2和CO2
c现阶段氢能已经大规模使用
氢能
氢能是一种理想的清洁能源,其制取和储存是科学研究的重要方向。
制氢的技术有多种,其中煤气化制氢约占56%、天然气重整制氢约占21%,电解水制氢约占1%。此外,在一定温度下,利用Fe-Mo/C作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中Mo与Fe最佳质量比的实验结果如图1,氢气产率越高,说明催化剂效果越好。
近几年,制氢的工艺也有进展。我国科学家发明了一种用稀土元素铈(Ce)的氧化物为催化剂将甲烷中的氢转化为氢气的工艺,反应原理如图2所示。


目前,我国已经成为世界最大的制氢国。随着低耗能制氢及高效储氢问题的解决,氢能终将在各领域实现大规模的应用。

(2)对比图1中的曲线,得到的实验结论是
(3)图2中反应器Ⅱ内发生的化学方程式为
(4)图3中“储氢”消耗的氢气质量
(5)下列说法中不正确的是
a.目前制氢的原料主要来源于化石燃料
b.裂解乙醇(C2H5OH)制氢指将乙醇分解成H2和CO2
c现阶段氢能已经大规模使用
您最近一年使用:0次



