用化学方程式表示:
(1)用稀盐酸除去小刀上的铁锈______________ 。
(2)有非金属单质参加的置换反应_____________________ 。
(3)有非金属单质生成的反应_____________________ 。
(1)用稀盐酸除去小刀上的铁锈
(2)有非金属单质参加的置换反应
(3)有非金属单质生成的反应
2017九年级下·江苏·专题练习 查看更多[2]
更新时间:2016-11-27 16:33:15
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】科学食用营养物质,可以保障人体健康。
(1)某同学的部分体液的pH如如图所示。________ 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平【主要成分为 】治疗,其原理是
】治疗,其原理是________ (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
①次氯酸钠中氯元素的化合价为_______ ,次氯酸的化学式为_______ 。
②据表信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1:_____ 进行稀释,即可用于餐具消毒。
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气( )。请将该反应的化学方程式补充完整:
)。请将该反应的化学方程式补充完整: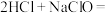
____ 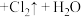 。
。
(1)某同学的部分体液的pH如如图所示。
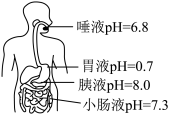
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平【主要成分为
 】治疗,其原理是
】治疗,其原理是(2)某84消毒液产品的部分说明如下表。
| 84消毒液 【产品特点】主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%. 【餐具消毒】用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 【注意事项】 ①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如厕类清洁产品)同时使用。 |
②据表信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1:
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(
 )。请将该反应的化学方程式补充完整:
)。请将该反应的化学方程式补充完整: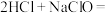
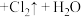 。
。
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下列科普短文,然后回答问题。
臭氧的化学式是O3,在通常状况下是淡蓝色、有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成O2,并放出大量的热,臭氧的氧化能力比氧气(O2)强得多。若将O2通过臭氧发生器,在无声放电条件下,从臭氧发生器出来的O2中含有3%的O3.臭氧在地面附近的大气层中含量极少,在离地面25km处有一个厚度极薄的臭氧层。臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害。它是一切生命的保护层,超音速飞机排出的废气中的一氧化碳(CO)、二氧化碳(CO2)、一氧化氮(NO)等气体、家用电冰箱中使用的制冷剂“氟里昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加,如不采取措施,后果不堪设想。
(1)写出臭氧(O3)的物理性质___________ (至少写出一条),臭氧(O3)___________ (填“属于”或“不属于”)空气污染物。
(2)将带火星的木条伸入到盛有臭氧(O3)的集气瓶中,可以看到___________ 的现象。
(3)红磷在臭氧中燃烧与在氧气中燃烧相似,生成物相同,请写出红磷在臭氧中燃烧的符号表达式:___________ 。
(4)应采取___________ 的方法保护臭氧层。
(5)大气中的臭氧层遭破坏,它会引起___________。
臭氧的化学式是O3,在通常状况下是淡蓝色、有鱼腥臭味的气体。臭氧不稳定,一旦受热极易转化成O2,并放出大量的热,臭氧的氧化能力比氧气(O2)强得多。若将O2通过臭氧发生器,在无声放电条件下,从臭氧发生器出来的O2中含有3%的O3.臭氧在地面附近的大气层中含量极少,在离地面25km处有一个厚度极薄的臭氧层。臭氧层能吸收太阳辐射中的大量紫外线,使地球上的生物免遭紫外线的伤害。它是一切生命的保护层,超音速飞机排出的废气中的一氧化碳(CO)、二氧化碳(CO2)、一氧化氮(NO)等气体、家用电冰箱中使用的制冷剂“氟里昂”等对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加,如不采取措施,后果不堪设想。
(1)写出臭氧(O3)的物理性质
(2)将带火星的木条伸入到盛有臭氧(O3)的集气瓶中,可以看到
(3)红磷在臭氧中燃烧与在氧气中燃烧相似,生成物相同,请写出红磷在臭氧中燃烧的符号表达式:
(4)应采取
(5)大气中的臭氧层遭破坏,它会引起___________。
| A.光合作用增加 | B.动物生长得更好 | C.皮肤癌患者增多 | D.太阳照射时间长 |
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】化学兴趣小组的同学在学完了九年级化学上册课本后,设计了如下几个小实验,请你完成下列问题。
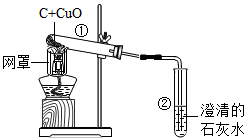
实验一、探究碳的还原性
(1)酒精灯加灯罩的目的______________ ;
(2)先预热然后集中加热,可观察到试管中的现象是________________ ,请你写出反应的化学方程式:_____________________ ;
(3)停止加热时,应先将导管从试管②中撤出,再熄灭酒精灯,这样的操作的原因是___________________ 。
实验二、探究天然水的组成
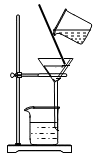
(1)化学小组的同学为了探究天然水的组成,从学校附近的人工湖边收集了一瓶湖水,发现收集的湖水中含有大量杂质无法实验,因此决定先进行过滤,装置图如图所示,图中玻璃棒的作用是________ ,过滤后发现滤液仍浑浊,可能的原因是_______________________ 。
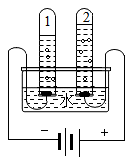
(2)经过二次过滤后可进行下一步实验,实验装置如图所示,试管1中的气体是_____________________ ,该反应的化学方程式是____________________ ,该实验最终得到的实验结论是______________________ 。

实验一、探究碳的还原性
(1)酒精灯加灯罩的目的
(2)先预热然后集中加热,可观察到试管中的现象是
(3)停止加热时,应先将导管从试管②中撤出,再熄灭酒精灯,这样的操作的原因是
实验二、探究天然水的组成
(1)化学小组的同学为了探究天然水的组成,从学校附近的人工湖边收集了一瓶湖水,发现收集的湖水中含有大量杂质无法实验,因此决定先进行过滤,装置图如图所示,图中玻璃棒的作用是

(2)经过二次过滤后可进行下一步实验,实验装置如图所示,试管1中的气体是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】碳与碳的化合物在工农业生产及日常生活中有广泛的用途。
(1)如图是碳原子结构示意图,质子数为______ ,在元素周期表中位于第______ 周期。最外层电子数为______ ,常温下不易得失电子,所以化学性质_________ ,古代用墨书写或绘制的字画可保持年久仍不变色。
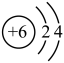
(2)木炭具有_________ 性,可用于冶金工业。还原氧化铜的实验化学方程式为____ ,可以看到的现象是____________ 。酒精灯加网罩的目的是______________ 。
(1)如图是碳原子结构示意图,质子数为

(2)木炭具有
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B为两种黑色粉末,D为红色单质。E是一种白色沉淀,C、F组成元素相同,且F是一种极易与血红蛋白结合的有毒气体,A、B、C、D、E、F五种物质之间的转化关系如下图所示。(部分生成物已省略)请回答:
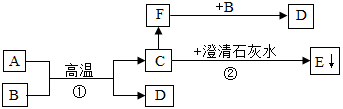
(1)D的化学式为___________ ,F的化学式为___________ ,A与B发生反应的化学方程式为___________ 。
(2)将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了。造成小白鼠死亡的主要原因___________ (填“相同”或“不同”)。

(1)D的化学式为
(2)将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了。造成小白鼠死亡的主要原因
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】某学习小组用如图I所示装置测定锌铜合金中锌、铜的质量分数。
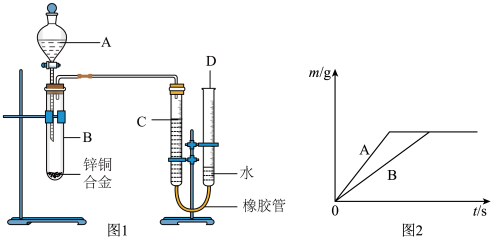
(1)实验前,先将锌铜合金在稀硫酸中浸泡片刻,其目的______ 。
(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量稀硫酸试剂。
上述再进行的操作的顺序是______ (填序号);
(3)B中发生反应的化学方程式为______ 。
(4)若实验用锌铜合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的数据是______。
(5)若实验用锌铜合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为______ (用含a、b的式子表示);
(6)按照(5)中的计算方法,若未洗涤过滤所得的不溶物,则测得锌的质分数将______ (填“偏大”“偏小”或“不受影响”)。
(7)将等质量锌粉和铁粉分别放入质量相等、浓度相同的稀盐酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图2所示。对该图像的理解下列说法正确的是______ (填序号)。
①A表示锌和稀盐酸的反应曲线
②反应消耗两种金属的质量相等
③反应结束后稀盐酸都没有剩余
④反应结束后两种金属一定都有剩余
(8)把锌粉放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,得到滤渣和蓝色滤液,下列说法正确的是______。

(1)实验前,先将锌铜合金在稀硫酸中浸泡片刻,其目的
(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B滴加足量稀硫酸试剂。
上述再进行的操作的顺序是
(3)B中发生反应的化学方程式为
(4)若实验用锌铜合金的质量为ag,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的数据是______。
| A.反应前加入稀硫酸的体积 | B.反应前加入稀硫酸的质量 |
| C.实验前反应装置中空气的体积 | D.实验条件下氢气的密度 |
(5)若实验用锌铜合金的质量为ag,与酸充分反应后,B中剩余固体的质量为bg,则锌的质量分数为
(6)按照(5)中的计算方法,若未洗涤过滤所得的不溶物,则测得锌的质分数将
(7)将等质量锌粉和铁粉分别放入质量相等、浓度相同的稀盐酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图2所示。对该图像的理解下列说法正确的是
①A表示锌和稀盐酸的反应曲线
②反应消耗两种金属的质量相等
③反应结束后稀盐酸都没有剩余
④反应结束后两种金属一定都有剩余
(8)把锌粉放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,得到滤渣和蓝色滤液,下列说法正确的是______。
| A.滤液中只有硝酸铜 | B.滤渣中含有锌 |
| C.滤液中一定有硝酸锌和硝酸铜 | D.滤渣中一定含有铜和银 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】铁元素是人体血液中血红蛋白的重要组成元素。绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以某工厂的铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
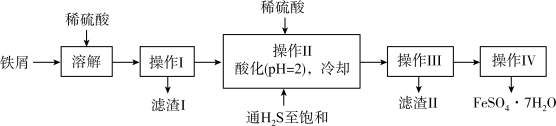
查询资料,得有关物质的相关数据如下表:
(1)操作Ⅰ的名称是_________ 。
(2)为了提高溶解的速率,可采用的措施是_______ (填一种即可)。
(3)已知金属活动性:铁>锡>氢,请写出稀硫酸与锡(反应后为+2价)发生反应的化学方程式________ 。
(4)通过分析查阅资料数据,操作Ⅱ中通入硫化氢至饱和并且用硫酸酸化至pH=2的目的之一是_____ 。
(5)操作Ⅳ得到的绿矾晶体用少量水洗涤,洗涤的目的是_________ 。

查询资料,得有关物质的相关数据如下表:
| 25℃时 | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
(1)操作Ⅰ的名称是
(2)为了提高溶解的速率,可采用的措施是
(3)已知金属活动性:铁>锡>氢,请写出稀硫酸与锡(反应后为+2价)发生反应的化学方程式
(4)通过分析查阅资料数据,操作Ⅱ中通入硫化氢至饱和并且用硫酸酸化至pH=2的目的之一是
(5)操作Ⅳ得到的绿矾晶体用少量水洗涤,洗涤的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】黄铜是以Zn为主要添加元素的铜合金。黄铜渣中还含有Zn、ZnO、Cu、CuO,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
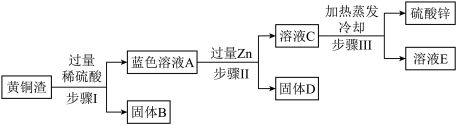
(1)步骤Ⅰ中产生气体的化学反应方程式为______ 。
(2)溶液A中的金属阳离子有______ (填化学式)。
(3)步骤Ⅰ、Ⅱ中均包含的操作名称为______ ,此操作中要用到的玻璃仪器是______ 。
(4)根据步骤Ⅲ可以推出硫酸锌的溶解度受温度影响______ 。

(1)步骤Ⅰ中产生气体的化学反应方程式为
(2)溶液A中的金属阳离子有
(3)步骤Ⅰ、Ⅱ中均包含的操作名称为
(4)根据步骤Ⅲ可以推出硫酸锌的溶解度受温度影响
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D分别表示初中化学常见的四种物质,它们的反应和转化关系如图所示(“一”表示两种物质能发生反应,“ ”或“
”或“ ”表示两种物质间能单向转化或双向转化,且省略部分反应物或生成物及条件),A与B反应可生成D,C与D反应可生成B。
”表示两种物质间能单向转化或双向转化,且省略部分反应物或生成物及条件),A与B反应可生成D,C与D反应可生成B。
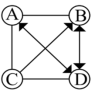
(1)若D为细铁丝,且B为黑色固体氧化物,请回答:
①写出A、C的化学式:A______ ;C_______ ;
②C与D发生反应生成B的实验现象为:银白色固体剧烈燃烧,______ ,生成一种黑色固体。
(2)若D为氯化钡时,B为胃液主要成分,请回答:
①写出AB的化学式:A______ ;B________ ;
②C与D发生反应的化学方程式为________ 。
 ”或“
”或“ ”表示两种物质间能单向转化或双向转化,且省略部分反应物或生成物及条件),A与B反应可生成D,C与D反应可生成B。
”表示两种物质间能单向转化或双向转化,且省略部分反应物或生成物及条件),A与B反应可生成D,C与D反应可生成B。
(1)若D为细铁丝,且B为黑色固体氧化物,请回答:
①写出A、C的化学式:A
②C与D发生反应生成B的实验现象为:银白色固体剧烈燃烧,
(2)若D为氯化钡时,B为胃液主要成分,请回答:
①写出AB的化学式:A
②C与D发生反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的化合物,图中短线表示两种物质在一定条件下可以发生化学反应,请你据图回答。
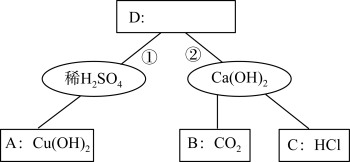
(1)A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是_______ 。
(2)能同时实现反应①和②的物质D是________ (填一种),反应①的实验现象为_____ 。
(3)请写出氢氧化钙与B发生反应的化学方程式___ 。

(1)A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是
(2)能同时实现反应①和②的物质D是
(3)请写出氢氧化钙与B发生反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
【推荐3】A~H是初中化学常见的八种物质,且分别由H、C、N、O、Na、S、Cl、Ca、Fe、Ag中的一种或几种元素组成。它们之间的转化关系如图所示。(图中“→”表示物质间存在转化关系,“—”表示两端的物质能发生反应,图中已略去部分物质),其中A是年产量最高的金属;D、G类别相同;B、F类别相同;E是氧化物:G是胃酸的主要成分,H俗称为纯碱。请回答:___________ 。
(2)H—F反应的化学方程式为___________ 。
(3)D→G反应的化学方程式为___________ 。
(4)A与G反应的基本反应类型是___________ 。
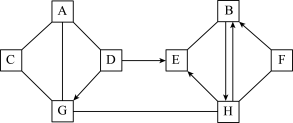
(2)H—F反应的化学方程式为
(3)D→G反应的化学方程式为
(4)A与G反应的基本反应类型是
您最近一年使用:0次



