某小组同学取过氧化氢溶液与二氧化锰的混合物155.5 g,反应后分别于t1、t2、t3、t4分钟后,分别称量剩余质量,记录的有关数据如下表:
试计算:
(1)计算:参加反应的过氧化氢质量____ 。
(2)另一组同学收集生成的氧气并测量体积,结果发现比理论值大,其原因可能是______ 。
| 反应时间t/min | t1 | t2 | t3 | t4 |
| 剩余质量(g) | 153.4 | 151.2 | 150.7 | 150.7 |
(1)计算:参加反应的过氧化氢质量
(2)另一组同学收集生成的氧气并测量体积,结果发现比理论值大,其原因可能是
更新时间:2023-03-04 16:57:19
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某固体样品由氧化铜和铜粉混合而成,为了确定该样品中各成分的比例。某兴趣小组将5.0g该样品放入如图1装置中,固体样品反应完全后实验测定的数据如图2所示,根据要求回答问题:

I.CO还原CuO实验
(1)如图1装置有一处明显缺陷是______ ;检验装置气密性后,装入药品,实验开始,应该先______ 。
II.实验数据处理
(2)由如图2可知5.0g固体样品与足量CO反应生成CO2的质量为______ ;固体样品减少的质量是______ (填字母序号)。
A.5.0g固体样品中CuO的质量
B.5.0g固体样品中CuO所含铜元素的质量
C.5.0g固体样品中CuO所含氧元素的质量
D.参加反应的CO中所含氧元素的质量
(3)计算该样品中CuO的质量______ (写出计算过程)。
(4)该样品中铜元素的质量分数是_______ 。

I.CO还原CuO实验
(1)如图1装置有一处明显缺陷是
II.实验数据处理
(2)由如图2可知5.0g固体样品与足量CO反应生成CO2的质量为
A.5.0g固体样品中CuO的质量
B.5.0g固体样品中CuO所含铜元素的质量
C.5.0g固体样品中CuO所含氧元素的质量
D.参加反应的CO中所含氧元素的质量
(3)计算该样品中CuO的质量
(4)该样品中铜元素的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】“碳中和”指力争实现二氧化碳的排放量等于二氧化碳的吸收量,二氧化碳的吸收方式有“自然吸收”和“人工转化”。
(1)“自然吸收”的途径之一是“海水吸收”,其涉及的原理包括水与二氧化碳发生的反应,其化学方程式为___________ 。
(2)“人工转化”的方法之一是指二氧化碳转化为优质的燃料甲醇(CH3OH)。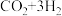

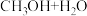 ,请计算,要得到32吨甲醇,理论上可以吸收多少吨二氧化碳?(写出计算过程)
,请计算,要得到32吨甲醇,理论上可以吸收多少吨二氧化碳?(写出计算过程)
(1)“自然吸收”的途径之一是“海水吸收”,其涉及的原理包括水与二氧化碳发生的反应,其化学方程式为
(2)“人工转化”的方法之一是指二氧化碳转化为优质的燃料甲醇(CH3OH)。
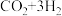

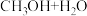 ,请计算,要得到32吨甲醇,理论上可以吸收多少吨二氧化碳?(写出计算过程)
,请计算,要得到32吨甲醇,理论上可以吸收多少吨二氧化碳?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将3.9g过氧化钠粉末逐渐加入101.8g低温硫酸铜溶液中,至恰好完全反应后过滤,得到蓝色沉淀和无色滤液。其反应过程如下:第一步:2Na2O2+2H2O=4NaOH+O2↑;第二步:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。请根据相关信息回答下列问题。
(1)生成氧气的质量为_______ g。
(2)请计算反应后所得溶液的溶质质量分数。(请写出计算过程)
(1)生成氧气的质量为
(2)请计算反应后所得溶液的溶质质量分数。(请写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组的同学在实验室发现一瓶久置过氧化氢溶液,溶质质量分数标明为10%。为探究该瓶过氧化氢溶液的实际溶质质量分数,进行如下实验:取34.0g过氧化氢溶液放入盛有2g二氧化锰固体的烧杯中,静置至质量不再改变,测得相关实验数据如图:

(1)二氧化锰的作用是_________。
(2)过氧化氢溶液中溶质的质量分数是_____________?

(1)二氧化锰的作用是_________。
(2)过氧化氢溶液中溶质的质量分数是_____________?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】小璐向容器中加入85.2g双氧水和二氧化锰的混合物制取氧气,其中二氧化锰的质量为0.2g,产生气体的质量变化如下图所示。已知每68份质量的过氧化氢完全分解可产生36份质量的水和32份质量的氧气。_____ g;
(2)求原双氧水中过氧化氢的质量分数(质量分数是指混合物中某种物质质量占总质量的百分比)。

(2)求原双氧水中过氧化氢的质量分数(质量分数是指混合物中某种物质质量占总质量的百分比)。
您最近一年使用:0次



