某化学兴趣小组的同学想从含有Al2(SO4)3、CuSO4的废液中回收金属铜,设计流程如图:
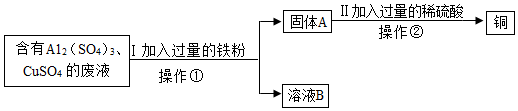
(1)操作①是________ 。
(2)I中有关反应的化学方程式________ 。
(3)溶液B中所含的溶质是________ ;固体A的成分是_______ 。(均填化学式)
(4)II中加入过量的稀硫酸的目的是_________ 。

(1)操作①是
(2)I中有关反应的化学方程式
(3)溶液B中所含的溶质是
(4)II中加入过量的稀硫酸的目的是
更新时间:2023-03-04 11:44:45
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】开发利用氢能源是实现可持续发展的需要。
(1)根据如图示分析,回答问题:

①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是________ (填序号)。
A 涤纶靠垫
B 橡胶轮胎
C 铜质导线
D 铝合金轮毂
②氢燃料电池的工作原理是:将氢气送到燃料电池中,经过催化剂的作用,通过质子交换膜,再与氧气反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式_____ 。
③氢气作燃料未能广泛应用的原因是(填一点)______ 。
(2)工业上可通过如图工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。
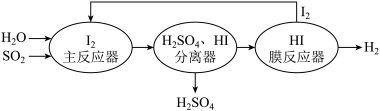
主反应器中反应的化学方程式是__ 。膜反应器中反应的类型是_____ 。
(1)根据如图示分析,回答问题:

①氢燃料电池汽车模型标示的各部件中,用金属材料制成的是
A 涤纶靠垫
B 橡胶轮胎
C 铜质导线
D 铝合金轮毂
②氢燃料电池的工作原理是:将氢气送到燃料电池中,经过催化剂的作用,通过质子交换膜,再与氧气反应,同时产生电流。请写出氢燃料电池工作原理示意图中反应的化学方程式
③氢气作燃料未能广泛应用的原因是(填一点)
(2)工业上可通过如图工艺流程处理工厂排放的含二氧化硫的尾气并获得氢气。

主反应器中反应的化学方程式是
您最近一年使用:0次
【推荐2】目前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡,如图是碳循环和碳中和策略的示意图。

(1)化石燃料包括煤、石油和___________ 。
(2)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一、对此可采取的碳中和策略②有___________ 。
(3)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式___________ 。
(4)2020年12月下旬,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由___________ 。

(1)化石燃料包括煤、石油和
(2)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一、对此可采取的碳中和策略②有
(3)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式
(4)2020年12月下旬,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列化学反应的方程式及方程式配平。
(1)硫在氧气中充分燃烧___________ 。
(2)氧化铜与氢气在加热条件下反应___________ 。
(3)加热氯酸钾和二氧化锰混合物___________ 。
(4)铁与硫酸铜溶液反应___________ 。
(5)配平下列化学反应方程式(将化学计量数填入空格内,计量数为1时可省略)。
①__________

②_____________

(1)硫在氧气中充分燃烧
(2)氧化铜与氢气在加热条件下反应
(3)加热氯酸钾和二氧化锰混合物
(4)铁与硫酸铜溶液反应
(5)配平下列化学反应方程式(将化学计量数填入空格内,计量数为1时可省略)。
①

②

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】金属材料在生产、生活中起着重要作用。

(1)如图是同学们经常使用的交通工具一自行车,请完成下列各题:
①图中所标的自行车各部件中,由金属材料制成的是________________ (答出一种即可)。
②自行车的闸线为钢丝,说明金属具有_____________ 性。
(2)铝制品具有很好的抗腐蚀性能,其原因是____________________ (用化学方程式表示)。
(3)下图是与铁的性质有关的部分实验,请回答下列问题:

①A中细铁丝燃烧的化学方程式是_______________________ 。
②B中铁钉最易生锈的部位是_______________ (填a 或b或c)。
③C中反应一段时间后,溶液颜色变化的现象是________________ ,生反应的化学方程式________________ 。
(4)下表是一些金属熔点的数据:
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为________________ (填序号)。
A300-320°C
B230-250°C
C60-80°C
D20-40°C

(1)如图是同学们经常使用的交通工具一自行车,请完成下列各题:
①图中所标的自行车各部件中,由金属材料制成的是
②自行车的闸线为钢丝,说明金属具有
(2)铝制品具有很好的抗腐蚀性能,其原因是
(3)下图是与铁的性质有关的部分实验,请回答下列问题:

①A中细铁丝燃烧的化学方程式是
②B中铁钉最易生锈的部位是
③C中反应一段时间后,溶液颜色变化的现象是
(4)下表是一些金属熔点的数据:
| 金属 | 锡 | 铅 | 铋 | 镉 |
| 熔点/°C | 231.9 | 327.5 | 271.3 | 320.9 |
A300-320°C
B230-250°C
C60-80°C
D20-40°C
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】分类、类比是学习化学常用的方法。
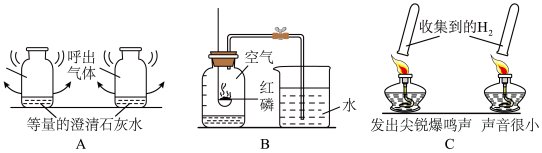
(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将上述实验中的 A 与_______ 分为一类,分类依据是_______ 。
(2)已知镓(Ga)及其化合物应用广泛,常用于半导体、合金、磁性材料等领域。已知镓在化合物中常为+3 价,金属活动性顺序:Zn>Ga>Fe。(已知氢氧化镓是难溶于水的白色固体,且镓的硫酸盐和盐酸盐都是可溶的)请设计金属镓转化为氢氧化镓的一种方案,并用方程式表示出来(依次写出化学方程式)_______ 。

(1)在初中化学学习中,我们进行了比较物质的含量多少、测定物质的含量等不同类型的化学实验,据此将上述实验中的 A 与
(2)已知镓(Ga)及其化合物应用广泛,常用于半导体、合金、磁性材料等领域。已知镓在化合物中常为+3 价,金属活动性顺序:Zn>Ga>Fe。(已知氢氧化镓是难溶于水的白色固体,且镓的硫酸盐和盐酸盐都是可溶的)请设计金属镓转化为氢氧化镓的一种方案,并用方程式表示出来(依次写出化学方程式)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某工厂欲从只含有 的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
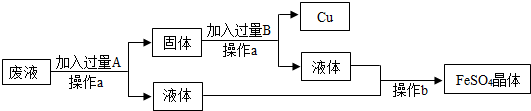
(1)操作 、
、 的名称分别是
的名称分别是______ 、______ 。
(2) 是
是______ ,加入过量 的目的是
的目的是______ 。 是
是______ ,利用其除去铜中杂质。写出流程中有关反应的化学方程式:______ 、______ 。以上两个反应能够发生的原因是______ 。
 的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
(1)操作
 、
、 的名称分别是
的名称分别是(2)
 是
是 的目的是
的目的是 是
是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】老师用下图所示装置为同学们做了一个实验。A装置中装有体积比约为3:1的空气和二氧化碳的混合气;B装置中盛有足量铁粉;C装置中盛有足量的稀硫酸。

(1)关闭活塞K,当将A装置中胶头滴管里足量的氢氧化钠溶液挤入瓶中,可以观察到A装置中的现象是_________ ;A装置发生反应的化学方程式_________ 。
(2)立即打开活塞K,一段时间后,关闭活塞K。在整个实验过程中,可以观察到C装置中的现象是_________ ;_________ 。
(3)C装置的作用是_________ (填字母)。
a.提供药品 b.控制气体总量 c.调节装置内的压强 d.可用来储存气体

(1)关闭活塞K,当将A装置中胶头滴管里足量的氢氧化钠溶液挤入瓶中,可以观察到A装置中的现象是
(2)立即打开活塞K,一段时间后,关闭活塞K。在整个实验过程中,可以观察到C装置中的现象是
(3)C装置的作用是
a.提供药品 b.控制气体总量 c.调节装置内的压强 d.可用来储存气体
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】硫酸亚铁晶体是重要的化学试剂。传统制备方法是用铁屑与稀硫酸反应,因铁屑中含有硫、磷等杂质,与稀硫酸反应会产生刺鼻、呛人的有毒气体。某科技小组改用铁屑与硫酸铜溶液反应制备硫酸亚铁晶体,流程如下:
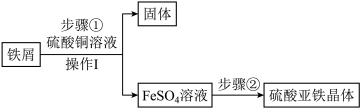
(1)步骤①中反应的化学方程式为___________ ;该反应的现象是___________ 。
(2)操作Ⅰ的名称是___________ ,用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(3)用硫酸铜溶液代替稀硫酸制备硫酸亚铁晶体,优点是___________ 。

(1)步骤①中反应的化学方程式为
(2)操作Ⅰ的名称是
(3)用硫酸铜溶液代替稀硫酸制备硫酸亚铁晶体,优点是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】在一定温度下,将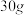 、
、 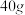 、
、 、
、 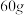 、
、 的硝酸钾固体分别加入到
的硝酸钾固体分别加入到  水中,其五次实验数据记录如下表:(
水中,其五次实验数据记录如下表:(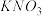 的溶解能力随温度升高而增大)
的溶解能力随温度升高而增大)
根据表中数据分析回答下列问题:
(1)第_________ 次起得到的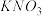 溶液为饱和溶液;
溶液为饱和溶液;
(2)在该温度下, 水中溶解
水中溶解 ___________ 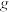
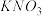 刚好达到饱和,所得溶液的溶质质量分数是
刚好达到饱和,所得溶液的溶质质量分数是 ___ ;
(3)要使接近饱和的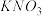 溶液,在不改变溶液质量的前提下变为饱和溶液,可以采用的方法是
溶液,在不改变溶液质量的前提下变为饱和溶液,可以采用的方法是 _ ;
(4)如图所示,小烧杯中盛放的是硝酸钾的饱和溶液,若将少量的下列物质分别放入大烧杯中的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是_________ (填字母)。

A.硝酸铵 B.氢氧化钠 C.冰 D.浓硫酸
(5)通过___________ 操作可将上述(4)中析出的硝酸钾晶体与硝酸钾溶液分离。
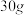 、
、 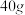 、
、 、
、 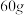 、
、 的硝酸钾固体分别加入到
的硝酸钾固体分别加入到  水中,其五次实验数据记录如下表:(
水中,其五次实验数据记录如下表:(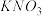 的溶解能力随温度升高而增大)
的溶解能力随温度升高而增大)实验次数 | 1 | 2 | 3 | 4 | 5 |
加入 | 30 | 40 | 50 | 60 | 70 |
所得 | 80 | 90 | 100 | 105 | 105 |
(1)第
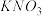 溶液为饱和溶液;
溶液为饱和溶液;(2)在该温度下,
 水中溶解
水中溶解 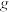
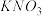 刚好达到饱和,所得溶液的溶质质量分数是
刚好达到饱和,所得溶液的溶质质量分数是 (3)要使接近饱和的
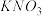 溶液,在不改变溶液质量的前提下变为饱和溶液,可以采用的方法是
溶液,在不改变溶液质量的前提下变为饱和溶液,可以采用的方法是 (4)如图所示,小烧杯中盛放的是硝酸钾的饱和溶液,若将少量的下列物质分别放入大烧杯中的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是

A.硝酸铵 B.氢氧化钠 C.冰 D.浓硫酸
(5)通过
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】生产印刷电路板产生的废液,如果直接排放,会对自然环境产生严重污染。工厂对废液的处理经常采取如下流程中的两种途径变废为宝,如图,请回答:

(1)操作a的名称是___________ 。
(2)写出FeCl3溶液与敷铜板中的铜反应生成FeCl2和CuCl2的化学方程式:___________ 。
(3)途径①向废液加入过量铁粉。检验铁粉是否过量的方法是:在滤渣中___________ 。
(4)从节能角度看,途径___________ (填“①”或“②”)更优越。

(1)操作a的名称是
(2)写出FeCl3溶液与敷铜板中的铜反应生成FeCl2和CuCl2的化学方程式:
(3)途径①向废液加入过量铁粉。检验铁粉是否过量的方法是:在滤渣中
(4)从节能角度看,途径
您最近一年使用:0次





