请回答下列问题。
I.某化学兴趣小组欲用如图甲所示的装置来制取纯净干燥的二氧化碳,并测定石灰石中碳酸钙的质量分数(装置气密性良好;石灰石中杂质不参与反应;导管内的水忽略不计:试管体积相同)。

(1)仪器a的名称是_______ 。
(2)①中发生反应的化学方程式为:_______ 。
(3)②中饱和NaHCO3溶液的作用是_______ 。
(4)图甲测得石灰石中碳酸钙的质量分数_____ (填“偏大”或“偏小”)。
(5)图乙中分别加入2mL石蕊试液和2mL澄清石灰水后,观察到U型管中左边液面比右边液面低,请说明原因_______ 。
II. CO2与NaOH反应再探究。
【实验探究】探究CO2与NaOH溶液是否发生了化学反应
实验:如图丙,将收集满CO2的试管倒扣在NaOH溶液中

(6)丙中观察到的现象是_______ ;CO2与NaOH溶液反应的方程式为________ 。
(7)老师告诉同学们仅凭上述实验现象还不足以说明CO2与NaOH溶液发生了化学反应,其理由是_______ ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是______ 。
I.某化学兴趣小组欲用如图甲所示的装置来制取纯净干燥的二氧化碳,并测定石灰石中碳酸钙的质量分数(装置气密性良好;石灰石中杂质不参与反应;导管内的水忽略不计:试管体积相同)。

(1)仪器a的名称是
(2)①中发生反应的化学方程式为:
(3)②中饱和NaHCO3溶液的作用是
(4)图甲测得石灰石中碳酸钙的质量分数
(5)图乙中分别加入2mL石蕊试液和2mL澄清石灰水后,观察到U型管中左边液面比右边液面低,请说明原因
II. CO2与NaOH反应再探究。
【实验探究】探究CO2与NaOH溶液是否发生了化学反应
实验:如图丙,将收集满CO2的试管倒扣在NaOH溶液中

(6)丙中观察到的现象是
(7)老师告诉同学们仅凭上述实验现象还不足以说明CO2与NaOH溶液发生了化学反应,其理由是
更新时间:2023-03-19 15:17:51
|
相似题推荐
实验题
|
适中
(0.65)
【推荐1】有一新制的碳酸钙产品,某同学设计如图所示的实验,通过测定反应生成的BaCO3的质量来确定该产品中CaCO3的含量(图中夹持仪器已略去,杂质不与盐酸反应,NaOH溶液可吸收CO2,Ba(OH)2溶液与CO2的反应与Ca(OH)2溶液与CO2的反应相似,碱石灰主要成分为NaOH和CaO,可吸收H2O和CO2)。

(1)关闭止水夹,打开分液漏斗活塞,缓慢滴加盐酸至不再有气泡产生,关闭分液漏斗活塞;打开止水夹,缓缓通入空气。通入空气的作用是___________ 。
(2)装置B中发生反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验时,称取的碳酸钙产品的质量为m1g,反应后得到BaCO3的质量为m2g,则该产品中CaCO3的质量分数为___________ (用含m1和m2的代数式表示)。

(1)关闭止水夹,打开分液漏斗活塞,缓慢滴加盐酸至不再有气泡产生,关闭分液漏斗活塞;打开止水夹,缓缓通入空气。通入空气的作用是
(2)装置B中发生反应的化学方程式为
(3)装置D的作用是
(4)实验时,称取的碳酸钙产品的质量为m1g,反应后得到BaCO3的质量为m2g,则该产品中CaCO3的质量分数为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】某同学为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如下图所示的装置(图中的铁架台已略去),实验步骤如下:①按图连接好装置;②称取氢氧化钠样品2克,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中过量,关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液220mL。请回答下列问题:
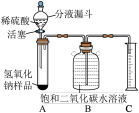
(1)判断氢氧化钠变质的实验现象是__________ ,氢氧化钠变质的原因是_________ ,因此,实验中氢氧化钠必须____________________ 保存。
(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是__________ 。
(3)B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是__________ 。
(4)判断步骤③中滴入的稀硫酸已过量的标志是______________________ 。
(5)氢氧化钠样品中的碳酸钠的质量分数为__________ 。(CO2的密度约为2.0g /L,二氧化碳的体积等于排出的饱和二氧化碳水溶液的体积。)
(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是_____ 。

(1)判断氢氧化钠变质的实验现象是
(2)在实验步骤①和②之间,还缺少一个实验步骤,该实验步骤是
(3)B中集气瓶装的饱和二氧化碳水溶液不能用水代替,其理由是
(4)判断步骤③中滴入的稀硫酸已过量的标志是
(5)氢氧化钠样品中的碳酸钠的质量分数为
(6)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】工业上用电解饱和食盐水的方法制得的烧碱中常含有一定量的氯化钠。为测定某烧碱样品的纯度,同学们设计了如下方案。
方案一:称取mg烧碱样品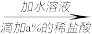 测定消耗稀盐酸的质量。
测定消耗稀盐酸的质量。
方案二:称取mg烧碱样品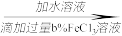 测定生成沉淀的质量。
测定生成沉淀的质量。
请回答:
(1)方案一中发生反应的化学方程式为____ 。方案二中加入FeCl3溶液后出现的现象为____ 。
(2)方案一中为减少误差,最好选择下列方法中的_____ 来判断反应恰好完全进行。
A 向样品溶液中滴加2-3滴无色酚酞溶液根据溶液颜色变化判断
B 测定过程中边滴加稀盐酸边用pH试纸频繁测定混合液的pH
C 向样品溶液中滴加2-3滴紫色石蕊溶液,根据颜色变化判断。
(3)小李同学认为判断方案二中氯化铁FeCl3溶液过量的化学方法是____ 。
(4)小李同学可将方案二中的FeCl3溶液换成稀硝酸和__ (填化学式)溶液也能达到实验的目的。
(5)若方案二准确测得生成沉淀的质量为ng,则烧碱样品的纯度为___ (用分数表示)
方案一:称取mg烧碱样品
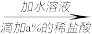 测定消耗稀盐酸的质量。
测定消耗稀盐酸的质量。方案二:称取mg烧碱样品
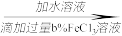 测定生成沉淀的质量。
测定生成沉淀的质量。请回答:
(1)方案一中发生反应的化学方程式为
(2)方案一中为减少误差,最好选择下列方法中的
A 向样品溶液中滴加2-3滴无色酚酞溶液根据溶液颜色变化判断
B 测定过程中边滴加稀盐酸边用pH试纸频繁测定混合液的pH
C 向样品溶液中滴加2-3滴紫色石蕊溶液,根据颜色变化判断。
(3)小李同学认为判断方案二中氯化铁FeCl3溶液过量的化学方法是
(4)小李同学可将方案二中的FeCl3溶液换成稀硝酸和
(5)若方案二准确测得生成沉淀的质量为ng,则烧碱样品的纯度为
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】根据下列装置图回答题:

(1)写出仪器a和b的名称;a_____ ,b_____ 。
(2)实验室用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为_____ (填字母),若用F装置干燥二氧化碳气体,气体应从F装置的_____ (填左或右)侧导管通入。
(3)实验室用高锰酸钾制取氧气,该反应的化学方程式为_____ 。
(4)实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品只需盖满试管底部,液体药品取用_____ mL。

(1)写出仪器a和b的名称;a
(2)实验室用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为
(3)实验室用高锰酸钾制取氧气,该反应的化学方程式为
(4)实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品只需盖满试管底部,液体药品取用
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室现有石灰石、稀盐酸、火柴、药匙、升降台、木条、棉花、镊子及以下仪器:

(1)若要制取二氧化碳,应选择的仪器有锥形瓶和_______ (填序号),还需补充的仪器是_______ (填名称)
(2)若补充一种药品还能制取氧气,发生反应的化学方程式为_______ 。
(3)用排水法收集氧气,当观察到导管口_______ 时,开始收集,气体逸出的原因是由于试管内温度升高且_______ ,使试管内压强_______ ,大于外界大气压,在压强差的作用下,气体逸出。

(1)若要制取二氧化碳,应选择的仪器有锥形瓶和
(2)若补充一种药品还能制取氧气,发生反应的化学方程式为
(3)用排水法收集氧气,当观察到导管口
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】实验室现有药品:高锰酸钾、氯酸钾、过氧化氢溶液、二氧化锰粉末、块状石灰石、稀盐酸、稀硫酸。使用装置C反应物应为块状固体和液体,反应条件是常温,优点是可控制反应的发生和停止。根据实验室现有药品和下列装置回答问题。______ 。
(2)仪器选用:用高锰酸钾制取较纯净的O2时,则发生装置和收集装置选用______ (填字母)。
(3)药品选用:用装置C来制取CO2时,选用的药品为______ (填药品名称)。
(4)收集气体:收集CO2用装置D,则气体应从______ 口进(填“a”或“b”)。
(5)趣味实验:某同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射。下列组合能产生类似现象的是______(填字母)。

(2)仪器选用:用高锰酸钾制取较纯净的O2时,则发生装置和收集装置选用
(3)药品选用:用装置C来制取CO2时,选用的药品为
(4)收集气体:收集CO2用装置D,则气体应从
(5)趣味实验:某同学在社团活动中利用F装置“发射火箭”,先挤压胶头滴管,套在玻璃管上的塑料火箭向上冲出,完成发射。下列组合能产生类似现象的是______(填字母)。
| A.碳酸钙和水 | B.氢氧化钠和水 | C.镁和稀盐酸 |
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】如图是实验室常用的装置,请回答下列问题:

(1)写出用装置A制取氧气的化学方程式。
(2)装置C与B相比,装置C的优点是什么?
(3)若用装置D收集CO2,写出验满方法。

(1)写出用装置A制取氧气的化学方程式。
(2)装置C与B相比,装置C的优点是什么?
(3)若用装置D收集CO2,写出验满方法。
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下图的实验装置,请回答:

(1)①仪器a的名称是:_____ ,②作用是: _____ 。③若用分液漏斗代替仪器a,其优点是: _____ 。
(2)用装置F和另一仪器(除导管外)收集并测量O2体积,在F中气体应从导管_____ (填“c”或“d”)端通入。
(3)甲烷(CH4)无色无味的气体,密度比空气小,极难溶于水。实验室里常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为_____ (填字母),用装置E收集甲烷,是因为 _____ 。
②点燃可燃气体(如:CH4)前一定要先验纯,否则容易引起爆炸。请写出验证CH4纯度的实验操作:收集一小试管CH4,_____ ,听到较小的爆鸣声,证明CH4比较纯净。
③已知化学反应前后元素的种类没有发生变化,请设计实验证明CH4中含有氢、碳元素。

(1)①仪器a的名称是:
(2)用装置F和另一仪器(除导管外)收集并测量O2体积,在F中气体应从导管
(3)甲烷(CH4)无色无味的气体,密度比空气小,极难溶于水。实验室里常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为
②点燃可燃气体(如:CH4)前一定要先验纯,否则容易引起爆炸。请写出验证CH4纯度的实验操作:收集一小试管CH4,
③已知化学反应前后元素的种类没有发生变化,请设计实验证明CH4中含有氢、碳元素。
| 实验步骤 | 实验现象 | 实验结论 |
| 证明CH4中含有氢元素 | ||
| 证明CH4中含有碳元素 |
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】根据下列实验装置图,按要求回答有关问题:

(1)写出图中带有标号仪器的名称:a___________ ;b ___________ 。
(2)实验室用加热高锰酸钾制取氧气时,应选择的发生装置是_____ (填写装置的字母代号,下同),该装置有一处不足是__________ ,所发生反应的化学反应方程式为_________ ;基本反应类型为___________ 。
(3)实验室制取二氧化碳气体时,应选择的发生装置为______ ,应选用的收集装置是_____ 。检验二氧化碳是否收集满的方法是:将燃着的木条放在_________ ,观察火焰是否熄灭。

(1)写出图中带有标号仪器的名称:a
(2)实验室用加热高锰酸钾制取氧气时,应选择的发生装置是
(3)实验室制取二氧化碳气体时,应选择的发生装置为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】认识二氧化碳的性质
如下图是有关二氧化碳的几个性质实验:


(1)甲中的现象是__________ 。
(2)乙中发生反应的文字表达式______________ 。
(3)丙中看到的现象有_________ ,由此证明二氧化碳具有的性质是____________ 。
(4)B试管中通入二氧化碳气体,液体颜色发生改变:再将所得液体加热,现象是_____________________ 。写出后一个反应的文字或符号表达式___________ 。
认识氧气的性质
根据下图中所发生的化学反应,进行总结归纳并回答下列问题:

(5)集气瓶丙中观察到的现象是_________ 。
(6)甲、丙两瓶中均放少量水,丙瓶放水的主要原因是警____________ 。
如下图是有关二氧化碳的几个性质实验:


(1)甲中的现象是
(2)乙中发生反应的文字表达式
(3)丙中看到的现象有
(4)B试管中通入二氧化碳气体,液体颜色发生改变:再将所得液体加热,现象是
认识氧气的性质
根据下图中所发生的化学反应,进行总结归纳并回答下列问题:

(5)集气瓶丙中观察到的现象是
(6)甲、丙两瓶中均放少量水,丙瓶放水的主要原因是警
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】实验室制取气体时需要的一些装置如下图所示,请回答下列问题。

(1)写出标有序号①的仪器名称:①______ 。
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是______ ,装置中使用分液漏斗的优点是______ ;
(3)若要得到干燥的氧气,所选择装置的连接顺序为:B→______ →______ (填字母序号);
(4)检验二氧化碳是否收集满的操作方法是______ 。
(5)某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,装置中溶液变浑浊,则B装置中反应的化学方程式为______ 。
(6)(探究活动)探究二氧化碳能否与碱溶液反应。
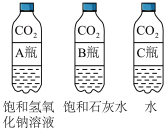
①分别振荡三个软质塑料瓶,观察到塑料瓶变瘪的程度由大到小的顺序为______ 。
②对比A瓶与______ 瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应。

(1)写出标有序号①的仪器名称:①
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是
(3)若要得到干燥的氧气,所选择装置的连接顺序为:B→
(4)检验二氧化碳是否收集满的操作方法是
(5)某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,装置中溶液变浑浊,则B装置中反应的化学方程式为
(6)(探究活动)探究二氧化碳能否与碱溶液反应。

①分别振荡三个软质塑料瓶,观察到塑料瓶变瘪的程度由大到小的顺序为
②对比A瓶与
您最近一年使用:0次
【推荐3】根据下列装置,结合所学化学知识回答问题:

(1)写出有标号仪器的名称:①______ ;②______ 。
(2)用氯酸钾制取氧气的化学方程式为______ ,若收集较纯净的氧气应选择的收集装置是_________ ,判断氧气是否集满的现象是_________ 。若用装置G收集氧气,则气体应从______ (填“a”或“b”)通入。
(3)H2O2溶液既可用作实验室制取氧气,也是常用作的消毒剂。
① H2O2溶液与二氧化锰混合制取氧气,化学方程式为______ 。
②用 的
的 溶液对不同金属进行腐蚀性实验,结果如下:
溶液对不同金属进行腐蚀性实验,结果如下:
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是______ (填序号)。
A.不锈钢锅 B. 铝盆 C. 铜火锅
(4)装置C与D组合可制取二氧化碳,反应的化学方程式为:______ ;
①装置B和C对比,用分液漏斗代替长颈漏斗进行实验的优点是_________ 。
②在圆底烧瓶中充满CO2(图1),图2是向烧瓶中分别注入同体积水和氢氧化钠溶液后通过传感器得到的气压变化图像。下列说法错误的是____ (填序号)。

A.开始时,瓶内气压增大可能是注入液体使瓶内气体压缩所致
B.曲线①显示气压最终恢复原状,说明CO2几乎不溶于水
C.两条曲线对比,可证明CO2能和氢氧化钠溶液反应
D.该实验不能证明CO2能与水反应

(1)写出有标号仪器的名称:①
(2)用氯酸钾制取氧气的化学方程式为
(3)H2O2溶液既可用作实验室制取氧气,也是常用作的消毒剂。
① H2O2溶液与二氧化锰混合制取氧气,化学方程式为
②用
 的
的 溶液对不同金属进行腐蚀性实验,结果如下:
溶液对不同金属进行腐蚀性实验,结果如下:| 金属种类 | 不锈钢片 | 铝片 | 铜片 |
| 腐蚀速度mg/h |  |  | 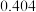 |
A.不锈钢锅 B. 铝盆 C. 铜火锅
(4)装置C与D组合可制取二氧化碳,反应的化学方程式为:
①装置B和C对比,用分液漏斗代替长颈漏斗进行实验的优点是
②在圆底烧瓶中充满CO2(图1),图2是向烧瓶中分别注入同体积水和氢氧化钠溶液后通过传感器得到的气压变化图像。下列说法错误的是

A.开始时,瓶内气压增大可能是注入液体使瓶内气体压缩所致
B.曲线①显示气压最终恢复原状,说明CO2几乎不溶于水
C.两条曲线对比,可证明CO2能和氢氧化钠溶液反应
D.该实验不能证明CO2能与水反应
您最近一年使用:0次



