某样品中含有CaCO3及少量CaCl2,小阳同学取该样品25g,再逐滴加入160g稀盐酸。反应中产生气体的质量与盐酸的用量关系如图所示。
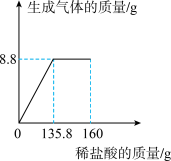
(1)产生二氧化碳的质量是__________ g。
(2)样品中碳酸钙的质量分数(写出计算过程)。

(1)产生二氧化碳的质量是
(2)样品中碳酸钙的质量分数(写出计算过程)。
2023·山西临汾·一模 查看更多[3]
更新时间:2023-04-01 21:29:11
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】某小组为了测定某矿山石灰石的纯度,取2.0 g该矿山石灰石样品,将20.0 g盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据如图所示。(已知杂质不溶于水、不溶于酸且不与酸反应)试求:

(1)该石灰石样品中杂质的质量是____g;
(2)加入的盐酸中溶质的质量分数是多少?

(1)该石灰石样品中杂质的质量是____g;
(2)加入的盐酸中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学实验室有一瓶久置的稀盐酸,华华同学想知道该盐酸的浓度。在老师的指导下,他将含碳酸钙的质量分数为80%的石灰石(杂质不溶于水也不参与反应)12.5克放入一只烧杯中,然后逐滴加入一定质量的该盐酸,恰好完全反应后,测得烧杯中物质的质量为108.1克(假设产生的气体全部逸出)。
(1)CaCO3中质量分数最大的是________________ 元素。
(2)华华同学所用盐酸的溶质质量分数。(写出计算过程)
(3)将该盐酸100克配制成浓度为5%的溶液,需要加入水的质量为________________ g。
(1)CaCO3中质量分数最大的是
(2)华华同学所用盐酸的溶质质量分数。(写出计算过程)
(3)将该盐酸100克配制成浓度为5%的溶液,需要加入水的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】请根据如图所示的实验过程和提供的数据计算,并回答下列问题:

(1)实验中发生反应的化学方程式是___________ ;
(2)求解样品中发生反应的物质的质量(x)的比例式___________ :
(3)所得不饱和溶液中溶质的质量分数为___________ ;
(4)若配制实验中所用的稀盐酸,需要溶质质量分数为36.5%的浓盐酸的质量为___________ 。
(5)工业上欲用上述样品100t制氯化钠,若不计损失,则最终能得到纯净的氯化钠的质量为____ 。
(6)通过海水晒盐也可以得到氯化钠,其大致过程如下,图A池是___________ 池。


(1)实验中发生反应的化学方程式是
(2)求解样品中发生反应的物质的质量(x)的比例式
(3)所得不饱和溶液中溶质的质量分数为
(4)若配制实验中所用的稀盐酸,需要溶质质量分数为36.5%的浓盐酸的质量为
(5)工业上欲用上述样品100t制氯化钠,若不计损失,则最终能得到纯净的氯化钠的质量为
(6)通过海水晒盐也可以得到氯化钠,其大致过程如下,图A池是

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】化学兴趣小组将鸡蛋壳粉碎(主要成分是碳酸钙)与稀盐酸进行了实验(鸡蛋壳中的其他成分不溶于水也不与酸反应),实验过程如图所示。请计算:

(1)鸡蛋壳中碳酸钙的质量为________ g。
(2)实验中鸡蛋壳捣成粉末的目的是________ ;若滤渣不经过洗涤干燥,最后计算所得碳酸钙的质量________ 。(填“ 偏大”或“偏小”)
(3)该鸡蛋壳中碳酸钙与稀盐酸完全反应生成二氧化碳的质量________ 。(写出计算过程)
(4)过滤后所得滤液的质量为________ g。

(1)鸡蛋壳中碳酸钙的质量为
(2)实验中鸡蛋壳捣成粉末的目的是
(3)该鸡蛋壳中碳酸钙与稀盐酸完全反应生成二氧化碳的质量
(4)过滤后所得滤液的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定某石灰石样品中碳酸钙的质量分数,取 25g 该样品(杂质不参加反应也不溶于水), 加入盛有 146g 稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为 162.2g。
(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数。
(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数。
您最近一年使用:0次




