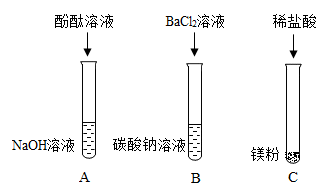
同学们在学习复分解反应条件时,进行了教材中的以下探究:利用实验室提供的五种试剂,分别在四支试管中进行如下实验,根据实验现象来判断稀硫酸与下表中四种化合物的溶液之间是否能发生反应:
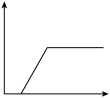
四支试管中能观察到的明显实验现象为______ 。根据复分解反应发生的条件判断某一试管没有发生化学反应的理由是______ ,A试管中发生反应的化学方程式为______ ,为了能够通过明显的实验现象证明A试管中物质发生了反应,实验小组的晓宁同学利用实验室提供的五种试剂中的部分药品,重新设计实验,将实验中的明显现象绘制成图像,如下图,则同学们设计的实验操作为______ 。为了探究晓宁实验后所得溶液溶质的成分,向所得溶液中加入______ ,通过______ 的现象确定溶液的成分。
总结:验证所得溶液中溶质成分时,只需验证______ 的物质是否存在即可。
| 编号 | A试管 | B试管 | C试管 | D试管 |
| 试剂 | 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸钡溶液 |
| 稀硫酸 |

总结:验证所得溶液中溶质成分时,只需验证
更新时间:2023-04-06 23:58:00
|
相似题推荐
填空与简答-科普阅读题
|
较难
(0.4)
名校
解题方法
【推荐1】请根据以下文章回答问题。
生物质能
生物质是指通过光合作用产生的各种有机体,生物质能是贮存在生物质中的能量。 利用秸秆生产生物质能已成为一大亮点。秸秆的生物质能利用方式有多种:将秸秆粉碎、 添加乳酸菌发酵,即可做成牲畜饲料;以秸秆为主要原料,经粉碎、厌氧发酵即可生产沼气;利 用秸秆和畜禽粪便为原料,经无害化处理、发酵腐熟就可制成有机肥料;秸秆经粉碎、水解、糖 化发酵、蒸馏等过程,可获得燃料酒精。 目前,生物质能源已成为世界第四大能源。生物质能产生二氧化碳的量相当于它生长时吸 收的二氧化碳,因而对大气的二氧化碳净排放量近似为零。
(1)生物质能是一种________ (填“可再生”或“不可再生”)能源。
(2)秸秆的生物质能利用方式中,都需要经过的一个化学变化是________ 。
(3)燃料酒精充分燃烧的化学方程式是________ 。
(4)推广使用生物质能的优点是________ 。
(5)利用秸秆生产沼气、燃料酒精的厂房应张贴的安全标志是________。
生物质能
生物质是指通过光合作用产生的各种有机体,生物质能是贮存在生物质中的能量。 利用秸秆生产生物质能已成为一大亮点。秸秆的生物质能利用方式有多种:将秸秆粉碎、 添加乳酸菌发酵,即可做成牲畜饲料;以秸秆为主要原料,经粉碎、厌氧发酵即可生产沼气;利 用秸秆和畜禽粪便为原料,经无害化处理、发酵腐熟就可制成有机肥料;秸秆经粉碎、水解、糖 化发酵、蒸馏等过程,可获得燃料酒精。 目前,生物质能源已成为世界第四大能源。生物质能产生二氧化碳的量相当于它生长时吸 收的二氧化碳,因而对大气的二氧化碳净排放量近似为零。
(1)生物质能是一种
(2)秸秆的生物质能利用方式中,都需要经过的一个化学变化是
(3)燃料酒精充分燃烧的化学方程式是
(4)推广使用生物质能的优点是
(5)利用秸秆生产沼气、燃料酒精的厂房应张贴的安全标志是________。
A. | B. | C. | D. |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】在点燃条件下,4.8gCH4与12.8gO2恰好完全反应生成10.8gH2O、5.6gCO和物质X。则X的质量为_______________ g,化学方程式为________________________ 。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】中和反应是一类重要的化学反应,某同学利用图1装置研究稀硫酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3.
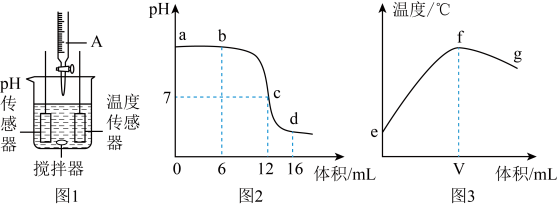
(1)图1烧杯中发生的化学反应的实质为_____ ;仪器A中溶液的溶质是_____ (填化学式);
(2)图3中V的数值最接近_____ (填“6”、“12”或“16”);
(3)下列说法错误的是_____ ;
A 图2中b点所示溶液中的溶质是硫酸钠和氢氧化钠
B 图2中c→d所示溶液中硫酸钠的质量不断增加
C 图3中e→f变化趋势可说明该反应是放热反应
(4)丙同学认为氢氧化钠溶液与稀硫酸混合没有明显现象。于是他想借助下列溶液来验证反应是否真的发生,你觉得肯定不可行的是_____ 。
A 无色酚酞试液
B 氯化钾溶液
C 氯化钡溶液
D 氢氧化镁固体
(5)实验后该同学反思,不能用氢氧化钠固体和稀硫酸反应来证明中和反应放热,原因是_____ 。

(1)图1烧杯中发生的化学反应的实质为
(2)图3中V的数值最接近
(3)下列说法错误的是
A 图2中b点所示溶液中的溶质是硫酸钠和氢氧化钠
B 图2中c→d所示溶液中硫酸钠的质量不断增加
C 图3中e→f变化趋势可说明该反应是放热反应
(4)丙同学认为氢氧化钠溶液与稀硫酸混合没有明显现象。于是他想借助下列溶液来验证反应是否真的发生,你觉得肯定不可行的是
A 无色酚酞试液
B 氯化钾溶液
C 氯化钡溶液
D 氢氧化镁固体
(5)实验后该同学反思,不能用氢氧化钠固体和稀硫酸反应来证明中和反应放热,原因是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】中和反应是一类重要的化学反应,某同学利用图 1 装置研究稀盐酸与氢氧化钠溶液反应的过程,并用 pH 和温度传感器测量反应过程中相关物理量的变化情况,得到图 2 和图 3。
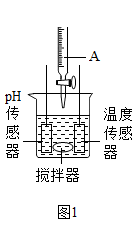
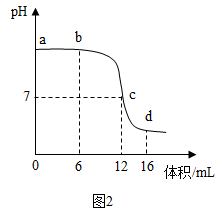
(1)下列说法正确的是 ______。
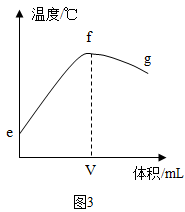
(2)图3中v的数值最接近______ 。
(3)通过微观进一步深入了解中和反应,如下图:
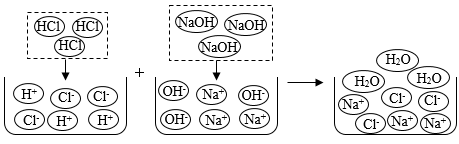
【归纳】HCl与NaOH的反应实质:_________ 的反应。



(1)下列说法正确的是 ______。
| A.图 2 中 b点所示溶液中的溶质是 NaCl和NaOH |
| B.取图 2 中 d点所示溶液加热蒸干所得固体为纯净物 |
| C.图 2 中 c→d所示溶液中 NaCl 的质量不断增加 |
| D.通过图 3 中 e→f 变化趋势可说明该反应的热量变化 |
(3)通过微观进一步深入了解中和反应,如下图:

【归纳】HCl与NaOH的反应实质:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
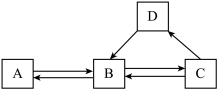
【推荐1】下图中A、B、C、D、E、F为初中化学常见的六种物质,F是一种黑色粉末,E是密度最小的气体,D是一种常见的液体,A与C可用于配制农药波尔多液(图中用“一”或“ ”表示两种物质能发生反应,用“→”或“
”表示两种物质能发生反应,用“→”或“ ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。根据判断回答下列问题:
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。根据判断回答下列问题:
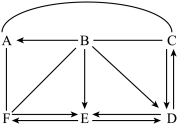
(1)E的化学式为______ 。
(2)F与少量B溶液反应的现象是______ 。
(3)B与C反应的化学方程式为______ 。
(4)D生成C的化学方程式为______ 。
 ”表示两种物质能发生反应,用“→”或“
”表示两种物质能发生反应,用“→”或“ ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。根据判断回答下列问题:
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。根据判断回答下列问题:
(1)E的化学式为
(2)F与少量B溶液反应的现象是
(3)B与C反应的化学方程式为
(4)D生成C的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3和不与酸反应的不溶性杂质)为原料制备高纯氧化镁的实验流程图如图1。
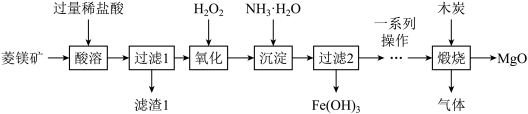
(1)酸溶时,需将菱镁矿磨成粉末状,目的是______ 。MgCO3与稀硫酸反应的化学方程式为______ 。
(2)氧化时,反应的方程式为2FeSO4+H2O2+______ ═Fe2(SO4)3+2H2O,KMnO4溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,选择H2O2的优点是______ 。
(3)沉淀时,需严格控制NH3•H2O的用量,其目的是使Fe3+完全沉淀,______ (填离子符号)不沉淀。
(4)流程中“一系列操作”主要过程为:蒸发浓缩,______ ,过滤、洗涤、干燥等。

(1)酸溶时,需将菱镁矿磨成粉末状,目的是
(2)氧化时,反应的方程式为2FeSO4+H2O2+
(3)沉淀时,需严格控制NH3•H2O的用量,其目的是使Fe3+完全沉淀,
(4)流程中“一系列操作”主要过程为:蒸发浓缩,
您最近一年使用:0次
【推荐3】(1)某城市有甲乙两工厂排放污水(两厂不含相同离子),污水中各含有下列六种离子中的三种: 、
、 、
、 、
、 、
、 、Cl- 。两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清只含
、Cl- 。两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清只含______ (填化学式)的溶液。请根据你对污水的认识,写出其中一个工厂污水中所含的离子(该工厂污水所含的三种离子已经给出一种,请补充另两种) 
______ 。
(2)从海水中提取溴常用吹出法,即用氯气将海水里溴化钠(NaBr)中的溴置.换出来,再用空气或水蒸气吹出溴(Br2),写出氯气置换出溴单质的化学方程式:______ 。该反应要在 pH=3 的酸性条件下进行,可用______ 测定反应液的酸碱度。
 、
、 、
、 、
、 、
、 、Cl- 。两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清只含
、Cl- 。两厂单独排放都会造成严重的水污染,若将两厂的污水按一定比例混合,便会变成无色澄清只含
(2)从海水中提取溴常用吹出法,即用氯气将海水里溴化钠(NaBr)中的溴置.换出来,再用空气或水蒸气吹出溴(Br2),写出氯气置换出溴单质的化学方程式:
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐1】实验室有三瓶失去标签的无色液体,分别是氢氧化钙溶液、氢氧化钠溶液和氯化钾溶液,设计一个实验方案把它们区别开来,并完成以下实验报告。
| 实验操作 | 预期现象与结论 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环,如图所示:

(1)步骤1的化学方程式为:__
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量__ 溶液,若观察到试管内 __ .则分解不完全.
(3)CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为__ ,若要检验甲酸水溶液是否显酸性,能选用的有 __ (填字母序号)
a.无色酚酞溶液 b.紫色石蕊溶液 c.PH试纸
(3)请列举CO2的另一种用途__ .

(1)步骤1的化学方程式为:
(2)为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量
(3)CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为
a.无色酚酞溶液 b.紫色石蕊溶液 c.PH试纸
(3)请列举CO2的另一种用途
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐3】制作皮蛋料泥的原料主要有:生石灰、纯碱、草木灰(含K2CO3)等。将它们按一定比例混合加入适量水得到皮蛋料泥。料泥的主要成分是什么呢?同学们进行了如图所示的探究:
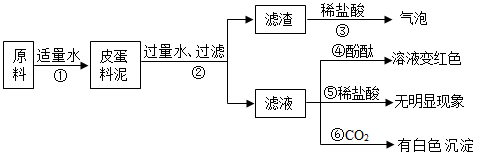
(1)步骤②的操作中,玻璃棒的作用是______ 。
(2)由上述实验现象推断,滤液中的溶质一定含有______ 。
(3)步骤③发生化学反应的方程式______ 。
(4)步骤⑥通入少量二氧化碳生成白色沉淀的化学反应的化学方程式______ 。

(1)步骤②的操作中,玻璃棒的作用是
(2)由上述实验现象推断,滤液中的溶质一定含有
(3)步骤③发生化学反应的方程式
(4)步骤⑥通入少量二氧化碳生成白色沉淀的化学反应的化学方程式
您最近一年使用:0次