稻草秸秆中含有大量的纤维素,通过预处理可以制备纤维素,用于造纸行业。过氧化氢溶液是一种理想的无污染漂白剂。某实验小组对影响过氧化氢漂白稻草纤维素效果的因素进行了探究。
查阅资料:漂白过程中,如果过氧化氢的分解不受控制,会导致无效分解,因此漂白前先在体系中加入3%的硅酸钠溶液为稳定剂,防止无效分解。
进行实验:
实验1:将稻草纤维素进行1次漂白
将预处理后的稻草纤维素与过氧化氢溶液混合,加入质量分数为3%的硅酸钠溶液,再加入质量分数为6%的氢氧化钠溶液调节初始pH值为10~11,保持温度70~75℃,反应时间90分钟,过滤,水洗至中性,45℃烘干,测定其白度。
实验序号 | 稻草纤维素与液体固液比 | 过氧化氢溶液质量分数 | 硅酸钠溶液与过氧化氢溶液的体积比 | 白度 |
1-1 | 1:5 | 5% | 0.5:1 | 36.5 |
1-2 | 1:8 | 5% | 0.5:1 | 46.9 |
1-3 | 1:10 | 5% | 0.5:1 | 52.4 |
实验2:将稻草纤维素进行二段漂白
首先进行第一段漂白:将预处理后的纤维素与质量分数为3%的过氧化氢溶液混合,加入质量分数为3%的硅酸钠溶液,再加入质量分数为6%的氢氧化钠溶液调节初始pH值为10~11,保持温度70~75℃,反应时间60分钟。
然后进行第二段漂白:经过第一段漂白后的纤维素与过氧化氢溶液混合,接着重复实验1的步骤。记录第二段漂白实验结果如下:
实验序号 | 稻草纤维素与液体固液比 | 过氧化氢溶液质量分数 | 硅酸钠溶液与过氧化氢溶液的体积比 | 白度 |
2-1 | 1:5 | 5% | 0.5:1 | 56.9 |
2-2 | 1:8 | 5% | 0.5:1 | 63.3 |
2-3 | 1:10 | 5% | 0.5:1 | 74.3 |
2-4 | 1:10 | 5% | 0 | 37.3 |
2-5 | a | 5% | 0.25:1 | 54.6 |
2-6 | 1:10 | 5% | 0.75:1 | 72.5 |
2-7 | 1:10 | 5% | 1:1 | 72.1 |
解释与结论:
(1)过氧化氢不稳定,易分解,发生反应的化学方程式
(2)实验2中,表格内a处应该填入的数据是
(3)依据实验1-1至1-3,可以得出的结论是
(4)根据实验结果可知,过氧化氢漂白稻草纤维素的最佳条件是:质量分数为3%的硅酸钠溶液与过氧化氢体积比为
反思与评价:
(5)依据实验数据,不能得出“稻草纤维素与液体固液比相同时,分别用3%和5%的过氧化氢溶液进行两段漂白时,质量分数为3%的硅酸钠溶液与过氧化氢溶液的体积比越大,漂白效果越好”的结论,其证据是
相似题推荐
【猜想与假设】

猜想1:Al2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变;
猜想2:Al2O3参与反应并产生O2,反应前后质量和化学性质发生了改变;
猜想3:Al2O3是反应的催化剂,反应前后
【实验设计】用天平称量Al2O3 0.2 g,取5 mL 5%的过氧化氢溶液于试管中,进行如下实验:
(2)步骤①③的目的是
(3)写出Al2O3催化过氧化氢溶液分解产生氧气的文字表达式:
【继续探究】氧化铝是否比二氧化锰的催化效果更好?
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
溶液中有气泡放出带火星的木条复燃 | 称量Al2O3的质量仍为0.2g | 溶液中有大量气泡放出, | 猜想3成立 |
(4)上述实验测量的“待测数据”是
实验序号 | 5%过氧化氩溶液体积 | 催化剂种类及质量 | 待测数据 |
① | 5mL | / | |
② | 5mL | 0.5gAl2O3 | |
③ | 5mL | 0.5gMnO2 |
【注意:若答对以下小题奖励4分,化学试卷总分不超过60分】
【实验反思】
(6)影响过氧化氢溶液分解产生氧气快慢的因素还可能有:
(7)请设计实验验证你的其中一种猜想:
实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中。 ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象。  | A试管中无明显现象 B试管中有 | A试管中的无色液体是: B试管中的无色液体是: |
怎么样检验B试管中气体:
反思:
①李明同学认为B试管能产生大量氧气,是因为过氧化氢溶液与二氧化锰发生了化学反应生成的。你认为这种说法
②你的说法是
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_______(填字母)。
| A.不加入催化剂化学反应就一定不能发生 |
| B.在化学反应前后催化剂的质量和性质都不发生改变 |
| C.用作催化剂的物质还可能是其他反应的反应物或生成物 |
| D.一个化学反应可能有多种催化剂 |
【任务二】探究催化剂
(2)查阅资料发现氧化铜也可以作为过氧化氢分解的催化剂,于是进行相应探究。称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如图所示实验。
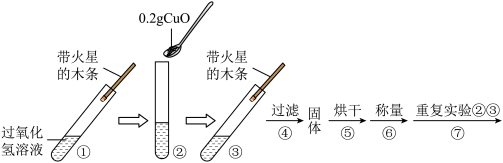
| 步骤①现象 | 步骤⑥结果 | 步骤⑦现象 | 实验结论 |
| 试管中有极少量的气泡产生,带火星的木条没有复燃 | 称得氧化铜的质量为 | 氧化铜是过氧化氢分解反应的催化剂 |
【任务三】探究催化剂的催化效果
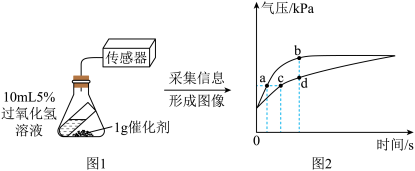
分别取10m 5%过氧化氢溶液、1g 二氧化锰、1g 氧化铜,按图1所示装置进行实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂完全接触,测得相同条件下瓶内气压的变化如图2所示。
(3)对比分析图2中的
(4)请从催化剂的角度解释在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同的原因是
【任务一】了解制氧方法
(1)分子筛制氧法的工作原理如下图,该过程发生的变化属于

(2)某品牌制氧机中有一包白色颗粒和一包黑色粉末,白色颗粒成分为过碳酸钠(化学式为
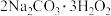 ,它是过氧化氢与碳酸钠的化合物,遇水后放出氧气)。从质量守恒的角度分析,你认为过碳酸钠能够作为制氧剂的原因是
,它是过氧化氢与碳酸钠的化合物,遇水后放出氧气)。从质量守恒的角度分析,你认为过碳酸钠能够作为制氧剂的原因是【任务二】探究过碳酸钠制氧原理
(3)如下图所示,分别取等质量的白色颗粒和等体积的水加入甲、乙两支试管,再向乙试管中加入黑色粉末。观察到甲试管仅有少量气泡,乙试管有大量气泡。

①黑色粉末起
②该制氧机的制氧原理有两步反应,写出第二步的化学方程式。
第一步:
 ;
;第二步:
【任务三】设计简易家用制氧机
(4)同学们设计的简易制氧机,其原理示意图如下图,制氧机工作时,氧气通过装有水的洗气室仍能排出,利用的性质是

(5)制氧机制氧选择过碳酸钠而不选择双氧水的根本原因是______(填字母)。
| A.产物无污染 | B.制取成本更低 | C.运输储存更方便 |
兴趣小组的同学设计并完成了下表所示的探究实验:
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 结论 | 总结 | |||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应慢。 | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | ||
| 实验三 | 二氧化锰能加快过氧化氢的分解 | |||
(1)请你帮小组内的同学填写上表中未填完的空格。
(2)在上述的探究实验中,“实验一”和“实验二”起的作用是
(3)老师认为仅由上述实验还不能完全得出表内的“总结”,她要求同学们补充设计了两个方面的探究实验,最终证明了“二氧化锰是过氧化氢分解的催化剂”。
第一方面的实验操作中包含了两次称量,其目的是:
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验,其实验操作、现象和结论是:
(1)提出问题:小松同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现有大量气泡产生。小松想水泥块是否可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥。
(2)猜想:水泥块可以作过氧化氢分解的催化剂。
(3)实验验证:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管中, | 木条不复燃 | 常温下过氧化氢分解速率很慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 |
讨论:小芳认为:仅凭上述两个实验还不能证明水泥块是过氧化氢分解反应的催化剂,还需要增加一个探究实验:探究是
(4)但小华认为,要证明小松的猜想,小芳的补充实验还是不够,还需要再补充一个实验:该探究是
【查阅资料】
a.水泥负载二氧化锰催化剂是将二氧化锰与水泥按照一定比例混合,加水搅拌制成的一种块状催化剂。
b.可通过测定反应过程中密闭容器的压强变化值来衡量过氧化氢分解速率,压强变化值越大,说明过氧化氢分解速率越快。
【进行实验】
每次实验时均向反应容器中加入5mL过氧化氢溶液并采集相同时间内的压强变化值,记录如下:
| 实验序号 | 过氧化氢溶液浓度/% | 水泥与二氧化锰的质量比 | 水泥负载二氧化锰的质量/g | 压强变化值/kPa |
| ① | 5 | 1:1 | 0.5 | 7.92 |
| ② | 5 | 1:2 | 0.5 | 11.98 |
| ③ | 5 | 1:3 | 0.5 | 15.82 |
| ④ | 8 | 1:2 | 0.5 | 23.26 |
| ⑤ | 11 | 1:2 | 0.5 | 31.47 |
| ⑥ | 5 | 1:2 | 0.3 | 13.22 |
| ⑦ | 5 | 1:2 | 0.1 | 10.78 |
| ⑧ | 5 | 1:2 | 0 | 0.02 |
【解释与结论】
(1)水泥负载二氧化锰属于
(2)水泥负载二氧化锰催化过氧化氢分解的符号表达式为
(3)依据表中数据回答,⑦中压强变化值比⑧大的原因是
(4)对比实验①②③,得出的结论是
(5)探究等体积过氧化氢溶液中,过氧化氢溶液浓度对过氧化氢分解速率的影响的实验是
【反思与评价】
(6)依据表中数据回答,不能得出“过氧化氢溶液浓度、水泥与二氧化锰的质量比相同时,水泥负载二氧化锰的质量越大,过氧化氢分解速率越快”的实验结论,其证据是
(1)兴趣小组的同学发现取回的水样浑浊且有一股臭味.小方提出往水中加入适量的某种物质,搅拌后即可消除臭味,该物质是
(2)通过以上操作,得到的水中可能还含有其他杂质,若想得到纯度较高的水,你认为可选择以下操作中的
A 蒸馏 B 加明矾 C 通入氯气消毒
【查阅资料】明矾[化学式:KA1(SO4)2·12H2O]是一种常见的净水剂,它在水中离解出的离子主要有K+、A13+、SO42- 。
【提出问题】明矾中哪一种离子有净水作用?
【设计实验】小敏进行了如下实验,请填写表中空白
| 实验操作 | 实验现象 | 结论 |
| 在一杯浑浊的水中加入少量KCl,静置 | 烧杯中的水仍然浑浊 | |
| 在一杯浑浊的水中加入少量Al2(SO4)3,静置 | A13+有净水作用 |
【反思】研究表明:河水部分水体污染是由于水中氮、磷含量过高导致水质恶化,水体中氮、磷含量过高的可能原因是
【猜想】苹果可作过氧化氢分解的催化剂
【实验】设计并完成下表所示的探究实验:
| 实验操作 | 实验现象 | 实验结论 | 总结 | |
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是反应速率很慢。 | 苹果可作过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入苹果,伸入带火星的木条 | 没有明显现象 | 水和苹果不能放出氧气 | |
| 实验三 | 取5mL5%的过氧化氢溶液于试管中,加入苹果,伸入带火星的木条 | 苹果能加快过氧化氢的分解速率 |
(2)在小明的探究实验中,“实验一”和“实验二”起的作用是
【反思】小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完全证明猜想是正确的:
第一方面的实验操作中包含了两次称量,其目的是
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。向剩余物中再加入过氧化氢溶液,有大量气泡产生,其目的是:



