化学材料广泛存在和应用于我们的生活中。
(1)请用化学用语填空:
①镁元素______ 。
②2个氢氧根离子______ 。
③地壳中含量最高的元素______ 。
④标出氯酸钾中氯离子的化合价:______ 。
(2)氧化锌广泛用于皮肤病的治疗,工业氧化锌常含有少量杂质(CūO、FeO等)不能直接使用。提纯、净化氧化锌的简易流程如图所示:
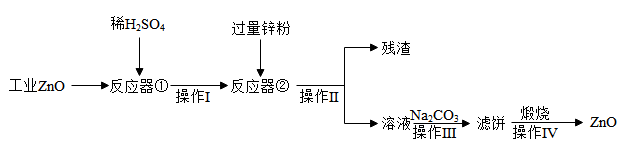
①操作I中,滤纸边缘要______ (填“低于”或“高于”)漏斗边缘。
②残渣中除了金属锌除外,还有______ 。
③滤饼得到氧化锌的化学方程式为:______ 。
(1)请用化学用语填空:
①镁元素
②2个氢氧根离子
③地壳中含量最高的元素
④标出氯酸钾中氯离子的化合价:
(2)氧化锌广泛用于皮肤病的治疗,工业氧化锌常含有少量杂质(CūO、FeO等)不能直接使用。提纯、净化氧化锌的简易流程如图所示:

①操作I中,滤纸边缘要
②残渣中除了金属锌除外,还有
③滤饼得到氧化锌的化学方程式为:
2023·云南曲靖·二模 查看更多[1]
更新时间:2023-05-03 07:07:04
|
相似题推荐
【推荐1】通过化学课程的学习,我们收获很多。
收获一:在宏观、微观和符号之间建立联系是化学学科的特点.
(1)请用合适的化学符号填空:
①用“ ”表示氮原子,则“
”表示氮原子,则“ ”表示
”表示______ ; ②地壳中的元素含量第二的元素_____ ;
③构成硫酸铜的阴离子_________ ; ④氧化铁中铁元素的化合价为+3_______ ;
⑤相对分子质量最小的气体化学式是_____________ 。
(2)物质的组成及构成关系如图1所示,图1中 ①表示的是______ 。

(3)图2是氧、硫、氯三种元素的粒子结构示意图。
①氯离子的结构示意图中x的数值是______ 。
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的______ 相同。
③氧和氯两种元素最本质的区别是它们原子中的______ 不相同。
收获二:我们学会了从微观的角度认识物质及其反应。
(4)下列各图中“ ”“
”“ ”分别表示两种不同元素的原子,其中可能表示氧化物的是
”分别表示两种不同元素的原子,其中可能表示氧化物的是____ 。

(5)某反应前后分子变化的微观示意图如下,下列说法正确的是_________。
 “
“ ”和“
”和“  ”表示不同元素的原子
”表示不同元素的原子
(6)收获三:我们知道常见物质之间存在着一定的转化关系.
A、B、C、D、E、F、G是常见的七种物质。它们的转化关系如下图所示,A、B是组成元素完全相同的两种无色液体,C、D是两种无色气体,E是暗紫色固体,G是黑色固体,试推断:

①写出D、F两种物质的化学式:D________ ,F_________ ;
②G在反应①中起_______ 作用;
③反应②符号表达式为____________ ,产生气体D、C的体积比为_________ 。
收获一:在宏观、微观和符号之间建立联系是化学学科的特点.
(1)请用合适的化学符号填空:
①用“
 ”表示氮原子,则“
”表示氮原子,则“ ”表示
”表示③构成硫酸铜的阴离子
⑤相对分子质量最小的气体化学式是
(2)物质的组成及构成关系如图1所示,图1中 ①表示的是

(3)图2是氧、硫、氯三种元素的粒子结构示意图。
①氯离子的结构示意图中x的数值是
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的
③氧和氯两种元素最本质的区别是它们原子中的
收获二:我们学会了从微观的角度认识物质及其反应。
(4)下列各图中“
 ”“
”“ ”分别表示两种不同元素的原子,其中可能表示氧化物的是
”分别表示两种不同元素的原子,其中可能表示氧化物的是
(5)某反应前后分子变化的微观示意图如下,下列说法正确的是_________。
 “
“ ”和“
”和“  ”表示不同元素的原子
”表示不同元素的原子| A.反应物与生成物共有3种物质 | B.反应后原子的个数增多 |
| C.该图可示意加热氧化汞的反应 | D.该反应属于分解反应 |
A、B、C、D、E、F、G是常见的七种物质。它们的转化关系如下图所示,A、B是组成元素完全相同的两种无色液体,C、D是两种无色气体,E是暗紫色固体,G是黑色固体,试推断:

①写出D、F两种物质的化学式:D
②G在反应①中起
③反应②符号表达式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】(1)1774年,科学家____ 通过用金属汞在空气中加热生成氧化汞(HgO)等实验,第一次明确得出空气是由氧气和氮气组成。
A 诺贝尔 B 张青莲 C 门捷列夫 D 拉瓦锡
(2)下图的微观示意图可简单表示金属汞与氧气反应的过程,请在反应后方框内画出正确的图示_____ 。

(3)如图甲所示是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替乙实验中的水,甲图和乙图中都有的玻璃仪器①的名称为___ ,实验中产生气体的文字表达式为_____ ,与乙相比,甲优点有________ 。

(4)化学兴趣小组知道二氧化锰能作过氧化氢分解的催化剂后
【猜想】Al2O3能作过氧化氢分解的催化剂
请你一起参与他们的探究过程,并填写下列空白。
【实验验证】
(5)过氧化氢(H2O2)中存在过氧根( ),两个数字2的含义分别是
),两个数字2的含义分别是_____ 和____ ,钠离子和过氧根形成的过氧化钠的化学式为_____ 。
A 诺贝尔 B 张青莲 C 门捷列夫 D 拉瓦锡
(2)下图的微观示意图可简单表示金属汞与氧气反应的过程,请在反应后方框内画出正确的图示

(3)如图甲所示是铁丝在氧气中燃烧的改进实验,用适量双氧水和二氧化锰代替乙实验中的水,甲图和乙图中都有的玻璃仪器①的名称为

(4)化学兴趣小组知道二氧化锰能作过氧化氢分解的催化剂后
【猜想】Al2O3能作过氧化氢分解的催化剂
请你一起参与他们的探究过程,并填写下列空白。
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 木条不复燃 | 过氧化氢分解缓慢 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量A12O3,然后将带火星的木条伸入试管中 | 产生大量气泡,木条复燃 |
(5)过氧化氢(H2O2)中存在过氧根(
 ),两个数字2的含义分别是
),两个数字2的含义分别是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】过氧化镁( )是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[
)是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[ ]制备过氧化镁的过程如图所示。
]制备过氧化镁的过程如图所示。 和
和 常温下比较稳定,加热时容易发生分解;
常温下比较稳定,加热时容易发生分解;
ⅱ、MgO与 反应放出大量的热。
反应放出大量的热。
(1) 中氢、氧原子的个数比为
中氢、氧原子的个数比为______ 。
(2) 煅烧时分解生成三种氧化物,分别为MgO和
煅烧时分解生成三种氧化物,分别为MgO和______ 、______ (填化学式)。
(3)反应2的化学方程式为 。用40gMgO,理论上可制备
。用40gMgO,理论上可制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)
(4)加入稳定剂的目的是______ 。
 )是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[
)是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[ ]制备过氧化镁的过程如图所示。
]制备过氧化镁的过程如图所示。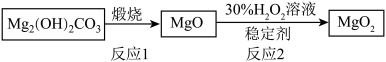
 和
和 常温下比较稳定,加热时容易发生分解;
常温下比较稳定,加热时容易发生分解;ⅱ、MgO与
 反应放出大量的热。
反应放出大量的热。(1)
 中氢、氧原子的个数比为
中氢、氧原子的个数比为(2)
 煅烧时分解生成三种氧化物,分别为MgO和
煅烧时分解生成三种氧化物,分别为MgO和(3)反应2的化学方程式为
 。用40gMgO,理论上可制备
。用40gMgO,理论上可制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)(4)加入稳定剂的目的是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】为了比较镁、铜、铁三种金属的活动性强弱,兴趣小组的同学用这三种金属分别与稀硫酸和硝酸银溶液反应。
(1)能否根据镁、铜、铁与硝酸银溶液反应的结果来判断三种金属的活动性强弱?_________ (选填“能”或“不能”),写出铜和硝酸银溶液反应的化学方程式______________ 。
(2)金属锌、铜、铁的活动性由强到弱的顺序是_________________ 。(用元素符号表示)
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是在高温下,铝与氧化铁反应得到熔融的铁与一种氧化物。该反应的化学方程式为_______________ 。
(4)将一定量的镁粉加入到硝酸银、硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生,则下列叙述中完全正确的组合是______________ 。
①滤渣中一定含有银,一定不含有铜
②滤液中的溶质一定含有硝酸镁,一定不含有硝酸银
③若滤液为蓝色,则滤液中的溶质一定含有硝酸铜和硝酸镁
④若滤液为无色,则滤渣中一定含有银和铜,滤液中的溶质一定只含有硝酸锌
A.①② B.②③ C.③④ D.①④
(1)能否根据镁、铜、铁与硝酸银溶液反应的结果来判断三种金属的活动性强弱?
(2)金属锌、铜、铁的活动性由强到弱的顺序是
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是在高温下,铝与氧化铁反应得到熔融的铁与一种氧化物。该反应的化学方程式为
(4)将一定量的镁粉加入到硝酸银、硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸无气泡产生,则下列叙述中完全正确的组合是
①滤渣中一定含有银,一定不含有铜
②滤液中的溶质一定含有硝酸镁,一定不含有硝酸银
③若滤液为蓝色,则滤液中的溶质一定含有硝酸铜和硝酸镁
④若滤液为无色,则滤渣中一定含有银和铜,滤液中的溶质一定只含有硝酸锌
A.①② B.②③ C.③④ D.①④
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】金属材料与人类的生产和生活密切相关。
(1)为防止钢铁锈蚀,常在其表面涂油漆或镀上其他金属,这些方法能防止钢铁锈蚀的原因是______ 。
(2)在古代,常常用“湿法炼铜”或“火法炼铜”。“湿法炼铜”的原理是:“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。“湿法炼铜”的反应类型为______ ,“火法炼铜”的化学方程式是______ 。
(3)某化学兴趣小组的同学想从含有A1 2(SO4)3、CuSO4的废液中回收金属铜,设计了如下实验。

步骤II中加入过量的稀硫酸的目的是______ , 写出该步骤反应的化学方程式______ 。
(4)已知锌和锌的化合物存在以下转换关系: ,
, ,
,
计算:198g Zn(OH)2理论上能得到Zn的质量为______ g。
(1)为防止钢铁锈蚀,常在其表面涂油漆或镀上其他金属,这些方法能防止钢铁锈蚀的原因是
(2)在古代,常常用“湿法炼铜”或“火法炼铜”。“湿法炼铜”的原理是:“曾青(硫酸铜溶液)得铁则化为铜”;“火法炼铜”中用辉铜矿(主要成分Cu2S)炼铜的原理是:Cu2S与氧气在高温条件下反应生成铜和一种会导致酸雨的气体(其相对分子质量为64)。“湿法炼铜”的反应类型为
(3)某化学兴趣小组的同学想从含有A1 2(SO4)3、CuSO4的废液中回收金属铜,设计了如下实验。

步骤II中加入过量的稀硫酸的目的是
(4)已知锌和锌的化合物存在以下转换关系:
 ,
, ,
,计算:198g Zn(OH)2理论上能得到Zn的质量为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】金属文物的锈蚀在一定程度上阻碍了我们对古代文明的追溯、对优秀文化的传承。
已知:Cu2(OH)3Cl是一种典型的有害锈,人们发现青铜器在含有氯离子的环境中易生成CuCl,CuCl在过量水的作用下生成Cu2O,随着环境条件的变化而发生锈蚀。青铜器表面的锈分为2种:无害锈能保护青铜器,有害锈则会使其受损加剧并不断扩散。
(1)有害锈会使青铜器受损加剧,是因为其具有疏松多孔的结构,具有_____ 性。
(2)Cu2O与H2O、O2、HCl发生化合反应生成Cu2(OH)3Cl,该反应的化学方程式为____ 。
(3)青铜器表面的绿色物质是铜绿,主要成分是Cu2(OH)3Cl3,铜制品在空气中能与空气中的H2O、CO2和____ 反应生成铜绿。
(4)为了有效保护锈蚀的青铜器,第一步需清洗,常用蒸馏水而不选用自来水反复漂洗,从而能够有效避免有害锈的生成,其原因是自来水中可能含有少量的______ (填化学用语)。
(5)我国古代青铜器制造工艺的全过程可以概括为三个主要程序:勘探原料、冶炼精铜、浇铸成器。现代工业上以孔雀石为原料提取Cu的主要转化过程如下。

①孔雀石可将Cu2(OH)2CO3固体从碱浸液中分离出来的操作I为_______ 。
②酸浸步骤中加入足量酸的目的是____ 。
③电解CuSO4溶液可制得Cu、H2SO4和O2。该反应是将电能转化为_______ ,其反应化学方程式为______ 。结合流程、以及电解CuSO4溶液的原理分析可知,能够实现资源化循环利用的物质是______ (填化学式)。
④若孔雀石中Cu2(OH)2CO3的质量分数为88.8%,取100t孔雀石进行反应,计算理论上可制得Cu的质量____ (写出计算过程)。
已知:Cu2(OH)3Cl是一种典型的有害锈,人们发现青铜器在含有氯离子的环境中易生成CuCl,CuCl在过量水的作用下生成Cu2O,随着环境条件的变化而发生锈蚀。青铜器表面的锈分为2种:无害锈能保护青铜器,有害锈则会使其受损加剧并不断扩散。
(1)有害锈会使青铜器受损加剧,是因为其具有疏松多孔的结构,具有
(2)Cu2O与H2O、O2、HCl发生化合反应生成Cu2(OH)3Cl,该反应的化学方程式为
(3)青铜器表面的绿色物质是铜绿,主要成分是Cu2(OH)3Cl3,铜制品在空气中能与空气中的H2O、CO2和
(4)为了有效保护锈蚀的青铜器,第一步需清洗,常用蒸馏水而不选用自来水反复漂洗,从而能够有效避免有害锈的生成,其原因是自来水中可能含有少量的
(5)我国古代青铜器制造工艺的全过程可以概括为三个主要程序:勘探原料、冶炼精铜、浇铸成器。现代工业上以孔雀石为原料提取Cu的主要转化过程如下。

①孔雀石可将Cu2(OH)2CO3固体从碱浸液中分离出来的操作I为
②酸浸步骤中加入足量酸的目的是
③电解CuSO4溶液可制得Cu、H2SO4和O2。该反应是将电能转化为
④若孔雀石中Cu2(OH)2CO3的质量分数为88.8%,取100t孔雀石进行反应,计算理论上可制得Cu的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】某化学兴趣小组欲探究实验室氧化铜和稀硫酸反应后某剩余废液的溶质成分,其实验步骤及对应实验现象如图一所示:______ (填化学式)。
(2)实验中加入NaOH溶液的溶质质量分数均为10%。在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答:
①由图二可知,OA段反应过程没有沉淀生成,该过程对应图一中的步骤______ (选填“a”、“b”、“c”之一)。
②当滴入10%的NaOH溶液160g时(至图中C点)。烧杯中溶液里一定大量存在的阴离子是______ (写离子符号)。
③当滴入10%的NaOH溶液120g时(即图中B点),试通过计算,求生成沉淀的质量______ (写出计算过程,计算结果精确到0.1)。


(2)实验中加入NaOH溶液的溶质质量分数均为10%。在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答:
①由图二可知,OA段反应过程没有沉淀生成,该过程对应图一中的步骤
②当滴入10%的NaOH溶液160g时(至图中C点)。烧杯中溶液里一定大量存在的阴离子是
③当滴入10%的NaOH溶液120g时(即图中B点),试通过计算,求生成沉淀的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】某硫酸厂以黄铁矿(主要成分是 FeS2)为主要原料,生产硫酸的简要流程图如图:

(1)实验室里稀释浓硫酸的方法:把浓硫酸沿烧杯内壁注入水中,并用______ 不断搅拌。
(2)沸腾炉中发生反应的化学方程式为______ 。
(3)沸腾炉中的炉渣(Fe2O3)可用于炼铁,写出用一氧化碳和炉渣炼铁的化学方程式:______ 。
(4)现将质量分数为9.8%的稀硫酸逐滴滴加到盛有20g炉渣(主要成分Fe2O3)的烧杯中、烧杯中固体的质量与加入稀硫酸的质量的关系如图所示。

①反应过程中的现象有______ (填一种即可)。
②当滴加稀硫酸至200g时,烧杯中溶液里的溶质是______ (写化学式)。
③试通过计算求出20g炉渣中所含Fe2O3的质量分数______ 。

(1)实验室里稀释浓硫酸的方法:把浓硫酸沿烧杯内壁注入水中,并用
(2)沸腾炉中发生反应的化学方程式为
(3)沸腾炉中的炉渣(Fe2O3)可用于炼铁,写出用一氧化碳和炉渣炼铁的化学方程式:
(4)现将质量分数为9.8%的稀硫酸逐滴滴加到盛有20g炉渣(主要成分Fe2O3)的烧杯中、烧杯中固体的质量与加入稀硫酸的质量的关系如图所示。

①反应过程中的现象有
②当滴加稀硫酸至200g时,烧杯中溶液里的溶质是
③试通过计算求出20g炉渣中所含Fe2O3的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】家庭厨房就是一个化学小世界,包含着许多的化学知识。请回答问题。
一、厨房里离不开水。
(1)下图中用“ ”表示氧原子,用“
”表示氧原子,用“ ”表示氢原子。下列选项中可以表示水分子的是
”表示氢原子。下列选项中可以表示水分子的是______ (填字母序号,下同 )

(2)用下图装置将水通电一段时间后能产生气体,则此时发生反应的化学方程式为______ 。厨房中烧水也可以将水变成气体,请从微观角度解释这两种变化的本质区别。______

(3)下列能证明水是由氧元素和氢元素组成的实验是______
A 水的净化
B 水的蒸发
C 氢气在氧气中燃烧生成水
二、下列厨房用品所用的主要材料中,属于金属材料的是_____ (填字母序号,下同 ),其中利用金属导热性的是______ 。

三、厨房里离不开燃料,燃料燃烧产生热量为我们所用。
(1) 化石燃料是当前人类的主要燃料,包括煤、______ 和天然气。
(2) 写出天然气燃烧的化学方程式。______
(3)化石能源是有限的,我们在合理利用的同时,要努力开发新能源。请写出一种你所知道的新能源_______ 。
(4) 炒菜时,油锅着火,盖上锅盖即可灭火,原因是______ 。
四、下表列出了两种家用清洁剂的功能、有效成分和注意事项。
据表回答下列问题:
(1) “洁厕灵”勿用于铁制品清洁的理由是______ (用化学方程式表示)。
(2)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为NaClO + 2HCl = NaCl + X个+ H2O,则X的化学式为______ ;NaC1O中氯元素的化合价为______ 。
一、厨房里离不开水。
(1)下图中用“
 ”表示氧原子,用“
”表示氧原子,用“ ”表示氢原子。下列选项中可以表示水分子的是
”表示氢原子。下列选项中可以表示水分子的是
(2)用下图装置将水通电一段时间后能产生气体,则此时发生反应的化学方程式为

(3)下列能证明水是由氧元素和氢元素组成的实验是
A 水的净化
B 水的蒸发
C 氢气在氧气中燃烧生成水
二、下列厨房用品所用的主要材料中,属于金属材料的是

三、厨房里离不开燃料,燃料燃烧产生热量为我们所用。
(1) 化石燃料是当前人类的主要燃料,包括煤、
(2) 写出天然气燃烧的化学方程式。
(3)化石能源是有限的,我们在合理利用的同时,要努力开发新能源。请写出一种你所知道的新能源
(4) 炒菜时,油锅着火,盖上锅盖即可灭火,原因是
四、下表列出了两种家用清洁剂的功能、有效成分和注意事项。
| 名称 | 洁厕灵 | 漂白精 |
| 功能 | 有效清除污垢,除异味 | 快速漂除衣物污渍 |
| 有效成分 | HCl | NaCIO |
| 注意事项 | 勿用于铁、铝等金属制品清洁 | 勿与酸性制品或其他清洁产品混合使用 |
(1) “洁厕灵”勿用于铁制品清洁的理由是
(2)“洁厕灵”与“漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为NaClO + 2HCl = NaCl + X个+ H2O,则X的化学式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两个化学研究小组的同学对金属铜及其化合物的性质进行了一系列的研究。
Ι.甲组同学收集了一些废铜屑。他们欲用这些废铜屑制取硫酸铜,设计了如下两个方案:
方案1:Cu→O2→CuO CuSO4
CuSO4
方案2:Cu CuSO4[已知Cu+2H2SO4(浓)
CuSO4[已知Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O]
CuSO4+SO2↑+2H2O]
(1)方案1中氧化铜与稀硫酸的化学反应,属于_______ 反应类型(填“化合”、“分解”、“置换”、“复分解”之一)。
(2)从绿色化学的观点出发,上述两个方案中,你认为比较合理的是方案____ (填“1”或“2”)。
Ⅱ.乙组同学利用甲组同学制取的硫酸铜溶液反应制取氢氧化铜。
取一定量的硫酸铜溶液放入烧杯中,逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。

(3)滴入上述NaOH溶液至B点时,溶液中溶质是_______ (填写化学式)。
(4)当滴入上述NaOH溶液至A点时,试通过计算,所得氢氧化铜沉淀的质量(计算结果精确至0.1g)。
Ι.甲组同学收集了一些废铜屑。他们欲用这些废铜屑制取硫酸铜,设计了如下两个方案:
方案1:Cu→O2→CuO
 CuSO4
CuSO4方案2:Cu
 CuSO4[已知Cu+2H2SO4(浓)
CuSO4[已知Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O]
CuSO4+SO2↑+2H2O](1)方案1中氧化铜与稀硫酸的化学反应,属于
(2)从绿色化学的观点出发,上述两个方案中,你认为比较合理的是方案
Ⅱ.乙组同学利用甲组同学制取的硫酸铜溶液反应制取氢氧化铜。
取一定量的硫酸铜溶液放入烧杯中,逐滴加入10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液质量的关系曲线如图所示。

(3)滴入上述NaOH溶液至B点时,溶液中溶质是
(4)当滴入上述NaOH溶液至A点时,试通过计算,所得氢氧化铜沉淀的质量(计算结果精确至0.1g)。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】项目式学习能助力五育并举。化学兴趣小组开展制备醋酸钙【(CH3COO)2Ca,相对分子质量为158】的项目式学习活动。
【活动一】寻找反应原理
根据复分解反应的原理,能生成醋酸钙的物质组合可能是:①醋酸与氧化钙反应;②醋酸与_____ 反应;③醋酸与碳酸钙反应。
小组同学一致认为组合③更好。因为该反应有________ 产生,现象明显,便于判断反应是否结束。
【活动二】定量计算药品用量
现需要制备15.8g醋酸钙,需要碳酸钙的质量是__ ?(请写出计算过程)
[已知:CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑]
通过计算,需要量取冰醋酸___ mL(保留到小数点后一位)。
【活动三】制作与反思
将上述量取的冰醋酸稀释成质量分数为20%的溶液,然后再加入所需的碳酸钙,充分反应后,通过蒸发结晶,共得到17.6g醋酸钙固体。小组同学发现,与理论值15.8g不相符,请分析可能的原因__ 。
【活动一】寻找反应原理
根据复分解反应的原理,能生成醋酸钙的物质组合可能是:①醋酸与氧化钙反应;②醋酸与
小组同学一致认为组合③更好。因为该反应有
【活动二】定量计算药品用量
现需要制备15.8g醋酸钙,需要碳酸钙的质量是
[已知:CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑]
通过计算,需要量取冰醋酸
| 冰醋酸 (又名无水乙酸) 溶质质量分数 98% 密 度 1.05g/mL |
将上述量取的冰醋酸稀释成质量分数为20%的溶液,然后再加入所需的碳酸钙,充分反应后,通过蒸发结晶,共得到17.6g醋酸钙固体。小组同学发现,与理论值15.8g不相符,请分析可能的原因
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】酸、碱、盐是重要的化学物质。在生活、生产和科学实验中用途广泛。
(1)向盛有澄清石灰水(滴有酚酞溶液)的烧杯中倒入一定量的盐酸,观察到烧杯中的溶液由红色变为无色(氯化钙溶液显中性)。为了确定其中溶质的成分,不可选用的试剂为______。
(2)因稀盐酸和稀硫酸中都含有______ ,故它们具有相似的化学性质;但也因为构成不同,它们具有不同的化学性质,请举一个例子,说明它们具有不同的化学性质______ 。
(3)根据下图回答问题。

①标号为a的仪器名称是______ 。
②实验室用过氧化氢溶液与二氧化锰混合制取氧气,应选择的气体发生装置是______ ,该反应的化学方程式为______ 。
③利用D装置采用排空气法收集氢气,从导气管______ 通入气体。
(4)碘元素对青少年智力发育影响较大,加碘盐通常在食盐中加碘酸钾(KIO3)。取未加碘的纯净食盐5.85克配成100毫升溶液,滴入足量的硝酸银溶液,最多可以从沉淀物中获得多少克新盐?
(1)向盛有澄清石灰水(滴有酚酞溶液)的烧杯中倒入一定量的盐酸,观察到烧杯中的溶液由红色变为无色(氯化钙溶液显中性)。为了确定其中溶质的成分,不可选用的试剂为______。
| A.二氧化碳 | B.铁 | C.碳酸钠 | D.氧化铜 |
(2)因稀盐酸和稀硫酸中都含有
(3)根据下图回答问题。

①标号为a的仪器名称是
②实验室用过氧化氢溶液与二氧化锰混合制取氧气,应选择的气体发生装置是
③利用D装置采用排空气法收集氢气,从导气管
(4)碘元素对青少年智力发育影响较大,加碘盐通常在食盐中加碘酸钾(KIO3)。取未加碘的纯净食盐5.85克配成100毫升溶液,滴入足量的硝酸银溶液,最多可以从沉淀物中获得多少克新盐?
您最近一年使用:0次



