金属锂(Li)在航空航天、电池等领域有广泛应用。已知锂与镁的化学性质相似,氯化锂(LiCl)易溶于水。
(1)我国“天问一号”火星探测器的制造中应用了新型镁锂合金材料。下列说法正确的是_______(填标号)。
(2)神舟十四号航天员出舱活动时身着的航天服,采用氢氧化锂来吸收航天员呼出的CO2,该反应的化学方程式为_______ 。
(3)用三种不同方法制备氯化锂(要求含锂原料分别属于不同类别物质),写出预期反应的化学方程式:
①用硫酸锂溶液作为其中一种原料来制备氯化锂,反应的化学方程式为_______ ,反应前后没有减少的离子是_______ (填离子符号)。
②_______ ,依据的反应规律是_______ 。
③_______ 。
(1)我国“天问一号”火星探测器的制造中应用了新型镁锂合金材料。下列说法正确的是_______(填标号)。
| A.镁锂合金是一种新型化合物 | B.镁是地壳中含量最高的金属元素 |
| C.镁锂合金中,原子之间存在间隔 | D.镁锂合金的硬度比镁大 |
(3)用三种不同方法制备氯化锂(要求含锂原料分别属于不同类别物质),写出预期反应的化学方程式:
①用硫酸锂溶液作为其中一种原料来制备氯化锂,反应的化学方程式为
②
③
2023·广东广州·一模 查看更多[2]
更新时间:2023-05-05 20:42:19
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
真题
【推荐1】A~I均为初中化学常见物貭,它们之间的转化关系如下图,部分产物已略去。已知A是人体胃酸的主要成分,B是大理石的主要成分,D为液体,F为气体,I能与A反应生成个数比为1:2的+2价、+3价铁盐。
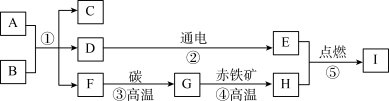
(1)写出下列物质的化学式C________ 、H_________ 。
(2)上述①②③④⑤中属于化合反应的是________ 、属于分解反应的是________
(3)写出G→H的化学反应方程式________ 。
(4)写出I和A反应的化学反应方程式________ 。

(1)写出下列物质的化学式C
(2)上述①②③④⑤中属于化合反应的是
(3)写出G→H的化学反应方程式
(4)写出I和A反应的化学反应方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】研究人员提出了一种基于锂元素(Li)的电化学过程来合成氨的方法,其工艺流程如图所示,请据此回答问题。

(1)应①利用太阳能光伏发电电解氢氧化锂固体。通电后氢氧化锂发生分解,在正极上有氧气和水产生,负极上析出银白色金属锂。根据上述信息,将反应中正极附近生成物微粒的示意图补充完整(要求体现反应中微粒数目的最简整数比,但不考虑生成物以外的物质)。

(2)反应②是高温条件下发生的化合反应,该反应的化学方程式为_____ 。
(3)反应③中参加反应的 和生成的
和生成的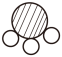 的分子个数比为
的分子个数比为_____ 。
(4)关于该项工艺流程设计的说法中,正确的是_____ (填标号)。
a.该流程可生产氮肥
b.该设计利用了太阳能,减少了环境污染
c.LiOH和O2可在该流程中循环利用
d.该流程的总反应方程式是

(1)应①利用太阳能光伏发电电解氢氧化锂固体。通电后氢氧化锂发生分解,在正极上有氧气和水产生,负极上析出银白色金属锂。根据上述信息,将反应中正极附近生成物微粒的示意图补充完整(要求体现反应中微粒数目的最简整数比,但不考虑生成物以外的物质)。

(2)反应②是高温条件下发生的化合反应,该反应的化学方程式为
(3)反应③中参加反应的
 和生成的
和生成的 的分子个数比为
的分子个数比为(4)关于该项工艺流程设计的说法中,正确的是
a.该流程可生产氮肥
b.该设计利用了太阳能,减少了环境污染
c.LiOH和O2可在该流程中循环利用
d.该流程的总反应方程式是

您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】下图A~F是初中化学中常见的物质,其中B、C常温下是气体,且组成元素相同,C是绿色植物进行光合作用必不可少的气体,X和Y能发生中和反应。F是厨房常见的调味品之一(图中反应条件和部分反应物、生成物已省略)
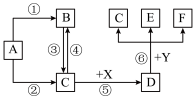
请回答下列问题:
(1)物质C的化学式是_______ ,物质D的俗称_______
(2)若B转化成C是化合反应,则反应的化学方程式为_______ 。
(3)写出X与Y反应的化学方程式_______ 。

请回答下列问题:
(1)物质C的化学式是
(2)若B转化成C是化合反应,则反应的化学方程式为
(3)写出X与Y反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】下图为高炉冶铁、炼钢并用生产的钢来探究白铜成分的流程图。(已知硫酸镍的化学式为NiSO4)

(1)用高炉冶铁的主要反应原理是________ (用化学方程式表示)
(2)分析流程图,三脱装置中发生反应的基本反应类型是______ 。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中_____ (填一种仪器的名称)的作用。
(4)铁与镍相比,铁的金属活动性______ 镍(选填“>”、“=”或“<”),判断依据是____ (用化学方程式表示)。
(5)通过以上信息,得出白铜的成分是_____ ,其硬度和抗腐蚀性比纯铜______ (填“大”或“小”)。

(1)用高炉冶铁的主要反应原理是
(2)分析流程图,三脱装置中发生反应的基本反应类型是
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中
(4)铁与镍相比,铁的金属活动性
(5)通过以上信息,得出白铜的成分是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】金属材料应用广泛,以下是有关金属的工艺及利用。
(1)《天工开物》中记载“凡红铜(纯铜)升黄(黄铜)而后熔化造器”,由此可知黄铜的熔点比纯铜______ (填“高”或“低”)。
(2)古代铁制品“烤蓝”是防止铁制品锈蚀的措施之一。现今将油漆均匀的涂抹在铁制品外表也能起到防锈的作用,其防锈原理是______ 。
(3)湿法冶金:为从含有硝酸银和硝酸镁的废液中回收银,向废液中加入一定量铁粉与铜粉,充分反应后过滤,得到滤渣和滤液。下列说法正确的是______。
(4)定量计算:质量守恒定律的发现使得化学科学由定性研究走向定量研究。在托盘天平两端分别放质量相同且盛有等质量等溶质质量分数的稀硫酸的烧杯,再向两个烧杯中分别加入等质量的锌粒和铜铝合金,充分反应后酸都有剩余,天平保持平衡,则铜铝合金中铜、铝的质量比为______ 。
(1)《天工开物》中记载“凡红铜(纯铜)升黄(黄铜)而后熔化造器”,由此可知黄铜的熔点比纯铜
(2)古代铁制品“烤蓝”是防止铁制品锈蚀的措施之一。现今将油漆均匀的涂抹在铁制品外表也能起到防锈的作用,其防锈原理是
(3)湿法冶金:为从含有硝酸银和硝酸镁的废液中回收银,向废液中加入一定量铁粉与铜粉,充分反应后过滤,得到滤渣和滤液。下列说法正确的是______。
| A.若向滤渣中加入稀盐酸,没有气泡生成,则滤渣中只有Ag |
| B.若滤液为有色溶液,则滤液中至少有2种金属阳离子 |
| C.向滤液中滴加稀盐酸,若产生白色沉淀,则滤液中一定有镁离子、银离子、铁离子,也可能有铜离子 |
| D.所得滤液质量一定比原溶液的质量小 |
(4)定量计算:质量守恒定律的发现使得化学科学由定性研究走向定量研究。在托盘天平两端分别放质量相同且盛有等质量等溶质质量分数的稀硫酸的烧杯,再向两个烧杯中分别加入等质量的锌粒和铜铝合金,充分反应后酸都有剩余,天平保持平衡,则铜铝合金中铜、铝的质量比为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】金属在当前科技、生产中应用广泛。
(1)我国自行研发的大型客机选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度______ 填“大于”或“小于”) 纯铝。
(2)“曾青得铁则化为铜”,将一定量的铁粉放入硫酸铜溶液中,充分反应后,烧杯内一定含有的固体是______ (3)钼矿的主要成分是 MoS2,某小组模拟化工生产设计了如下制备金属钼的流程图。

①将灼烧钼矿的化学方程式配平完整:
_____ MoS2+______ O2
______ MoO3+______ SO2
②SO2 化学性质与二氧化碳有相似之处,可用_________ 溶液吸收灼烧中产生的尾气。
③操作 1 和操作 2 的名称是________ 。
④写出钼酸铵溶液与盐酸发生复分解反应的化学方程式____________
(1)我国自行研发的大型客机选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度
(2)“曾青得铁则化为铜”,将一定量的铁粉放入硫酸铜溶液中,充分反应后,烧杯内一定含有的固体是

①将灼烧钼矿的化学方程式配平完整:

②SO2 化学性质与二氧化碳有相似之处,可用
③操作 1 和操作 2 的名称是
④写出钼酸铵溶液与盐酸发生复分解反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】A~E是初中常见的物质:氢氧化钠、盐酸、氢氧化钙、碳酸钠、二氧化碳中的某一种.A可用于金属表面除锈,B可用来改良酸性土壤,固体C在空气中易潮解。它们相互间发生反应或转化的关系如图所示(“﹣”表面两种物质间能发生反应,“→”表示两种物质间的转化关系)。

(1)A、C的化学式分别为____________ 、 ______________ ;D在生活和生产中的一种用途是 _____________ ;
(2)E→D反应的化学方程式为___________________ ;
C与D反应的化学方程式为________________________ 。

(1)A、C的化学式分别为
(2)E→D反应的化学方程式为
C与D反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】A、B、C、D、E、F均含同一种元素,它们之间的转化关系如图(部分物质已略去)。A是目前世界年产量最高的金属,D属于氧化物,氧元素质量分数为30%,F为红褐色的物质。

B的化学式为____ ;D→E的化学方程式为_______ ;C与氧气、水发生化合反应生成F,该反应的化学方程式为________________ 。

B的化学式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】以二氧化硫尾气、石灰石、空气、碳酸氢铵、氨气和KCl等为原料可以合成有重要应用价值的硫酸钾等物质。合成流程如下图所示:

(1)上述流程中可循环使用的物质是_________ 。
(2)写出反应II的总反应的化学方程式:________________ 。

(1)上述流程中可循环使用的物质是
(2)写出反应II的总反应的化学方程式:
您最近一年使用:0次
【推荐2】A~F是初中化学常见物质,它们的相互转化关系如图所示,其中E是紫红色金属,G是密度最小的气体,J是常用的溶剂,H由三种元素组成,A、B、C、D为不同类别的物质.请回答以下问题。________________ 。
(2)反应②的基本反应类型为________ 。
(3)反应④无明显现象,需要加入________ 才能判断反应是否发生。
(4)C的一种用途________________ 。

(2)反应②的基本反应类型为
(3)反应④无明显现象,需要加入
(4)C的一种用途
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】有一包白色固体样品,可能由NaOH、CaCO3、BaCl2、MgCl2中的一种或几种物质组成,为探究该榉品的组成,某小组取量样品进行如下试验:
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,有白色不溶物产生。
步骤Ⅱ:取步骤Ⅰ的白色不溶物,加入足最稀盐酸,固体完全溶解,且有气泡产生。
步骤Ⅲ:取少量步骤Ⅰ所得的无色滤液,通入二氧化碳气体,有白色沉淀生成。
【查阅资料】CO2不能直接与BaCl2成MgCl2发生反应。
请回答下列问题:
(1)步骤Ⅱ产生气体的化学方程式为______ 。步骤Ⅲ可以确定该白色固体样品一定含有______ 。(填化学式)
(2)若要进一步确定样品的成分,还需进行的实验操作是______ 。
步骤Ⅰ:取少量样品于烧杯中,加足量水,充分搅拌,有白色不溶物产生。
步骤Ⅱ:取步骤Ⅰ的白色不溶物,加入足最稀盐酸,固体完全溶解,且有气泡产生。
步骤Ⅲ:取少量步骤Ⅰ所得的无色滤液,通入二氧化碳气体,有白色沉淀生成。
【查阅资料】CO2不能直接与BaCl2成MgCl2发生反应。
请回答下列问题:
(1)步骤Ⅱ产生气体的化学方程式为
(2)若要进一步确定样品的成分,还需进行的实验操作是
您最近一年使用:0次




