某探究小组同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定。取50g废水于烧杯中,加入足量BaCl2溶液,过滤、洗涤、干燥,得BaSO4固体11.65g。请回答:
(1)50g废水中H2SO4的质量是多少?(写出计算过程)
(2)若改用NaOH溶液来测定50g废水中H2SO4的含量,测定结果会______ (选填“偏低”“偏高”或“不变”)。
(1)50g废水中H2SO4的质量是多少?(写出计算过程)
(2)若改用NaOH溶液来测定50g废水中H2SO4的含量,测定结果会
更新时间:2023-05-22 06:44:39
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】超氧化钾又称为“化学氧自救器”,主要用于煤矿井下救急,其涉及的化学反应方程式为: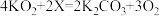 ,请回答:
,请回答:
(1)X的化学式为_______________ 。
(2)若产生9.6kg氧气,理论上需要消耗超氧化钾的质量(写出计算过程)。
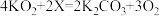 ,请回答:
,请回答:(1)X的化学式为
(2)若产生9.6kg氧气,理论上需要消耗超氧化钾的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】小潘同学为了测定大理石样品中碳酸钙的含量,将100g足量的稀盐酸加入装有20g大理石粉末的烧杯中(杂质不与盐酸反应),同时测量2分钟内烧杯中物质总质量的变化情况(不考虑气体残留),结果如下表所示:
(1)根据以上数据知生成二氧化碳的质量为______ g。
(2)计算大理石样品中碳酸钙的质量分数。
| 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| 烧杯中物质总质量(g) | 120 | 117.6 | 115.8 | 114.4 | 113.4 | 113.4 | 113.4 |
(2)计算大理石样品中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】某化工实验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液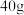 ,洗涤后的溶液呈中性;
,洗涤后的溶液呈中性;
(1)请问所消耗的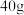 氢氧化钠溶液中溶质的质量为
氢氧化钠溶液中溶质的质量为___ g;
(2)这一定量石油产品中含 的质量是多少?(按格式要求写出计算过程)
的质量是多少?(按格式要求写出计算过程)
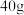 ,洗涤后的溶液呈中性;
,洗涤后的溶液呈中性;(1)请问所消耗的
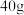 氢氧化钠溶液中溶质的质量为
氢氧化钠溶液中溶质的质量为(2)这一定量石油产品中含
 的质量是多少?(按格式要求写出计算过程)
的质量是多少?(按格式要求写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】一定质量溶质质量分数为10%氢氧化钠溶液和100g溶质质量分数为49%的稀硫酸恰好完全反应。求:(1)消耗氢氧化钠溶液的质量;(2)反应后所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】向一定质量的CuSO4溶液中逐滴加入NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示:

(1)完全反应后,产生沉淀的质量是 g。
(2)计算所加NaOH溶液的溶质质量分数。
(温馨提示:CuSO4+2NaOH = Cu(OH)2↓+Na2SO4)

(1)完全反应后,产生沉淀的质量是 g。
(2)计算所加NaOH溶液的溶质质量分数。
(温馨提示:CuSO4+2NaOH = Cu(OH)2↓+Na2SO4)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取硫酸钠和氯化钠的混合物23.3g,加入100g水使其完全溶解,再加入100g氯化钡溶液恰好完全反应,过滤,得200g滤液(不考虑实验过程中质量的损失)。计算:
(1)该混合物中硫酸钠的质量分数(计算结果精确到0.1%);
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
(1)该混合物中硫酸钠的质量分数(计算结果精确到0.1%);
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
您最近一年使用:0次

 )俗称酒精,可通过高粱、玉米和薯类等发酵、蒸馏而得到。乙醇在空气中燃烧时放出大量的热,其化学方程式为:
)俗称酒精,可通过高粱、玉米和薯类等发酵、蒸馏而得到。乙醇在空气中燃烧时放出大量的热,其化学方程式为: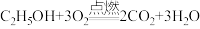 。燃烧
。燃烧 酒精,理论上可生成多少克二氧化碳?
酒精,理论上可生成多少克二氧化碳?
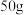 于烧杯中,向其中逐滴滴加溶质质量分数为
于烧杯中,向其中逐滴滴加溶质质量分数为 的盐酸溶液,同时测得其
的盐酸溶液,同时测得其 变化与加入盐酸的质量关系如图所示。
变化与加入盐酸的质量关系如图所示。



