往盛有4.0g久置的铝片的烧杯中滴加稀盐酸,让其充分反应,放出氢气的质量与所滴加稀盐酸的质量关系如图所示。请回答下列问题并计算:

(1)充分反应后,产生氢气的质量是___________ 。
(2)该铝片中铝的质量分数(写出计算过程)。

(1)充分反应后,产生氢气的质量是
(2)该铝片中铝的质量分数(写出计算过程)。
更新时间:2023-05-20 08:51:52
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】将34.6g氯酸钾和二氧化锰的混合物充分加热至质量不再发生变化,收集到9.6g氧气。
(1)氯酸钾中氯元素的质量分数为______ (结果精确到0.1%)。
(2)求上述混合物中氯酸钾的质量。(写出计算过程)
(1)氯酸钾中氯元素的质量分数为
(2)求上述混合物中氯酸钾的质量。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】侯氏制碱法生产的碳酸钠中常含有少量的氯化钠,为测定碳酸钠的含量,某综合实践活动小组的同学取含有氯化钠的碳酸钠样品12.5g,将其放入干净的烧杯中,向其中加入100克溶质质量分数为7.3%的稀盐酸,恰好完全反应。
求:碳酸钠和氯化钠的混合物样品中碳酸钠的质量分数(写出计算过程,结果精确至0.1%)。
求:碳酸钠和氯化钠的混合物样品中碳酸钠的质量分数(写出计算过程,结果精确至0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】铜锌合金外观似金子,化学小组为检测其中锌的质量分数,按下列流程进行探究实验,充分反应,所得数据如图所示(忽略盐酸的挥发):

求:
(1)生成氢气的总质量为____________ g。
(2)合金中锌的质量分数。

求:
(1)生成氢气的总质量为
(2)合金中锌的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】测定铁制品中铁的质量分数
铁是常用的金属材料,兴趣小组的同学对某铁制品中的质量分数进行测定.称取3g铁屑,缓慢加入一定溶质质量分数的硫酸溶液25g,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示.

请计算:
(1)该铁制品中的铁的质量分数.(最终结果保留到0.1%)
(2)所用硫酸溶液的溶质质量分数.(要求有计算的过程)
铁是常用的金属材料,兴趣小组的同学对某铁制品中的质量分数进行测定.称取3g铁屑,缓慢加入一定溶质质量分数的硫酸溶液25g,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示.

请计算:
(1)该铁制品中的铁的质量分数.(最终结果保留到0.1%)
(2)所用硫酸溶液的溶质质量分数.(要求有计算的过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
试回答下列问题:
(1)从以上数据可知,表格中,m=_______ 。
(2)计算所用稀硫酸中硫酸的质量分数是__________ ?
| 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
| 第1次 | 40 | m |
| 第2次 | 40 | 14.8 |
| 第3次 | 40 | 12.2 |
| 第4次 | 40 | 11.2 |
| 第5次 | 40 | 11.2 |
(1)从以上数据可知,表格中,m=
(2)计算所用稀硫酸中硫酸的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某同学在常温下进行了中和反应的实验探究。向 溶液(预先滴入3滴酚酞试液)中逐滴滴入
溶液(预先滴入3滴酚酞试液)中逐滴滴入 的稀盐酸(该稀盐酸的密度约为
的稀盐酸(该稀盐酸的密度约为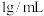 )。如图甲所示装置,同学们借助传感器监测溶液
)。如图甲所示装置,同学们借助传感器监测溶液 和温度的变化情况来探究稀盐酸和氢氧化钠溶液的反应,图乙为反应过程中溶液的
和温度的变化情况来探究稀盐酸和氢氧化钠溶液的反应,图乙为反应过程中溶液的 变化曲线,图丙为反应过程中溶液温度的变化曲线。
变化曲线,图丙为反应过程中溶液温度的变化曲线。

(1)由图丙可知该反应为______ (填“放热”或“吸热”)反应。
(2)计算所用氢氧化钠溶液的溶质质量分数。
 溶液(预先滴入3滴酚酞试液)中逐滴滴入
溶液(预先滴入3滴酚酞试液)中逐滴滴入 的稀盐酸(该稀盐酸的密度约为
的稀盐酸(该稀盐酸的密度约为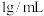 )。如图甲所示装置,同学们借助传感器监测溶液
)。如图甲所示装置,同学们借助传感器监测溶液 和温度的变化情况来探究稀盐酸和氢氧化钠溶液的反应,图乙为反应过程中溶液的
和温度的变化情况来探究稀盐酸和氢氧化钠溶液的反应,图乙为反应过程中溶液的 变化曲线,图丙为反应过程中溶液温度的变化曲线。
变化曲线,图丙为反应过程中溶液温度的变化曲线。
(1)由图丙可知该反应为
(2)计算所用氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室制取氧气时,某同学取质量为x的高锰酸钾加热,记录产生氧气的质量与加热时间的关系如图1所示,请回答下列问题:
(1)t0﹣t1时段固体质量不变,为什么_______ ?
(2)请根据图中数据计算高锰酸钾的质量x为____ ?(写出计算过程)请在图2坐标中,画出固体中锰元素质量在t0﹣t5时段变化示意图____ 。

(1)t0﹣t1时段固体质量不变,为什么
(2)请根据图中数据计算高锰酸钾的质量x为

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】羰基铁粉在国防军工领域有重要应用,我国是少数几个掌握其生产技术的国家之一。制备羰基铁粉的过程如图1所示。

(1) Fe(CO)5中碳、氧元素的原子个数比为______ ,质量比为______ 。
(2)反应2的化学方程式为 。若要获得1l.2kg的羰基铁粉(Fe),则至少需要
。若要获得1l.2kg的羰基铁粉(Fe),则至少需要______ kg Fe(CO)5。
(3)一定质量的Fe(CO)5分解生成羰基铁粉的质量随时间的变化如图2所示,则在______ 时Fe(CO)5恰好完全分解(填写“t1”“t2”“t3”“t4")。

(1) Fe(CO)5中碳、氧元素的原子个数比为
(2)反应2的化学方程式为
 。若要获得1l.2kg的羰基铁粉(Fe),则至少需要
。若要获得1l.2kg的羰基铁粉(Fe),则至少需要(3)一定质量的Fe(CO)5分解生成羰基铁粉的质量随时间的变化如图2所示,则在
您最近一年使用:0次

 ,某石灰窑中装入60 t石灰石原料,充分煅烧(杂质不会转化为气体)后得到固体38 t。试计算原料石灰石中含碳酸钙的质量分数。(最后结果精确到0.1%)
,某石灰窑中装入60 t石灰石原料,充分煅烧(杂质不会转化为气体)后得到固体38 t。试计算原料石灰石中含碳酸钙的质量分数。(最后结果精确到0.1%)


