某小组同学利用含有Fe(NO3)2、Cu(NO3)2、AgNO3的废液回收Ag,实验流程如下。
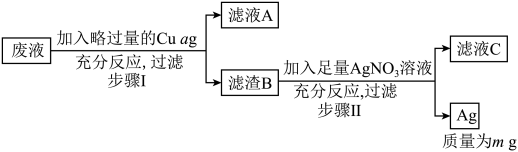
(1)滤液A中含有________ 溶质。
(2)写出步骤Ⅱ中发生反应的化学方程式________ 。
(3)若将步骤Ⅰ中的“加入略过量的Cu ag”改为“加入略过量的Fe ag”,最终得到Ag的质量_____ (选填“大于”、“等于”或“小于”)mg。

(1)滤液A中含有
(2)写出步骤Ⅱ中发生反应的化学方程式
(3)若将步骤Ⅰ中的“加入略过量的Cu ag”改为“加入略过量的Fe ag”,最终得到Ag的质量
更新时间:2023-05-26 22:31:59
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】根据下图回答下列问题。

(1)该配料表中,提供钙元素的物质中钙元素的质量分数为__________ 。
(2)服用该保健品后,有时会出现腹胀、打嗝等反应,出现这种反应的原因是___________ (用化学方程式表示)。

(1)该配料表中,提供钙元素的物质中钙元素的质量分数为
(2)服用该保健品后,有时会出现腹胀、打嗝等反应,出现这种反应的原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】在农村人们常常饮用河水,河水中常含有大量的泥沙、悬浮物和细菌等杂质,一般可用次氯酸杀死细菌。将漂白粉(主要成分是次氯酸钙Ca(ClO)2)溶于水和二氧化碳可生成碳酸钙和次氯酸(HClO)。下列是某户居民在饮用水之前对河水的处理步骤:
河水→A(加入明矾)→B(沉淀)→C(过滤)→D(加入漂白粉)→净水
(1)可以除去较大颗粒、悬浮物杂质的步骤是______ ;
(2)能够消毒、杀菌的步骤是______ 。
(3)A步骤中加入明矾的作用是______ 。
(4)该农户得到的净水是纯净物还是混合物,原因是______ 。
(5)在过滤时,若经过两次过滤后滤液仍然浑浊,其原因可能是______ ,______ (要求写出两个方面的原因)。
(6)写出漂白粉溶于水后的反应方程式______ 。
河水→A(加入明矾)→B(沉淀)→C(过滤)→D(加入漂白粉)→净水
(1)可以除去较大颗粒、悬浮物杂质的步骤是
(2)能够消毒、杀菌的步骤是
(3)A步骤中加入明矾的作用是
(4)该农户得到的净水是纯净物还是混合物,原因是
(5)在过滤时,若经过两次过滤后滤液仍然浑浊,其原因可能是
(6)写出漂白粉溶于水后的反应方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】已知常用的强酸(盐酸、硫酸、硝酸)跟常用的强碱(氢氧化钠、氢氧化钾)反应生成的盐的水溶液显中性。现将某蓝色晶体A溶入某一无色中性液体中,按下图所示过程进行实验:
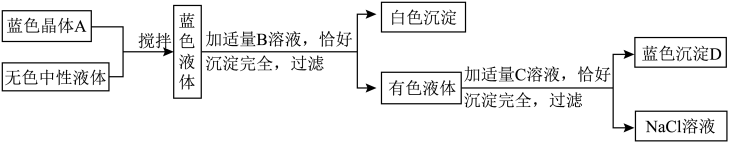
试按要求填写下列空白:
(1)写出B、C溶液中溶质的化学式:B_________ ,C ________ ;
(2)若A是纯净物,无色中性液体也是纯净物,则中性液体是______________ (填化学式);
(3)若A是纯净物,无色中性液体是只含有一种溶质的溶液,则其溶质是____ 或 _______ (填化学式);
(4)写出有色液体与C溶液反应的化学方程式___________________________ 。

试按要求填写下列空白:
(1)写出B、C溶液中溶质的化学式:B
(2)若A是纯净物,无色中性液体也是纯净物,则中性液体是
(3)若A是纯净物,无色中性液体是只含有一种溶质的溶液,则其溶质是
(4)写出有色液体与C溶液反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属材料广泛应用于生产、生活中。
(1)台灯中,铜质插头是利用了金属铜的______ 性(填“导电”或“导热”)。灯管后面的反光片为铝箔。铝在空气中与氧气反应,生成氧化铝,反应的化学方程式为______________ 。
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是______ (填序号)。
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收硫酸锌和有关金属,实验过程如下:
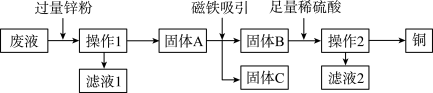
①“操作1”和“操作2”的名称是________ 。
②固体A的成分是________ 。
③废液的质量________ (填“大于”或“小于”或“等于”)滤液1的质量。
④若加锌粉量不足,则滤液1中的溶质不可能是___ (填字母).
A.ZnSO4和FeSO4 B.ZnSO4和CuSO4
C.CuSO4和FeSO4 D.ZnSO4、CuSO4和FeSO4
(4)现有一包由5.6 g铁、7.2 g镁、1.0 g碳混合而成的粉末,把它加入一定量的氯化铜溶液中,实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量不可能是______(填字母)。
(1)台灯中,铜质插头是利用了金属铜的
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收硫酸锌和有关金属,实验过程如下:

①“操作1”和“操作2”的名称是
②固体A的成分是
③废液的质量
④若加锌粉量不足,则滤液1中的溶质不可能是
A.ZnSO4和FeSO4 B.ZnSO4和CuSO4
C.CuSO4和FeSO4 D.ZnSO4、CuSO4和FeSO4
(4)现有一包由5.6 g铁、7.2 g镁、1.0 g碳混合而成的粉末,把它加入一定量的氯化铜溶液中,实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量不可能是______(填字母)。
| A.26.2 g | B.26.6 g | C.26.0 g | D.25.8 g |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品,加入镁粉,充分反应后过滤,得到滤液和滤渣。请填写下列空格:
(1)若滤渣中有镁粉,则滤渣中除镁粉外还含有______ (写化学式,下同)。
(2)若滤渣中有铜粉,则滤液中的溶质一定含有______ ,可能含有______ 。
(3)若滤渣中没有铜粉,则滤液中的溶质一定含有______ ,可能含有______ 。
(4)金属活动性顺序在工农业生产和科学研究中都有重要作用,现有A、B、C三种金属,A、B可溶于盐酸,C不溶于盐酸,将A投入BCl2溶液中可发生反应:A+BCl2=ACl2+B。
①A、B、C三者金属活动性由强到弱的顺序为______ 。与金属置换反应规律相同,非金属单质之间的置换反应也有类似的规律,根据下列反应:Cl2+2NaBr=Br2+2NaCl,Br2+2NaI= I2+2NaBr
②Cl2、Br2和I2单质的活泼性由强到弱的顺序为______ 。
③根据以上规律,下列反应可以发生的是______ 。
a Cl2+2KI= 2KCl+I2
b 2NaCl+I2 =2NaI+Cl2↑
(1)若滤渣中有镁粉,则滤渣中除镁粉外还含有
(2)若滤渣中有铜粉,则滤液中的溶质一定含有
(3)若滤渣中没有铜粉,则滤液中的溶质一定含有
(4)金属活动性顺序在工农业生产和科学研究中都有重要作用,现有A、B、C三种金属,A、B可溶于盐酸,C不溶于盐酸,将A投入BCl2溶液中可发生反应:A+BCl2=ACl2+B。
①A、B、C三者金属活动性由强到弱的顺序为
②Cl2、Br2和I2单质的活泼性由强到弱的顺序为
③根据以上规律,下列反应可以发生的是
a Cl2+2KI= 2KCl+I2
b 2NaCl+I2 =2NaI+Cl2↑
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】某工厂电镀车间的废液中含有硝酸亚铁、硝酸铜、硝酸银,回收贵重金属同时制取医药原料硝酸亚铁的简易流程如图所示。
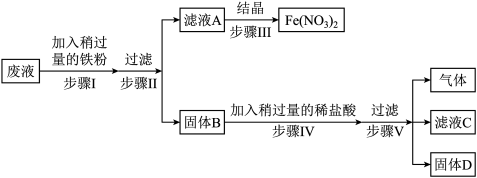
(1)固体B与稀盐酸反应生成气体的化学方程式是______ 。
(2)固体D的成分是______ 。
(3)步骤I中,加入的铁粉需“过量”,目的是______ 。
(4)下列有关该实验的分析中,不正确的是______(填字母)。

(1)固体B与稀盐酸反应生成气体的化学方程式是
(2)固体D的成分是
(3)步骤I中,加入的铁粉需“过量”,目的是
(4)下列有关该实验的分析中,不正确的是______(填字母)。
| A.滤液A为浅绿色 |
| B.固体B中有3种金属 |
| C.滤液C中的阳离子只有H+ |
| D.固体D的质量一定小于固体B的质量 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属及金属材料在生产、生活中的应用推动了社会的发展。
(1)下列生活用品中,主要利用金属导热性的是______(填序号)。
(2)人们常说的“五金”是指“金、银、铜、铁、锌”,根据所学知识判断,不能与盐酸反应的金属是______ (填名称)。黄铜是铜锌合金,其硬度比纯铜______ (填“大”“小”或“相同”)。
(3)向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B.向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有______ ;滤液B中一定没有的金属离子是______ 。
(4)某同学称量11.4g某铁合金样品,放入烧杯中,再往烧杯中加入189.2g稀硫酸,恰好完全反应(杂质不溶于水,也不参加反应),得到200g溶液。则该铁合金中铁的质量为______ g,属于______ (填“钢”或“生铁”)。
(1)下列生活用品中,主要利用金属导热性的是______(填序号)。
| A.铁锅 | B.导线 | C.易拉罐 |
(3)向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B.向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有
(4)某同学称量11.4g某铁合金样品,放入烧杯中,再往烧杯中加入189.2g稀硫酸,恰好完全反应(杂质不溶于水,也不参加反应),得到200g溶液。则该铁合金中铁的质量为
您最近一年使用:0次



