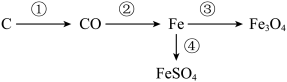
化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)小宸同学用氯化钠固体配制溶质质量分数为5%的氯化钠溶液100g,以备实验。
①通过计算,需称取氯化钠的质量为______ g。
②量取水的体积时,小宸同学仰视读数,则配制的氯化钠溶液的溶质质量分数将_______ (选填“偏小”、“不变”或“偏大”)。
(2)小组同学利用如图所示装置模拟工业炼铁。

①实验中a处观察到的现象是_________ 。
②写出一种可以处理尾气的合理方法:__________ 。
(3)用“海水晒盐”的方法得到的粗盐中,往往含有多种可溶性杂质(Na2SO4、MgCl2、CaCl2)和难溶性杂质(泥沙),需进行分离和提纯后才能用于人们的日常生活。下图是兴趣小组在实验室对粗盐样品提纯的流程图。

①Ⅰ中玻璃棒的作用是________ 。
②Ⅴ中发生反应的化学方程式为________ 。(写出一个即可)
③只调换Ⅱ和Ⅲ的顺序,能否达到实验目的,并说明理由:__________ 。
(4)小宸同学在实验室中取18g混有少量二氧化锰的高锰酸钾固体样品加热制取氧气,充分加热后,他称得剩余固体的总质量比反应前减少了1.6g。18g该固体样品中高锰酸钾的质量是多少?
(1)小宸同学用氯化钠固体配制溶质质量分数为5%的氯化钠溶液100g,以备实验。
①通过计算,需称取氯化钠的质量为
②量取水的体积时,小宸同学仰视读数,则配制的氯化钠溶液的溶质质量分数将
(2)小组同学利用如图所示装置模拟工业炼铁。

①实验中a处观察到的现象是
②写出一种可以处理尾气的合理方法:
(3)用“海水晒盐”的方法得到的粗盐中,往往含有多种可溶性杂质(Na2SO4、MgCl2、CaCl2)和难溶性杂质(泥沙),需进行分离和提纯后才能用于人们的日常生活。下图是兴趣小组在实验室对粗盐样品提纯的流程图。

①Ⅰ中玻璃棒的作用是
②Ⅴ中发生反应的化学方程式为
③只调换Ⅱ和Ⅲ的顺序,能否达到实验目的,并说明理由:
(4)小宸同学在实验室中取18g混有少量二氧化锰的高锰酸钾固体样品加热制取氧气,充分加热后,他称得剩余固体的总质量比反应前减少了1.6g。18g该固体样品中高锰酸钾的质量是多少?
更新时间:2023-05-26 22:31:59
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】工业上常用氢化锂(LiH)来制取氢气,反应的化学方程式为:LiH+H2O=LiOH+H2↑现将15克氢化锂与足量水反应,求:
(1)反应的化学方程式中氢元素的化合价有___ 种。LiH中阴离子的符号为___ ,反应物和生成物中氧化物为___ ,LiOH中一个阴离子中的电子数为___ 。
(2)列方程式计算生成氢气的质量____ 。(精确到小数后2位)
(1)反应的化学方程式中氢元素的化合价有
(2)列方程式计算生成氢气的质量
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)请用化学符号表示:硫酸亚铁中的阴离子________ 。
(2)A、B、C、D表示4种物质,其微观示意图见下表。A和B在一定条件下反应可生成C和D。回答下列问题:
①上述物质中属于氧化物的是________ (填字母代号);
②若反应后生成8.8 g C,则生成D的质量为________ 。
(1)请用化学符号表示:硫酸亚铁中的阴离子
(2)A、B、C、D表示4种物质,其微观示意图见下表。A和B在一定条件下反应可生成C和D。回答下列问题:
反应前 | 反应后 |
| ||
A | B | C | D | |
|
|
|
| |
②若反应后生成8.8 g C,则生成D的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】化学实验操作考试的考场收集到氢氧化铜和部分已经分解成氧化铜的固体混合物4.5g,滴入稀硫酸至固体完全溶解,得到溶液50g,经测定,该溶液中硫元素的质量分数为3.2%。向该溶液中加入足量的铁粉,发生的反应方程式为:_______ 。充分反应后,可回收到铜的质量为_______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】《天工开物》中记载了采矿和冶炼金属锡的场景。

(1)采矿(图1)
“水锡…其质黑色…愈经淘取”。水中淘取锡砂(指锡矿石)时,所用容器的孔径需___________ (填“大于”或“小于”)锡砂颗粒大小。锡砂主要成分为SnO2,___________ (填“易”或“难)溶于水。
(2)冶炼(图2)
“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”
冶炼的核心步骤是一氧化碳在高温条件还原锡砂,请写出该反应的方程式___________ 。
(3)使用
古代锡器常用来饮酒喝茶,很少装酸性物质,原因是___________ 。

(1)采矿(图1)
“水锡…其质黑色…愈经淘取”。水中淘取锡砂(指锡矿石)时,所用容器的孔径需
(2)冶炼(图2)
“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”
冶炼的核心步骤是一氧化碳在高温条件还原锡砂,请写出该反应的方程式
(3)使用
古代锡器常用来饮酒喝茶,很少装酸性物质,原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为高炉冶铁、炼钢,并用生产的钢来探究白铜成分的流程图。
(查阅资料:硫酸镍的化学式为NiSO4)
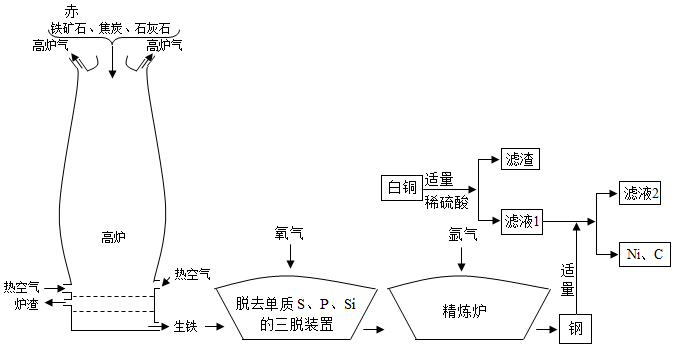
(1)用高炉冶铁的主要反应原理是___________ (用化学方程式表示)。
(2)分析流程图,三脱装置中发生反应时生成的一种生成物的化学式为___________ 。
(3)高炉炼铁中加入石灰石的作用___________ 。
(4)铁与镍相比,铁的金属活动性___________ 镍(选填“>”“=”或“<”)。
(5)通过以上信息,得出白铜的成分是___________ 。
(查阅资料:硫酸镍的化学式为NiSO4)

(1)用高炉冶铁的主要反应原理是
(2)分析流程图,三脱装置中发生反应时生成的一种生成物的化学式为
(3)高炉炼铁中加入石灰石的作用
(4)铁与镍相比,铁的金属活动性
(5)通过以上信息,得出白铜的成分是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是一种重要的物质,在日常生活和生产实践中有着不可替代的作用。请按要求回答下列问题。
Ⅰ.从组成角度看,水是由氢氧元素组成的,从结构角度看,水是由____ 构成的(填“分子”、“原子”或“离子”)。
Ⅱ.从变化角度看,水参加光合作用的化学方程式为6CO2+6H2O X +6O2,则X的化学式为
X +6O2,则X的化学式为___ ;水通电分解可以生成未来最理想的清洁能源——氢气,此过程是将电能转化成____ 能,但该方法需消耗大量电能,需要寻找更为有效的节能方法促进水的分解。
Ⅲ.从资源角度看,水是最常用的溶剂,天然水具有一定的硬度,最好采用____ 降低水的硬度(填“煮沸”或 “蒸馏”)来做实验室的溶剂。现有某兴趣小组同学需配制50克质量分数为12%的氯化钠溶液进行实验,实验操作过程如下图所示:
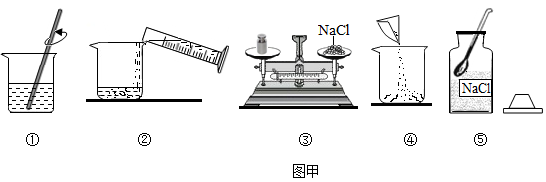
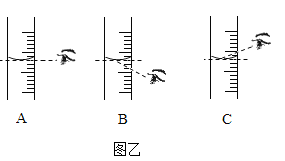
(1)图甲中一处明显错误的操作是____ (填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序____ ;其中图①中玻璃棒搅拌的目的是____ 。
(2)计算所需NaCl的质量为____ g,需要水____ mL (ρ水=1g/mL)。量取水时最好用____ mL的量筒(填“50mL”、“100mL”或“200mL”)量取。量取水操作如下:将水注入量筒,待液面接近量取体积对应刻度线时,改用____ (填仪器名称)滴加至刻度线;图乙中表示该同学正确读数方式的是____ (填序号);若用C观察方式量取水的体积,所配制溶液的溶质质量分数会____ (填“偏大”、“偏小”或“无影响”)。
Ⅰ.从组成角度看,水是由氢氧元素组成的,从结构角度看,水是由
Ⅱ.从变化角度看,水参加光合作用的化学方程式为6CO2+6H2O
 X +6O2,则X的化学式为
X +6O2,则X的化学式为Ⅲ.从资源角度看,水是最常用的溶剂,天然水具有一定的硬度,最好采用


(1)图甲中一处明显错误的操作是
(2)计算所需NaCl的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组展开了对硝酸钾固体及其溶液的实验探究,欲配制50g5%的硝酸钾溶液。

(1)以上正确的操作顺序是 。
(2)本实验需称取硝酸钾固体______ g;若称取固体时,托盘天平的指针略微向右偏移,需要进行的操作是______ 。
(3)现有10g20%的硝酸钾溶液(密度1.13g·cm-3),若将其稀释成5%的溶液,需要加入______ g水,稀释过程中除烧杯和玻璃棒外还需要的仪器是________ 。
(4)若所配150g5%硝酸钾溶液中硝酸钾的质量分数偏小(5克以下用游码),可能的原因有 。

(1)以上正确的操作顺序是 。
| A.④⑤①②③ | B.①②③④⑤ | C.⑤②①④③ | D.③④①②⑤ |
(3)现有10g20%的硝酸钾溶液(密度1.13g·cm-3),若将其稀释成5%的溶液,需要加入
(4)若所配150g5%硝酸钾溶液中硝酸钾的质量分数偏小(5克以下用游码),可能的原因有 。
| A.用托盘天平称取时,左边放砝码右边放硝酸钾 |
| B.转移已配好的溶液时,有少量液体溅出 |
| C.用量筒量取水时仰视读数 |
| D.烧杯用蒸馏水润洗后再配制溶液 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的NaCl溶液50g,按如下步骤进行操作:

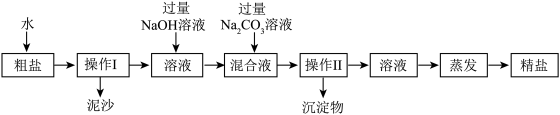
实验二:称取5.0g粗盐进行提纯。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示:
请你根据以上信息回答下述问题:
(1)配制50g溶质质量分数为6%的NaCl溶液,需NaCl________ g,水______ mL。把配好的溶液倒入试剂瓶中后,应盖好瓶塞并贴上标签,标签上应填写的内容为___________ 。
(2)NaCl溶解过程用到了玻璃棒,它的作用是________ 。蒸发过程中玻璃棒的作用是___________ 。
(3)粗盐提纯时,操作I的名称为________ ;该操作中用到的玻璃仪器有玻璃棒、__________ 和____________ 。
(4)某同学所得精盐比其他同学明显要少,原因可能是______。
实验一:配制溶质质量分数为6%的NaCl溶液50g,按如下步骤进行操作:

实验二:称取5.0g粗盐进行提纯。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示:

请你根据以上信息回答下述问题:
(1)配制50g溶质质量分数为6%的NaCl溶液,需NaCl
(2)NaCl溶解过程用到了玻璃棒,它的作用是
(3)粗盐提纯时,操作I的名称为
(4)某同学所得精盐比其他同学明显要少,原因可能是______。
| A.溶解时将5.0g粗盐一次全部倒入水中,立即过滤 |
| B.蒸发时有一些液体、固体溅出 |
| C.过滤时承接滤液的烧杯中有水 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数的氯化钠溶液的配制”两个实验。

(1)“粗盐中难溶性杂质的去除”的实验操作步骤为___________________ 。
(2)操作E中得到的滤液仍浑浊,其原因可能是_______ (答出一点即可)。
(3)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会_______ (填“偏大”、“偏小”或“不变”)。
(4)图D中玻璃棒的作用是_______________ 。
(5)图C中有一处明显的错误,请你改正:______________ 。

(1)“粗盐中难溶性杂质的去除”的实验操作步骤为
(2)操作E中得到的滤液仍浑浊,其原因可能是
(3)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会
(4)图D中玻璃棒的作用是
(5)图C中有一处明显的错误,请你改正:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化钠作为食盐的主要成分,同时在工业、农业等领域也具有十分重要的意义、工业上饱和氯化钠溶液可以作为侯氏制碱法的反应物之一,工业上以粗盐为原料制备氯化钠溶液时,首先要除去粗盐中的杂质CaCl2、MgCl2、Na2SO4和泥沙。为达到上述目的,某化学小组设计了如图实验。
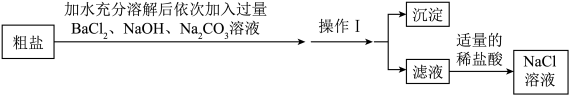
(1)写出除去Na2SO4时发生反应的化学方程式______ ;
(2)请设计实验验证操作Ⅰ后所得滤液中除氯化钠外还含有的溶质的成分______ ;(简要写出实验步骤、现象和结论)
(3)侯氏制碱法的其中一个反应为 。若消耗22.1t 饱和氯化钠溶液,理论上得到了8.4 t NaHCO3,则该饱和氯化钠溶液的溶质质量分数是多少?(计算结果精确到0.1%)
。若消耗22.1t 饱和氯化钠溶液,理论上得到了8.4 t NaHCO3,则该饱和氯化钠溶液的溶质质量分数是多少?(计算结果精确到0.1%)

(1)写出除去Na2SO4时发生反应的化学方程式
(2)请设计实验验证操作Ⅰ后所得滤液中除氯化钠外还含有的溶质的成分
(3)侯氏制碱法的其中一个反应为
 。若消耗22.1t 饱和氯化钠溶液,理论上得到了8.4 t NaHCO3,则该饱和氯化钠溶液的溶质质量分数是多少?(计算结果精确到0.1%)
。若消耗22.1t 饱和氯化钠溶液,理论上得到了8.4 t NaHCO3,则该饱和氯化钠溶液的溶质质量分数是多少?(计算结果精确到0.1%)
您最近一年使用:0次