以下是以空气、海水中的物质为原料,制得纯碱的工业流程。(已知粗盐中含有Ca2+、Mg2+、 等杂质离子)
等杂质离子)

(1)除去粗盐悬浊液中的Ca2+、Mg2+、 杂质离子,要依次加入稍过量的x、y、z溶液,分别可以是______。
杂质离子,要依次加入稍过量的x、y、z溶液,分别可以是______。
(2)请写出向粗盐悬浊液中加入适量稀盐酸的属于中和反应的化学方程式:______ 。
(3)经过操作1分离出粗制饱和食盐水和滤渣,滤渣中除含有泥沙外,含有的碳酸盐有______ 。(填化学式)
(4)空气经过操作2得到氮气,它的原理是利用物质的______ 不同,把氮气与其他物质分离,氢气与氮气在一定条件下转化为氨气的反应属于______ 反应(填基本反应类型)。
(5)请写出氨气与气体A、饱和食盐水反应生成氯化铵溶液和小苏打晶体的化学反应方程式:______ 。
(6)为了提高纯碱的产率,必须要吸收更多的氨气和气体A,根据两种气体的溶解性(如下表),请分析先通氨气后通气体A的原因:______ 。
 等杂质离子)
等杂质离子)
(1)除去粗盐悬浊液中的Ca2+、Mg2+、
 杂质离子,要依次加入稍过量的x、y、z溶液,分别可以是______。
杂质离子,要依次加入稍过量的x、y、z溶液,分别可以是______。| A.x是NaOH溶液,y是BaCl2溶液,z是Na2CO3溶液 |
| B.x是BaCl2溶液,y是NaOH溶液,x是Na2CO3溶液 |
| C.x是Na2CO3溶液,y是NaOH溶液,z是BaCl2溶液 |
(3)经过操作1分离出粗制饱和食盐水和滤渣,滤渣中除含有泥沙外,含有的碳酸盐有
(4)空气经过操作2得到氮气,它的原理是利用物质的
(5)请写出氨气与气体A、饱和食盐水反应生成氯化铵溶液和小苏打晶体的化学反应方程式:
(6)为了提高纯碱的产率,必须要吸收更多的氨气和气体A,根据两种气体的溶解性(如下表),请分析先通氨气后通气体A的原因:
气体 | 氨气 | 气体A |
溶解性/(mL/1mL水) | 700 | 1 |
2021·广东·模拟预测 查看更多[1]
更新时间:2023-06-11 16:00:45
|
相似题推荐
【推荐1】如图是某种胃药的部分标识。胃药中所含的物质能中和胃里过多的胃酸(主要是盐酸),某患者按标识上的服用方法服药,服药三天后病情好转。氢氧化镁与胃酸(含盐酸)作用的化学方程式为______ ;计算该患者在三天内所服用的此胃药中相当于吸收了______ 毫克的镁元素。


您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】归纳是学习的重要方法,小丽在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图1所示,连线表示相互反应)小君为表示反应实质绘制图2、图3.请根据下列图示和要求回答问题:

(1)图1中为了验证性质①,小丽将紫色石蕊试液滴加到盐酸溶液中,溶液变_____ 色。
(2)图1中A所表示的物质类别是______ 。
(3)图1中盐酸的性质③决定了盐酸可用于消除铁锈(主要成分Fe2O3),该反应的学方程式是_____ 。
(4)图1中选用合适的物质验证性质⑤,其反应的化学方程式为_______ 。
(5)图2描述了氢氧化钠溶液与盐酸反应的微观实质,该反应的基本反应类型为_______ ,图中A、B、C处应填入的离子符号或化学式依次为_______ 。
(6)镁与稀盐酸反应现象是_______ ,图3是二者反应过程的微观示意图,从微观角度看,该反应有效相互作用的微粒是_____ (写微粒符号,下同),产生的新微粒是______ 。
(7)不同酸具有相似的性质,但性质也存在差异,稀盐酸不能与氯化钡溶液反应,而稀硫酸却能与其反应,原因是_______ 。

(1)图1中为了验证性质①,小丽将紫色石蕊试液滴加到盐酸溶液中,溶液变
(2)图1中A所表示的物质类别是
(3)图1中盐酸的性质③决定了盐酸可用于消除铁锈(主要成分Fe2O3),该反应的学方程式是
(4)图1中选用合适的物质验证性质⑤,其反应的化学方程式为
(5)图2描述了氢氧化钠溶液与盐酸反应的微观实质,该反应的基本反应类型为
(6)镁与稀盐酸反应现象是
(7)不同酸具有相似的性质,但性质也存在差异,稀盐酸不能与氯化钡溶液反应,而稀硫酸却能与其反应,原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应。请回答下列问题:

(1)反应①的化学方程式为____________________________________________________ ;反应的实验现象有___________________________________________ 。
(2)物质C应是酸、碱、盐中的哪类物质?________ 。
(3)写出图中一个中和反应的化学方程式________________________________________ 。

(1)反应①的化学方程式为
(2)物质C应是酸、碱、盐中的哪类物质?
(3)写出图中一个中和反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A-E为初中化学常见的几种物质,其中B能供给呼吸,C常温下是液体,D是黑色固体,E溶液呈蓝色,F微溶于水。它们之间存在如图所示的关系。请回答下列问题。

(1)A的化学式为__________ 。
(2)C生成F反应过程中______ (填“吸收”或“放出”)热量。
(3)E与F反应的基本类型为_________ 反应。
(4)D生成E反应的化学方程式为__________ 。

(1)A的化学式为
(2)C生成F反应过程中
(3)E与F反应的基本类型为
(4)D生成E反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】为验证氯酸钾中含有氯元素,某化学兴趣小组的实验流程如图所示(夹持装置略去)。

(1)气体x的化学式_____ 。
(2)操作①的名称_____ 。
(3)产生白色沉淀的化学方程式_____ 。
(4)检验固体a中不含有KClO3的方法是_____ 。

(1)气体x的化学式
(2)操作①的名称
(3)产生白色沉淀的化学方程式
(4)检验固体a中不含有KClO3的方法是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。


(1)碳替代、碳减排、碳封存、碳循环是实现“碳中和”的4种主要途径,科学家预测,到2050年,4种途径对全球碳中和的贡献率如图一,由图一可知,到2050年,对全球碳中和贡献率最大的途径是______ 。
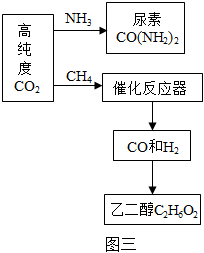
(2)“碳封存”是我国一项先进技术,运用该技术,CO2将被压到地下或海水中封存如图二,被封存的CO2有许多用途,如用于食品保鲜、化工原料等如图三,以此来消除资源的巨大浪费。
①将分离聚集的CO2压入地下的过程中,分子间隔会______ (填“增大”“减小”“不变”)。
②催化反应器中发生反应的化学方程式为______ 。
(3)“碳辅捉”是“碳封存“的首要环节,CO2的吸收常选用NaOH、氨水、一乙醇胺等作吸收剂。
Ⅰ、利用氢氧化钠溶液辅提CO2,将其再释出的一种途径如图四:


①“捕捉室”中反应的化学方程式为______ 。
②“煅烧炉”中反应的化学方程式为______ 。
③上述流程中可循环使用的物质有______ (填化学式)。
Ⅱ、膜吸收法吸收CO2研究人员通过实验比较了三种吸收剂,一乙醇胺、二乙醇胺、氨基乙酸钾对烟气中CO2的脱除效果,其结果如图五。
④由图五可知,随烟气流速增大,CO2脱除效果______ (填“增强”或“减弱”或“不变”)。
⑤从全面分析图五相关信息可知,采取______ 措施,可以进一步提升CO2脱除率。



(1)碳替代、碳减排、碳封存、碳循环是实现“碳中和”的4种主要途径,科学家预测,到2050年,4种途径对全球碳中和的贡献率如图一,由图一可知,到2050年,对全球碳中和贡献率最大的途径是
(2)“碳封存”是我国一项先进技术,运用该技术,CO2将被压到地下或海水中封存如图二,被封存的CO2有许多用途,如用于食品保鲜、化工原料等如图三,以此来消除资源的巨大浪费。
①将分离聚集的CO2压入地下的过程中,分子间隔会
②催化反应器中发生反应的化学方程式为
(3)“碳辅捉”是“碳封存“的首要环节,CO2的吸收常选用NaOH、氨水、一乙醇胺等作吸收剂。
Ⅰ、利用氢氧化钠溶液辅提CO2,将其再释出的一种途径如图四:


①“捕捉室”中反应的化学方程式为
②“煅烧炉”中反应的化学方程式为
③上述流程中可循环使用的物质有
Ⅱ、膜吸收法吸收CO2研究人员通过实验比较了三种吸收剂,一乙醇胺、二乙醇胺、氨基乙酸钾对烟气中CO2的脱除效果,其结果如图五。
④由图五可知,随烟气流速增大,CO2脱除效果
⑤从全面分析图五相关信息可知,采取
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氯化钠是日常生活的必需品,也是重要的化工原料。某粗盐样品除含NaCl外,还含有少量Na2SO4以及泥沙等杂质。下图是化学兴趣小组的同学做粗盐提纯的操作流程。

请回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ为同一操作,其名称是______ ,操作Ⅳ的名称是______ 。
(2)写出生成沉淀①的化学方程式______ 。
(3)物质X是______ 。
(4)他们用提纯得到的精盐配制200g0.9%的氯化钠溶液,需要NaCl的质量为______ 。
①配制该溶液时所需要的玻璃仪器有量筒、胶头滴管、烧杯、______ 。
②配制该溶液用量筒量取水时,俯视量筒读数,则所得氯化钠溶液的溶质质量分数______ (填“偏大”“偏小”或“不变”)。

请回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ为同一操作,其名称是
(2)写出生成沉淀①的化学方程式
(3)物质X是
(4)他们用提纯得到的精盐配制200g0.9%的氯化钠溶液,需要NaCl的质量为
①配制该溶液时所需要的玻璃仪器有量筒、胶头滴管、烧杯、
②配制该溶液用量筒量取水时,俯视量筒读数,则所得氯化钠溶液的溶质质量分数
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】食盐是我们日常生活必备的调味品,通过晾晒海水或煮盐井水、盐湖水可得粗盐。粗盐中除含泥沙外,还可能含有CaCl2、MgCl2、Na2SO4中的一种或几种杂质。某化学小组为确定杂质成分并将其除去,进行了如图所示实验。

(1)过滤操作需要的玻璃仪器有烧杯、漏斗和玻璃棒.其中玻璃棒的作用是什么
(2)写出加入BaCl2溶液时发生反应的化学方程式
(3)通过实验可得出粗盐中一定含有哪些杂质
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】我国是一个海洋大国,海水中蕴含着丰富的化学资源。

(1)海水晒盐:盐田法晒盐,盐田分蒸发池和结晶池两部分。下列说法正确的 _________。
(2)海水制镁:镁及其合金是一种用途很广的金属材料。结晶池中分离出氯化钠后的溶液称为母液,母液中含大量 MgC12,可制备金属镁,主要物质转化关系如图所示:

①写出生成 Mg(OH)2的化学反应方程式_____ 。
②步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是______ 。
③步骤①得到的 Mg(OH)2沉淀中混有少量的_____ (填化学式),除去少量该杂质的方法是将沉淀加入氯化镁溶液中,充分搅拌后经过滤、______ (填操作方法)、干燥,即可得到纯净的 Mg(OH)2。
(3)粗盐精制:粗盐水中主要含有 Ca2+、Mg2+、 等杂质离子,工业上常用加入稍过量的 A.NaOH 溶液 B.Na2CO3溶液 C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证 Na2CO3溶液在加入
等杂质离子,工业上常用加入稍过量的 A.NaOH 溶液 B.Na2CO3溶液 C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证 Na2CO3溶液在加入 _____ 之后再加入即可(填试剂序号)。

(1)海水晒盐:盐田法晒盐,盐田分蒸发池和结晶池两部分。下列说法正确的 _________。
| A.在蒸发池中水蒸发所需能量主要为太阳能和风能 |
| B.在结晶池中主要通过降温结晶使氯化钠析出 |
| C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液 |

①写出生成 Mg(OH)2的化学反应方程式
②步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是
③步骤①得到的 Mg(OH)2沉淀中混有少量的
(3)粗盐精制:粗盐水中主要含有 Ca2+、Mg2+、
 等杂质离子,工业上常用加入稍过量的 A.NaOH 溶液 B.Na2CO3溶液 C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证 Na2CO3溶液在加入
等杂质离子,工业上常用加入稍过量的 A.NaOH 溶液 B.Na2CO3溶液 C.BaCl2溶液和适量的盐酸等除杂、精制。加入前三种试剂顺序有很多,只要保证 Na2CO3溶液在加入
您最近一年使用:0次
【推荐1】二氧化碳的综合利用是实现“碳中和”的途径之一。如图是利用二氧化碳、氯化钠、氨气为原料制备碳酸钠的主要流程,回答下列问题。

(1)溶解池中,NaCl溶于水的过程中需不断搅拌,其目的是______ 。
(2)加热炉中发生反应的化学方程式为______ 。
(3)整个流程中除水之外可以循环利用的物质是______ 。
(4)制备得到的碳酸钠的用途有______ (写1种)。

(1)溶解池中,NaCl溶于水的过程中需不断搅拌,其目的是
(2)加热炉中发生反应的化学方程式为
(3)整个流程中除水之外可以循环利用的物质是
(4)制备得到的碳酸钠的用途有
您最近一年使用:0次
【推荐2】南海是我国的固有领海,蕴含着丰富的海洋资源。2017年5月18日,我国南海神狐海域的可燃冰试采取得圆满成功,实现历史性突破。
(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式_________________ 。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是_________________ 。
(3)1926年,我国著名化学家侯德榜先生创立了“侯氏制碱法”,促进了世界制碱技术的发展。“侯氏制碱法”以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度是_________________ 。
②t2℃时,Na2CO3的溶解度_______________ NaCl的溶解度(填“大于”“等于”“小于”之一)。
③t1℃时,50g水中加入18gNa2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为________________ (最简整数比)。
(1)可燃冰的主要成分是甲烷,试写出甲烷在空气中燃烧的化学方程式
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是
(3)1926年,我国著名化学家侯德榜先生创立了“侯氏制碱法”,促进了世界制碱技术的发展。“侯氏制碱法”以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度是
②t2℃时,Na2CO3的溶解度
③t1℃时,50g水中加入18gNa2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为
您最近一年使用:0次



