我国古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合加热到约800℃,得到黄铜(锌和铜的合金),现进行模拟,工艺流程如图所示。
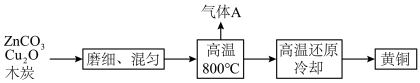
已知:2ZnCO3+2Cu2O+2C 2Zn+4Cu+4CO2↑
2Zn+4Cu+4CO2↑
(1)流程中体现了木炭的___________ (选填“可燃性”或“还原性”);“磨细、混匀”的目的是___________ 。
(2)气体A中一定含有CO2,可能含有___________ ;
(3)若用该工艺制备了1000g黄铜产品,其中铜单质的质量分数为64%。产生这些铜单质所需Cu2O的质量为___________ (写出计算过程)。
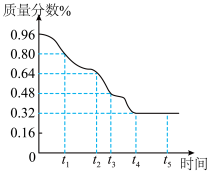
(4)“高温还原冷却”过程中,假设产品中氧元素质量分数随时间的变化如图所示。若(3)中产品是在t4后得到的,且产品中只含三种元素,则黄铜中至少含锌元素质量是多少?(写出计算过程)。

已知:2ZnCO3+2Cu2O+2C
 2Zn+4Cu+4CO2↑
2Zn+4Cu+4CO2↑(1)流程中体现了木炭的
(2)气体A中一定含有CO2,可能含有
(3)若用该工艺制备了1000g黄铜产品,其中铜单质的质量分数为64%。产生这些铜单质所需Cu2O的质量为
(4)“高温还原冷却”过程中,假设产品中氧元素质量分数随时间的变化如图所示。若(3)中产品是在t4后得到的,且产品中只含三种元素,则黄铜中至少含锌元素质量是多少?(写出计算过程)。

2023·广东·模拟预测 查看更多[2]
更新时间:2023-06-13 23:18:48
|
相似题推荐
【推荐1】钙是人体中含量最多的金属元素,钙的化合物在生产生活中有着广泛的应用。某化学兴趣小组对一些含钙的物质进行探究。
【温故知新】
(1)以下四种物质中能作为补钙剂的有
a.CaCO3 b. CaO c.Ca(OH)2 d.CaCl2
(2)CaO常用作食品干燥剂,其干燥原理是
【提出问题】
农场常储备熟石灰用于改良酸性土壤,仓库内长期存放的熟石灰样品,其成分是什么?
【作出猜想】
(3)猜想:Ca(OH)2;猜想二:CaCO3;猜想三:
【资料查阅】氢氧化钙微溶于水。
【实验步骤与现象】
(4)
| 步骤 | 操作 | 现象 |
| 1 | 取1g样品于试管中,加入10 mL蒸馏水充分振荡 | 得到上层清液和下层固体 |
| 2 | 溶液变红 | |
| 3 | 向步骤2后的试管中逐滴滴加稀盐酸 | 溶液由红色变为无色,固体物质消失并产生气泡 |
【实验结论】通过以上实验可以知道猜想三正确。
【评价与反思】实验人员根据步骤1认为猜想三正确。其实该结论并不严密,请说明理由。
【拓展延伸】
(5)用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图2所示。由图1可知,该反应是将

(6)某化工厂用含氢氧化钙75%的熟石灰处理150 t质量分数为15%的硫酸废液(假设废液中的其他物质不与氢氧化钙反应),测得pH=7后再进行排放。计算理论上需要熟石灰多少吨?(精确到0.01)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】回答下列问题
(1)下图A、B是实验室常用制取氧气的发生装置,C是小红同学利用医疗器械自己组装的装置,请结合下列装置回答问题:
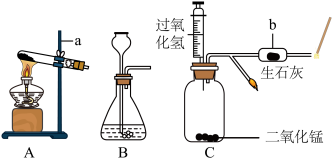
①仪器a的名称是___________ 。
②B装置制取氧气时长颈漏斗应伸到液面以下,原因是___________ 。
③C装置输液瓶内发生反应的化学方程式为___________ ,b处生石灰的作用是___________ 。
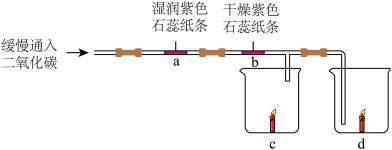
(2)某同学利用以下实验探究二氧化碳的性质。实验开始后,能观察到___________ 处的石蕊纸条变红,原因是___________ (用化学方程式表示)。一段时间后两只烧杯中蜡烛均熄灭,能证明CO2密度大于空气的是___________ 处的烧杯。
(3)向20g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。

请计算:该大理石样品中碳酸钙的质量分数是多少?(写出计算过程及结果)
(1)下图A、B是实验室常用制取氧气的发生装置,C是小红同学利用医疗器械自己组装的装置,请结合下列装置回答问题:

①仪器a的名称是
②B装置制取氧气时长颈漏斗应伸到液面以下,原因是
③C装置输液瓶内发生反应的化学方程式为
(2)某同学利用以下实验探究二氧化碳的性质。实验开始后,能观察到

(3)向20g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。

请计算:该大理石样品中碳酸钙的质量分数是多少?(写出计算过程及结果)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】高纯碳酸钙广泛应用于精密电子陶瓷、医药等生产。下图为模拟制各高纯碳酸钙的主要流程,已知该大理石中杂质是二氧化硅和氧化铁。按要求填空。

(1)大理石需经过粉碎处理,其目的是______ 。
(2)“除杂”中,适量的氨水是与______ 反应。(填物质的化学式)
(3)“转化”发生的主要反应的化学方程式是______ 。
(4)操作a为组合操作,步骤为______ 、洗涤、干燥。
(5)经查阅资料得知,鸡蛋壳的主要成分也是碳酸钙。某兴趣小组为了测定鸡蛋亮中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸,滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算该鸡蛋壳中CaCO3的质量分数(请依据化学方程进行计算)。


(1)大理石需经过粉碎处理,其目的是
(2)“除杂”中,适量的氨水是与
(3)“转化”发生的主要反应的化学方程式是
(4)操作a为组合操作,步骤为
(5)经查阅资料得知,鸡蛋壳的主要成分也是碳酸钙。某兴趣小组为了测定鸡蛋亮中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸,滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算该鸡蛋壳中CaCO3的质量分数(请依据化学方程进行计算)。

您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】每年的3月22日是“世界水日”,水与人类的生产、生活密切相关。
(1)家庭常用的净水器的基本原理可以用如图所示的简易装置表示。

①石子、细沙的作用是______ 。
②活性炭的作用是______ 。
③请设计实验检验净化后的水是硬水还是软水______ 。(简要叙述实验步骤及现象)
(2)为了探究水的组成,某小组利用如图装置进行实验。
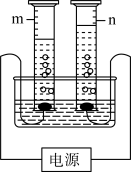
①与量筒n相连的是电源的______ (选填“正”或“负”)极。
②m、n量筒内生成的气体聚集在上部的原因是什么?______ 。
③该实验证明水是由______ 组成的。
④电解水的符号表达式为______ 。
(3)预防新冠肺炎期间,很多医院使用来苏水进行杀菌消毒,来苏水的主要成分之一是对甲基苯酚(C7H8O)。计算50g对甲基苯酚中碳元素的质量。
(1)家庭常用的净水器的基本原理可以用如图所示的简易装置表示。

①石子、细沙的作用是
②活性炭的作用是
③请设计实验检验净化后的水是硬水还是软水
(2)为了探究水的组成,某小组利用如图装置进行实验。

①与量筒n相连的是电源的
②m、n量筒内生成的气体聚集在上部的原因是什么?
③该实验证明水是由
④电解水的符号表达式为
(3)预防新冠肺炎期间,很多医院使用来苏水进行杀菌消毒,来苏水的主要成分之一是对甲基苯酚(C7H8O)。计算50g对甲基苯酚中碳元素的质量。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐2】过氧化钙(CaO2)可用于改善地表水质、处理重金属粒子废水、应急供氧等。称取7.2g过氧化钙固体加热。发生反应:2CaO2 2CaO+O2↑。该过程中,固体质量随温度变化如图所示。求:
2CaO+O2↑。该过程中,固体质量随温度变化如图所示。求:

(1)求B点对应纵坐标的数值(需要写出计算过程)。
(2)A点时,固体成分为_____ ,其中钙元素的质量为_____ g。
(3)CaO2是鱼类长途运输的供氧剂,它与水反应生成氧气,还生成一种碱,该反应的化学方程式为_______ 。
 2CaO+O2↑。该过程中,固体质量随温度变化如图所示。求:
2CaO+O2↑。该过程中,固体质量随温度变化如图所示。求:
(1)求B点对应纵坐标的数值(需要写出计算过程)。
(2)A点时,固体成分为
(3)CaO2是鱼类长途运输的供氧剂,它与水反应生成氧气,还生成一种碱,该反应的化学方程式为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】某同学用如图所示装置进行实验室氧气的制取。

(1)仪器a的名称为_______ 。
(2)反应的符号表达式为_______ 。
(3)实验中试管口必须略向下倾斜的原因是_______ 。
(4)待集气瓶口有大气泡向外冒出时,盖上玻璃片取出发现集气瓶中气体未收集满,主要原因是___ ;经检验收集到的氧气纯度较低,可能原因是____ 。
(5)氯酸钾和二氧化锰混合加热也可用于实验室制取氧气。请计算:
①氯酸钾的相对分子质量为____ 。
②_____ 质量的氯酸钾中含有9.6g氧元素?(写出解题过程)

(1)仪器a的名称为
(2)反应的符号表达式为
(3)实验中试管口必须略向下倾斜的原因是
(4)待集气瓶口有大气泡向外冒出时,盖上玻璃片取出发现集气瓶中气体未收集满,主要原因是
(5)氯酸钾和二氧化锰混合加热也可用于实验室制取氧气。请计算:
①氯酸钾的相对分子质量为
②
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】某研究小组为探究木炭还原氧化铜的实验后的产物,主要流程如下:

查阅资料:①氧化铜跟稀硫酸反应生成蓝色溶液;②常温下铜不与稀硫酸反应。
(1)“研磨”的目的是________ 。
(2)操作①名称是_______ 。如果液体C的颜色为蓝色,说明固体B中除了含有铜外还含有______ (填写物质的化学式)。
(3)要使40g氧化铜完全反应,需要木炭的质量至少是多少?(请写出计算过程)
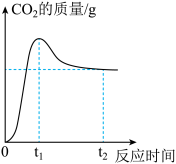
(4)小组同学将40g氧化铜和4.2g的炭粉在隔绝空气的密闭容器中持续加强热,通过CO2传感器测量密闭容器内CO2的质量变化曲线如图所示。发现在t1-t2时CO2在密闭容器中的质量会减少,你认为原因是_______ 。(用化学方程式表示)

查阅资料:①氧化铜跟稀硫酸反应生成蓝色溶液;②常温下铜不与稀硫酸反应。
(1)“研磨”的目的是
(2)操作①名称是
(3)要使40g氧化铜完全反应,需要木炭的质量至少是多少?(请写出计算过程)
(4)小组同学将40g氧化铜和4.2g的炭粉在隔绝空气的密闭容器中持续加强热,通过CO2传感器测量密闭容器内CO2的质量变化曲线如图所示。发现在t1-t2时CO2在密闭容器中的质量会减少,你认为原因是

您最近一年使用:0次
【推荐2】铜及其化合物在生活、生产中用途广泛。
(1)铜的制取:以氧化铜为原料制取铜。某研究小组为探究CO的还原性,设计了如下系列实验。

实验1:将CuO加水制成糊状,刷在试管内壁,在试管底部加入炭粉,再向试管中通入CO2(见图甲),集满后立即用气球密封。
实验2:用酒精灯加热CuO部位(见图乙),无明显现象。
实验3:用加网罩的酒精灯加热炭粉(见图丙);一段时间后,利用CO2传感器测得试管内CO2含量变小。
实验4:加热CuO(见图丁),黑色固体变成紫红色。
①实验1中浓硫酸的作用是___________ 。
②实验2得到的结论是___________ 。
③实验3的目的是___________ 。
④写出实验4中发生反应的化学方程式:___________ 。
(2)铜的锈蚀:铜锈的主要成分是碱式碳酸铜[化学式为Cu2(OH)2CO3]。
进行如下图所示的实验,探究铜生锈的条件。
将大小相同的4小块铜片按下图装置所示放置一个月,结果如下:
①实验中使用的蒸馏水需“经煮沸并迅速冷却”,其目的是___________ 。
②能说明铜生锈与H2O有关的实验是___________ 。
③通过上述实验现象,写出铜片表面生成铜锈的化学方程式:___________ 。
【查阅资料】铜锈一般分为无害锈与有害锈两种。[Cu2(OH)2CO3]属于“无害锈”,无害锈能保护青铜器。青铜器表面的有害锈为CuCl2·3Cu(OH)2,为绿色粉末,有害锈会使器物受损加剧,并不断扩散。有害锈的形成原理:铜在有Cl-的条件下生成CuCl,CuCl与氧气、水继续发生如下反应: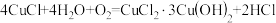 。
。
④与有害锈相比,无害锈能保护青铜器的原因可能是___________ 。
⑤为了有效的保护受腐蚀的青铜器,先将受腐蚀的青铜器用蒸馏水清洗干净,然后对锈蚀区用氧化银(Ag2O)封闭处理,再以苯骈三氮唑封护。氧化银的作用是___________ 。
(1)铜的制取:以氧化铜为原料制取铜。某研究小组为探究CO的还原性,设计了如下系列实验。

实验1:将CuO加水制成糊状,刷在试管内壁,在试管底部加入炭粉,再向试管中通入CO2(见图甲),集满后立即用气球密封。
实验2:用酒精灯加热CuO部位(见图乙),无明显现象。
实验3:用加网罩的酒精灯加热炭粉(见图丙);一段时间后,利用CO2传感器测得试管内CO2含量变小。
实验4:加热CuO(见图丁),黑色固体变成紫红色。
①实验1中浓硫酸的作用是
②实验2得到的结论是
③实验3的目的是
④写出实验4中发生反应的化学方程式:
(2)铜的锈蚀:铜锈的主要成分是碱式碳酸铜[化学式为Cu2(OH)2CO3]。
进行如下图所示的实验,探究铜生锈的条件。
将大小相同的4小块铜片按下图装置所示放置一个月,结果如下:
| 编号 | ① | ② | ③ | ④ |
| 实验 | 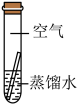 |  |  |  |
| 现象 | 铜片表面有绿色物质 | 无明显现象 | 无明显现象 | 无明显现象 |
②能说明铜生锈与H2O有关的实验是
③通过上述实验现象,写出铜片表面生成铜锈的化学方程式:
【查阅资料】铜锈一般分为无害锈与有害锈两种。[Cu2(OH)2CO3]属于“无害锈”,无害锈能保护青铜器。青铜器表面的有害锈为CuCl2·3Cu(OH)2,为绿色粉末,有害锈会使器物受损加剧,并不断扩散。有害锈的形成原理:铜在有Cl-的条件下生成CuCl,CuCl与氧气、水继续发生如下反应:
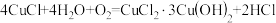 。
。④与有害锈相比,无害锈能保护青铜器的原因可能是
⑤为了有效的保护受腐蚀的青铜器,先将受腐蚀的青铜器用蒸馏水清洗干净,然后对锈蚀区用氧化银(Ag2O)封闭处理,再以苯骈三氮唑封护。氧化银的作用是
您最近一年使用:0次




