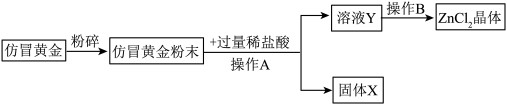
某化学兴趣小组对某仿冒黄金(铜锌合金)进行如下处理,请回答有关问题:
(1) 的金属活动性更强的是
的金属活动性更强的是________ 。
(2)操作A之前加入过量稀盐酸,请写出相关反应的化学方程式________ 。
(3)液体Y中含有 和
和_______ (写化学式)。
(4)将 该铜锌合金投入到足量的硫酸亚铁溶液中充分反应,过滤后将滤渣洗涤、干燥,称得固体减少的质量为
该铜锌合金投入到足量的硫酸亚铁溶液中充分反应,过滤后将滤渣洗涤、干燥,称得固体减少的质量为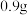 .则该合金中锌的质量分数为
.则该合金中锌的质量分数为________ 。

(1)
 的金属活动性更强的是
的金属活动性更强的是(2)操作A之前加入过量稀盐酸,请写出相关反应的化学方程式
(3)液体Y中含有
 和
和(4)将
 该铜锌合金投入到足量的硫酸亚铁溶液中充分反应,过滤后将滤渣洗涤、干燥,称得固体减少的质量为
该铜锌合金投入到足量的硫酸亚铁溶液中充分反应,过滤后将滤渣洗涤、干燥,称得固体减少的质量为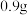 .则该合金中锌的质量分数为
.则该合金中锌的质量分数为
更新时间:2023-06-15 09:16:13
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“鍮石”是一种铜锌合金。北宋时,我国已出现了利用炉甘石(ZnCO3)、铜、木炭的混合物冶炼这种合金的技术,并用于铸造实用器。
(1)“鍮石”比纯铜更有利于铸造,原因是其熔点比纯铜更___________ (填“高”或“低”)。
(2)800°C时,炉甘石发生分解反应产生两种氧化物,该反应的方程式为:___________ 。
(3)冶炼“鍮石”过程中,木炭与氧化锌的反应为 ,反应中X的化学式为
,反应中X的化学式为___________ ,该反应中氧化锌发生了___________ 反应(填“氧化”或“还原”)。
(4)为测定“鍮石”中锌的质量分数,用足量稀盐酸与质量为a的“鍮石”样品充分反应,测得反应最终生成的气体质量为b,固体残余物质量为c。根据所测数据,“鍮石”中锌的质量分数的计算表达式:ω(Zn)=___________ ×100%。
(1)“鍮石”比纯铜更有利于铸造,原因是其熔点比纯铜更
(2)800°C时,炉甘石发生分解反应产生两种氧化物,该反应的方程式为:
(3)冶炼“鍮石”过程中,木炭与氧化锌的反应为
 ,反应中X的化学式为
,反应中X的化学式为(4)为测定“鍮石”中锌的质量分数,用足量稀盐酸与质量为a的“鍮石”样品充分反应,测得反应最终生成的气体质量为b,固体残余物质量为c。根据所测数据,“鍮石”中锌的质量分数的计算表达式:ω(Zn)=
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐2】某同学取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,如图:

(1)塑料试剂瓶膨胀破裂的原因是___________ ,反应的化学方程式为___________ 。
(2)破裂后瓶内试剂会吸收空气中CO2生成CaCO3.为测定其中CaCO3的质量分数,兴取小组分别进行如下实验:
实验1:称取10.0g样品,加50.0g水溶解,搅拌、静置、过滤,将沉淀洗涤、干燥、称重。
实验2:称取10.0g样品,向其中加入足量稀盐酸,充分反应,收集产生的气体。
①根据实验1称重计算样品中CaCO3的质量分数可能偏高,原因是________________ 。
②若实验2中收集的气体为2.2g,计算样品中CaCO3的质量分数。(请写出计算过程)____

(1)塑料试剂瓶膨胀破裂的原因是
(2)破裂后瓶内试剂会吸收空气中CO2生成CaCO3.为测定其中CaCO3的质量分数,兴取小组分别进行如下实验:
实验1:称取10.0g样品,加50.0g水溶解,搅拌、静置、过滤,将沉淀洗涤、干燥、称重。
实验2:称取10.0g样品,向其中加入足量稀盐酸,充分反应,收集产生的气体。
①根据实验1称重计算样品中CaCO3的质量分数可能偏高,原因是
②若实验2中收集的气体为2.2g,计算样品中CaCO3的质量分数。(请写出计算过程)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】木炭与氧化铜充分反应后的混合粉末中含有铜粉和木炭粉,某化学实验小组设计提纯金属铜的方案如下:

(1)将混合粉末在空气中充分灼烧后所得气体为________ (填化学式)。
(2)在实验室中进行过滤操作时,玻璃棒的作用是________ 。
(3)从固体②中提取出纯净的铜,可加入的试剂为________ 。
(4)取100g氧化铜和木炭的混合物在高温下充分反应后,测得剩余固体质量为78g,请计算原混合物中被还原的氧化铜的质量为________ g。

(1)将混合粉末在空气中充分灼烧后所得气体为
(2)在实验室中进行过滤操作时,玻璃棒的作用是
(3)从固体②中提取出纯净的铜,可加入的试剂为
(4)取100g氧化铜和木炭的混合物在高温下充分反应后,测得剩余固体质量为78g,请计算原混合物中被还原的氧化铜的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】Y形管的使用能增强实验的对比性。请根据如图三个实验回答问题。
已知:白磷和红磷的着火点分别为40℃、240℃。
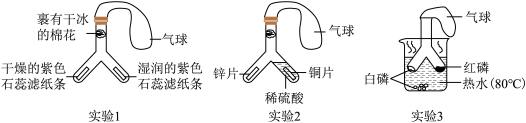
(1)实验1中,说明二氧化碳能与水反应的现象是______ 。
(2)实验2中,倾斜Y型管,使稀硫酸接触锌片,发生反应的化学方程式为______ 。锌片表面产生气泡,而铜片表面无气泡产生,说明金属活动性锌______ 铜(填>或<)。
(3)实验3中,若要证明燃烧需要氧气,应对比图中______ (填序号)处的实验现象。
已知:白磷和红磷的着火点分别为40℃、240℃。

(1)实验1中,说明二氧化碳能与水反应的现象是
(2)实验2中,倾斜Y型管,使稀硫酸接触锌片,发生反应的化学方程式为
(3)实验3中,若要证明燃烧需要氧气,应对比图中
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E均为初中化学中常见的物质。B是世界上年产量最高的金属,B与E在潮湿的环境中反应生成A,C是一种有毒气体。如图所示,相连的物质之间可以发生化学反应。请回答下列问题:
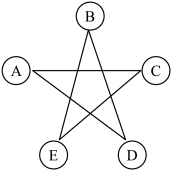
(1)物质C的化学式为_______ 。
(2)物质A与D反应的化学方程式为_____________ 。
(3)物质B与D反应的基本类型是____________ 。
(4)写出物质E的一种用途___________ 。

(1)物质C的化学式为
(2)物质A与D反应的化学方程式为
(3)物质B与D反应的基本类型是
(4)写出物质E的一种用途
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某金属加工厂有大量金属铝、铁、铜的废弃粉末,为充分利用金属资源,分离和回收金属,某化学兴趣小组通过查阅资料设计了如下实验方案:

请完成下列各题:
(1)步骤①中分离得到的金属B是______ 。
(2)步骤②发生反应的化学方程式为:_______ ,该反应的基本类型属于_________ 。
(3)步骤③生成沉淀的化学方程式为:_____ ;因Al(OH)3既能与酸反应又能与碱反应,故步骤③加入某试剂时应采用的是_______ (选填“滴加”或“倾倒”)操作。
(4)电解熔融Al2O3制金属铝的化学方程式为:______ 。

请完成下列各题:
(1)步骤①中分离得到的金属B是
(2)步骤②发生反应的化学方程式为:
(3)步骤③生成沉淀的化学方程式为:
(4)电解熔融Al2O3制金属铝的化学方程式为:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属材料广泛应用于生产生活中。
(1)铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为_____________ 。
(2)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是_____________ (写化学式)。
(3)铁矿石有多种,如赤铁矿(主要成分 Fe2O3)和磁铁矿(主要成分 Fe3O4)等。写出磁铁矿石中的主要成分与一氧化碳反应的化学方程式_____________ 。
(4)含有锌粉 6.5g、铁粉 5.6g、铜粉 3.2g、铝粉 l.8g 的混合物与一定质量的稀硫酸充分反应,反应停止后,有 6g 固体剩余。则生成氢气的质量为____________ g。
(1)铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物的化学式为
(2)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是
(3)铁矿石有多种,如赤铁矿(主要成分 Fe2O3)和磁铁矿(主要成分 Fe3O4)等。写出磁铁矿石中的主要成分与一氧化碳反应的化学方程式
(4)含有锌粉 6.5g、铁粉 5.6g、铜粉 3.2g、铝粉 l.8g 的混合物与一定质量的稀硫酸充分反应,反应停止后,有 6g 固体剩余。则生成氢气的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国古代就掌握了炼铜技术,青铜是铜冶铸史上最早得到的合金。
I.用孔雀石【主要成分Cu2(OH)2CO3】炼铜。高温煅烧孔雀石,可得黑色固体和两种非金属氧化物。部分含铜元素的物质类别及化合价转化关系如图所示。

(1)图中Cu2(OH)2CO3位于A点,黑色固体位于_______ (选填B、C或D)点。
(2)加入木炭,一定条件下可实现C→D的转化,同时产生可使澄清石灰水变浑浊的气体。该过程体现了木炭具有_______ 性质反应的化学方程式为_______ 。
(3)图中A→B的反应属于_______ 反应(填基本反应类型)。
II.《大治赋》记载由硫化铜矿(主要成分Cu2S)制取CuSO4溶液,再用铁片浸取铜的方法。硫化铜矿中Cu2S转化的流程如下:

(4)Cu2S中Cu与S的质量比为_______ 。“浸铁”中利用了Fe的金属活动性比Cu_______ 的性质(选填“强”或“弱”)。
(5)依据上述流程分析,若需将Cu2S中铜元素全转化为铜单质,除了H2O、O2和Fe以外,还需补充的物质是_______ 。
(6)在冶炼中加入锡等金属可得到青铜,下列说法正确的是_______。
I.用孔雀石【主要成分Cu2(OH)2CO3】炼铜。高温煅烧孔雀石,可得黑色固体和两种非金属氧化物。部分含铜元素的物质类别及化合价转化关系如图所示。

(1)图中Cu2(OH)2CO3位于A点,黑色固体位于
(2)加入木炭,一定条件下可实现C→D的转化,同时产生可使澄清石灰水变浑浊的气体。该过程体现了木炭具有
(3)图中A→B的反应属于
II.《大治赋》记载由硫化铜矿(主要成分Cu2S)制取CuSO4溶液,再用铁片浸取铜的方法。硫化铜矿中Cu2S转化的流程如下:

(4)Cu2S中Cu与S的质量比为
(5)依据上述流程分析,若需将Cu2S中铜元素全转化为铜单质,除了H2O、O2和Fe以外,还需补充的物质是
(6)在冶炼中加入锡等金属可得到青铜,下列说法正确的是_______。
| A.青铜是金属材料 |
| B.纯铜比青铜的硬度大 |
| C.青铜比纯铜的熔点低 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学金属的相关知识回答下列问题。
(1)某合金中含有金属钪(Sc)。相同条件下,取相同形状的、相同质量的金属钪和锌分别与同体积、同浓度的盐酸反应,观察到钪产生的气泡速率明显更快,则下列说法正确的是_____ (填序号)。
①用Sc、Cu、稀硫酸能验证钪和铜的活动性强弱
②用Sc、Fe、Zn(NO3)2能验证钪、铁、锌的活动性强弱
③用Sc、Cu(NO3)2溶液、AgNO3溶液能验证钪、铜、银的活动性强弱
④用Sc粉、Fe粉、稀硫酸、Cu(NO3)2溶液能验证钪、铁、铜的活动性强弱
(2)小柯为比较Mg、Fe、Cu三种金属的活动性顺序。进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,写出红色固体增多的方程式_____ 。

充分反应后过滤,滤液中一定含有的金属离子有_____ (写出离子符号)。
(1)某合金中含有金属钪(Sc)。相同条件下,取相同形状的、相同质量的金属钪和锌分别与同体积、同浓度的盐酸反应,观察到钪产生的气泡速率明显更快,则下列说法正确的是
①用Sc、Cu、稀硫酸能验证钪和铜的活动性强弱
②用Sc、Fe、Zn(NO3)2能验证钪、铁、锌的活动性强弱
③用Sc、Cu(NO3)2溶液、AgNO3溶液能验证钪、铜、银的活动性强弱
④用Sc粉、Fe粉、稀硫酸、Cu(NO3)2溶液能验证钪、铁、铜的活动性强弱
(2)小柯为比较Mg、Fe、Cu三种金属的活动性顺序。进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,写出红色固体增多的方程式

充分反应后过滤,滤液中一定含有的金属离子有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】向一定质量AgNO3、Cu(NO3)2和Fe(NO3)2的混合溶液中加入过量的Zn,溶液质量随反应时间变化的情况如图所示。

(1)写出ab段有关反应的化学方程式。___________
(2)若将反应至c点时的混合物过滤,所得固体中含有哪些物质? (写化学式)___________
(3)所得溶液的质量与原混合溶液的质量相比,可能减小,其原因是什么?___________

(1)写出ab段有关反应的化学方程式。
(2)若将反应至c点时的混合物过滤,所得固体中含有哪些物质? (写化学式)
(3)所得溶液的质量与原混合溶液的质量相比,可能减小,其原因是什么?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将金属R(化合价为+2价)的粉末放入盛有硝酸铜和硝酸银的混合溶液的烧杯中,充分后过滤,得到固体甲和溶液乙,若反应前后烧杯中溶液的质量不变,则:
(1)R可能是什么金属并说明原因______ 。
(2)分析固体甲的成分______ 。
(3)写出上述的其中一个化学方程式______ 。
(1)R可能是什么金属并说明原因
(2)分析固体甲的成分
(3)写出上述的其中一个化学方程式
您最近一年使用:0次



