扎实做好“碳达峰”“碳中和”各项工作,体现了我国主动承担应对气候变化的国际责任、推动构建人类命运共同体的责任担当。请回答:
(1)“碳达峰”“碳中和”中的“碳”指的是_____ (填化学式)。
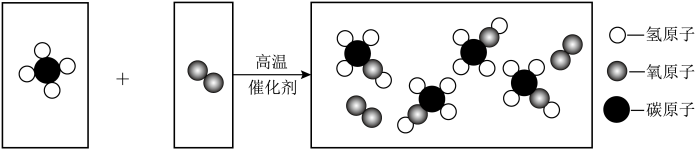
(2)“碳”减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为: ,则X的化学式为
,则X的化学式为_____ 。
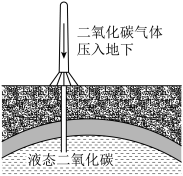
(3)“碳捕捉和封存”技术是实现“碳中和”的重要途径。重庆合川实验基地通过如图技术将 压入地下实现
压入地下实现 的封存。这里的
的封存。这里的 捕集是一个
捕集是一个_____ (填“物理”或“化学”)过程。此过程中 分子间隔
分子间隔_____ 。
(4)转化法是实现“碳中和”的措施之一,下图为根据初中化学有关知识、结合有关资料,得到的碳的转化关系。
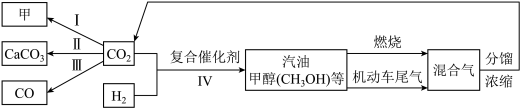
①若甲为单质,自然界通过光合作用完成转化I,则甲为_____ 。
②转化Ⅱ反应的化学方程式为_____ 。
③二氧化碳与碳反应,完成转化Ⅲ,反应的化学方程式为_____ 。
④转化Ⅳ是将 和
和 在催化剂的作用下转化成甲醇
在催化剂的作用下转化成甲醇 和水,是目前研究的热点,该反应的化学方程式为
和水,是目前研究的热点,该反应的化学方程式为_____ 。
(5)在日常生活中,你如何践行“低碳生活”理念_____ (写一条即可)。
(1)“碳达峰”“碳中和”中的“碳”指的是
(2)“碳”减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:
 ,则X的化学式为
,则X的化学式为(3)“碳捕捉和封存”技术是实现“碳中和”的重要途径。重庆合川实验基地通过如图技术将
 压入地下实现
压入地下实现 的封存。这里的
的封存。这里的 捕集是一个
捕集是一个 分子间隔
分子间隔
(4)转化法是实现“碳中和”的措施之一,下图为根据初中化学有关知识、结合有关资料,得到的碳的转化关系。

①若甲为单质,自然界通过光合作用完成转化I,则甲为
②转化Ⅱ反应的化学方程式为
③二氧化碳与碳反应,完成转化Ⅲ,反应的化学方程式为
④转化Ⅳ是将
 和
和 在催化剂的作用下转化成甲醇
在催化剂的作用下转化成甲醇 和水,是目前研究的热点,该反应的化学方程式为
和水,是目前研究的热点,该反应的化学方程式为(5)在日常生活中,你如何践行“低碳生活”理念
更新时间:2023-07-06 16:12:00
|
相似题推荐
【推荐1】分类研究是化学研究物质的常用方法。某化学兴趣小组同学总结了酸的“通性”,又分析了酸的“个性”,请回答下列问题:
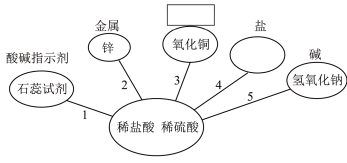
(1)稀盐酸、稀硫酸化学性质相似,是因为______ 。
(2)氧化铜的物质类别______ 。
(3)反应4中的盐既能与稀盐酸反应,又能与稀硫酸反应,写出这种盐与某种碱反应的化学方程式______ 。
(4)同学们发现实验室中还有硝酸,为了进一步了解硝酸的“个性”,他们在老师的指导下进行以下探究:
Ⅰ、硝酸能与金属反生成水: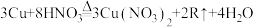 。则R的化学式为
。则R的化学式为______ 。
Ⅱ、浓硝酸能与蛋白质作用:向盛有蛋清溶液的试管中加几滴浓硝酸,微热,观察到出现黄色固体,该变化属于______ (填“物理变化”或“化学变化”)。
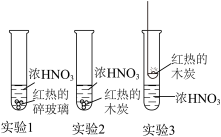
Ⅲ、硝酸能与某些非金属反应。同学们进行如下实验,发现均有红棕色NO2气体产生。
查阅资料:
a.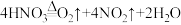
b.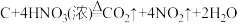
c.浓硝酸具有挥发性。
①实验1中所用碎玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用______ 。
②实验2中有红棕色气体产生,但并不能证明实验2中木炭与浓硝酸发生了反应,理由是______ 。
③实验3在生成的气体产物中检测出二氧化碳,且体积分数大于0.03%,但也不能证明实验3中木炭与浓硝酸发生了反应,理由是______ 。

(1)稀盐酸、稀硫酸化学性质相似,是因为
(2)氧化铜的物质类别
(3)反应4中的盐既能与稀盐酸反应,又能与稀硫酸反应,写出这种盐与某种碱反应的化学方程式
(4)同学们发现实验室中还有硝酸,为了进一步了解硝酸的“个性”,他们在老师的指导下进行以下探究:
Ⅰ、硝酸能与金属反生成水:
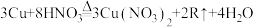 。则R的化学式为
。则R的化学式为Ⅱ、浓硝酸能与蛋白质作用:向盛有蛋清溶液的试管中加几滴浓硝酸,微热,观察到出现黄色固体,该变化属于
Ⅲ、硝酸能与某些非金属反应。同学们进行如下实验,发现均有红棕色NO2气体产生。

查阅资料:
a.
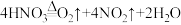
b.
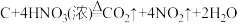
c.浓硝酸具有挥发性。
①实验1中所用碎玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用
②实验2中有红棕色气体产生,但并不能证明实验2中木炭与浓硝酸发生了反应,理由是
③实验3在生成的气体产物中检测出二氧化碳,且体积分数大于0.03%,但也不能证明实验3中木炭与浓硝酸发生了反应,理由是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】北京2022冬奥会秉持着“绿色冬奥”的理念,把碳达峰、碳中和纳入了生态文明建设的整体布局,采取了低碳场馆、低碳能源、低碳交通等多项科技助推的措施,真正让“绿色”成为这场冬奥会的鲜明底色。
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是 (填序号)。
(2)为减缓温室效应,有科学家猜想将空气中的二氧化碳输送到冰冷的深海中贮藏,但也有科学家担心这样做会增加海水的酸度,导致海洋生物死亡,二氧化碳使海水酸度增加的原因是____ (用化学方程式表示)。
(3)使用膜分离法可以从空气中分离出二氧化碳气体,该过程发生的是____ (填“物理”或“化学”)变化。
(4)实验室常用大理石和稀盐酸制取二氧化碳。某化学兴趣小组现取25g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。请根据要求回答问题:
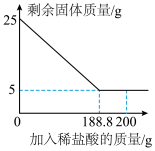
①参加反应的碳酸钙质量是____ g。
②计算恰好完全反应时,所得不饱和溶液的质量_____ (计算结果精确到0.1g)。
(1)为保护人类赖以生存的地球,我们应采取有效措施以防止大气中二氧化碳含量的大量增加,以下建议中行之有效的措施是 (填序号)。
| A.开发太阳能、风能、地热能、潮汐能等新能源 |
| B.禁止使用煤、石油、天然气等矿物燃料 |
| C.大量植树造林绿化环境,禁止乱砍滥伐 |
(2)为减缓温室效应,有科学家猜想将空气中的二氧化碳输送到冰冷的深海中贮藏,但也有科学家担心这样做会增加海水的酸度,导致海洋生物死亡,二氧化碳使海水酸度增加的原因是
(3)使用膜分离法可以从空气中分离出二氧化碳气体,该过程发生的是
(4)实验室常用大理石和稀盐酸制取二氧化碳。某化学兴趣小组现取25g含碳酸钙的大理石于烧杯中,缓慢加入稀盐酸(大理石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如图所示。请根据要求回答问题:

①参加反应的碳酸钙质量是
②计算恰好完全反应时,所得不饱和溶液的质量
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】空气是一种宝贵的自然资源。根据下列材料回答问题:
材料一:工业上制取氧气常见的有“深冷法”(如图1)和“变压吸附法”(如图2)。同时得到的副产品氮气也是一种重要的化学物质,可用于制造氨气、硝酸和氮肥。
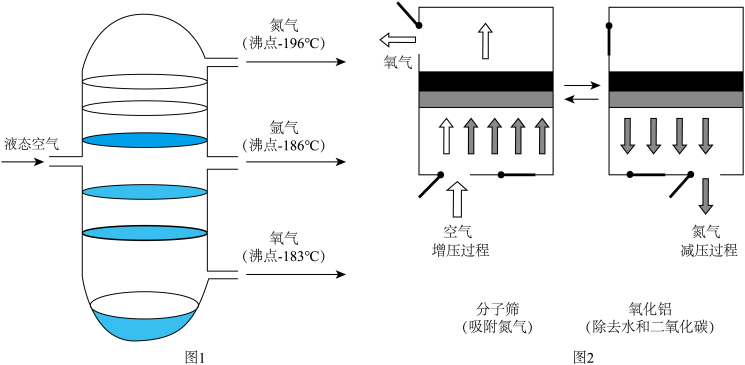
(1)“深冷法”(如图1)是先将空气在一定条件下液化,再利用氮气和氧气的____ 不同将其汽化分离。
(2)将燃着的木条置于盛满液态空气的集气瓶口,观察到的现象是____ 。
(3)“变压吸附法”(如图2)是利用分子筛吸附氮气和氧气能力的差异,通过增压与减压的交替循环,实现氮气和氧气的分离。
①用分子筛吸附氮气发生的是____ (填“物理”或“化学”)变化。
②分子筛对氮气的吸附能力与吸附塔内气体的____ 有关。
③分子筛____ (填“可以”或“不可以”)重复使用。
(4)工业上不用过氧化氢或高锰酸钾分解制取氧气的原因是_______ 。
材料二:工业用氮气合成氨的流程如图3所示。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如题图4所示。
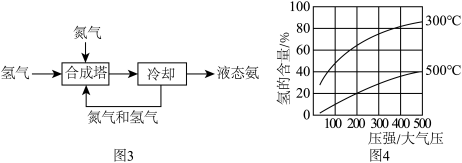
(5)①由图3可知合成塔中物质属于______ (填“混合物”、“纯净物”)。
②甲烷和水高温下反应得到一氧化碳和氢气,该反应的文字表达式为______ 。
③按下列条件进行合成氨反应,平衡时氨的含量最高的是______ (填字母)。
A.200大气压、300℃
B.200大气压、500℃
C.400大气压、300℃
D.400大气压、500℃
材料一:工业上制取氧气常见的有“深冷法”(如图1)和“变压吸附法”(如图2)。同时得到的副产品氮气也是一种重要的化学物质,可用于制造氨气、硝酸和氮肥。

(1)“深冷法”(如图1)是先将空气在一定条件下液化,再利用氮气和氧气的
(2)将燃着的木条置于盛满液态空气的集气瓶口,观察到的现象是
(3)“变压吸附法”(如图2)是利用分子筛吸附氮气和氧气能力的差异,通过增压与减压的交替循环,实现氮气和氧气的分离。
①用分子筛吸附氮气发生的是
②分子筛对氮气的吸附能力与吸附塔内气体的
③分子筛
(4)工业上不用过氧化氢或高锰酸钾分解制取氧气的原因是
材料二:工业用氮气合成氨的流程如图3所示。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如题图4所示。

(5)①由图3可知合成塔中物质属于
②甲烷和水高温下反应得到一氧化碳和氢气,该反应的文字表达式为
③按下列条件进行合成氨反应,平衡时氨的含量最高的是
A.200大气压、300℃
B.200大气压、500℃
C.400大气压、300℃
D.400大气压、500℃
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】低碳冶金技术的发展为我国实现2060年“碳中和”目标提供了有力的保障,其中氢冶金技术成为最受关注的领域。目前,氢气主要来源于化石燃料制氢,竖炉氢冶炼铁工艺流程如图所示。
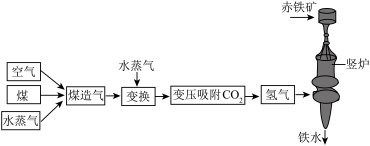
(1)“煤造气”过程发生的反应之一如下:C+H2O
_______ +H2,该反应中碳体现出_______ 性。
(2)“变换”过程发生了化学变化,其中水蒸气的作用是_______ (填一点即可)。
(3)用氢气代替一氧化碳炼铁可有效降低二氧化碳的排放。计算用氢气冶炼1000t赤铁矿(纯度为80%)时,可减少排放的二氧化碳质量_______ (写出计算过程)。④
(4)某种热分析仪记录下48.0gFe2O3被H2逐步还原成铁的有关数据,得到固体质量与反应温度的关系曲线如图所示,请计算分析P点固体的化学式_______ 。


(1)“煤造气”过程发生的反应之一如下:C+H2O

(2)“变换”过程发生了化学变化,其中水蒸气的作用是
(3)用氢气代替一氧化碳炼铁可有效降低二氧化碳的排放。计算用氢气冶炼1000t赤铁矿(纯度为80%)时,可减少排放的二氧化碳质量
(4)某种热分析仪记录下48.0gFe2O3被H2逐步还原成铁的有关数据,得到固体质量与反应温度的关系曲线如图所示,请计算分析P点固体的化学式

您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。
(1)建造航母用到了钛合金,构成金属钛的粒子是___ (填“原子”“分子”或“离子”),工业制钛有一种反应为: ,X的化学式为
,X的化学式为___ 。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与___ 接触而锈蚀。
(3)请你用化学方程式表示出探究航母材料中铝、铜两种金属活动性强弱的方法___ 。
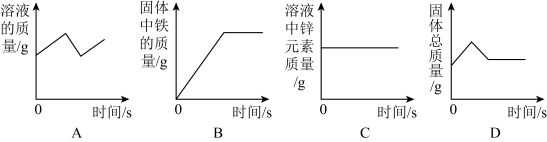
(4)康康为了探究航母中金属锌的化学性质,将一定量的锌粉加入到硝酸亚铁、硝酸银的混合溶液中,溶液最终变为无色。下列图像能表示对应变化关系的是___ (填字母序号)。
(5)如图是工业炼铁示意图。

①炼铁的固体原料需经过粉碎,其目的是什么?_____ 。
②冶炼过程中焦炭的作用是什么?______ 。
③若要炼制含铁96%的生铁70t,则理论上需要含杂质20%的赤铁矿的质量是多少?_____ 。
(1)建造航母用到了钛合金,构成金属钛的粒子是
 ,X的化学式为
,X的化学式为(2)航母外壳用涂料覆盖,是为了防止钢铁材料与
(3)请你用化学方程式表示出探究航母材料中铝、铜两种金属活动性强弱的方法
(4)康康为了探究航母中金属锌的化学性质,将一定量的锌粉加入到硝酸亚铁、硝酸银的混合溶液中,溶液最终变为无色。下列图像能表示对应变化关系的是

(5)如图是工业炼铁示意图。

①炼铁的固体原料需经过粉碎,其目的是什么?
②冶炼过程中焦炭的作用是什么?
③若要炼制含铁96%的生铁70t,则理论上需要含杂质20%的赤铁矿的质量是多少?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】A~E 均为初中化学常见的物质,它们之间的关系如图所示(“→”表示物质可以转化,“—”表示两物质可以发生反应,部分反应物、生成物和反应条件均已略去),已知 D 为一种常见的盐,D、E 的水溶液均呈碱性, 且 D、E 为不同类别物质,A 与 B 的组成元素相同,且 B 是最常见的液体,请回答下列问题:

(1)物质 B 的化学式为______ ,物质 D 俗称是______ 。
(2)请写出 D→E 的反应化学方程式:______ ;该反应的基本反应类型是______ 。
(3)请写出物质 C 在生活中的一种常见的用途______ 。
(4)实验室常用分解 A 来制备氧气,实验过程需要加入 MnO2作为催化剂。某研究性学习小组设计了将粗 MnO2(含有较多 MnO 和 MnCO3)样品转化为纯 MnO2的实验,其流程如图所示:
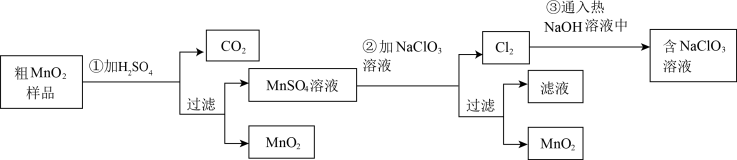
①加稀硫酸之前粗 MnO2样品必须研磨,目的是______ ;
②该流程中多次用到过滤操作,其中需要用到的玻璃仪器有烧杯、玻璃棒和______ ;
③请将第②步反应化学方程式补充完整:5MnSO4+2NaClO3+4______ =5MnO2+Cl2↑+4H2SO4+Na2SO4;
④检验第②步反应后过滤所得滤液中含 SO42-的设计方法是______ 。

(1)物质 B 的化学式为
(2)请写出 D→E 的反应化学方程式:
(3)请写出物质 C 在生活中的一种常见的用途
(4)实验室常用分解 A 来制备氧气,实验过程需要加入 MnO2作为催化剂。某研究性学习小组设计了将粗 MnO2(含有较多 MnO 和 MnCO3)样品转化为纯 MnO2的实验,其流程如图所示:

①加稀硫酸之前粗 MnO2样品必须研磨,目的是
②该流程中多次用到过滤操作,其中需要用到的玻璃仪器有烧杯、玻璃棒和
③请将第②步反应化学方程式补充完整:5MnSO4+2NaClO3+4
④检验第②步反应后过滤所得滤液中含 SO42-的设计方法是
您最近一年使用:0次
【推荐1】通过化学课程的学习,我们收获很多。
收获一:在宏观、微观和符号之间建立联系是化学学科的特点。
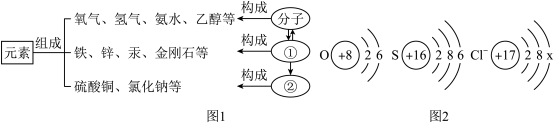
(1)物质的组成及构成关系如图1所示,图1中①表示的是______ 。
(2)图2是氧、硫、氯三种元素的粒子结构示意图。
①氯离子的结构示意图中x的数值是______ 。
②氧和氯两种元素最本质的区别是它们原子中的______ 不相同。
收获二:我们学会了从微观的角度认识物质及其反应。
(3)下列各图中“ ”“
”“ ”分别表示两种不同元素的原子,其中可能表示氧化物的是____。
”分别表示两种不同元素的原子,其中可能表示氧化物的是____。
(4)某反应前后分子变化的微观示意图如下,下列说法正确的是_____。
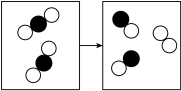 “
“ ”和“
”和“  ”表示不同元素的原子
”表示不同元素的原子
收获三:我们知道常见物质之间存在着一定的转化关系。
已知A~G都是初中化学常见的物质,通常情况下,A,C为无色液体,且都是由两种相同元素组成,D、E为气体,它们之间的转化关系如图所示。回答下列问题:
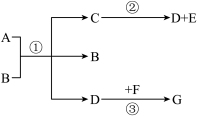
(5)请写出化学式A___________ 、C___________ 、D___________ 。
(6)物质B在反应①中的作用是_______________________ 。
(7)检验气体D的方法是__________________________ 。
收获一:在宏观、微观和符号之间建立联系是化学学科的特点。

(1)物质的组成及构成关系如图1所示,图1中①表示的是
(2)图2是氧、硫、氯三种元素的粒子结构示意图。
①氯离子的结构示意图中x的数值是
②氧和氯两种元素最本质的区别是它们原子中的
收获二:我们学会了从微观的角度认识物质及其反应。
(3)下列各图中“
 ”“
”“ ”分别表示两种不同元素的原子,其中可能表示氧化物的是____。
”分别表示两种不同元素的原子,其中可能表示氧化物的是____。A.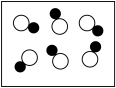 | B.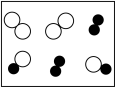 |
C. | D.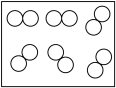 |
 “
“ ”和“
”和“  ”表示不同元素的原子
”表示不同元素的原子| A.反应物与生成物共有3种物质 | B.反应后原子的个数增多 |
| C.该图可示意加热氧化汞的反应 | D.该反应属于分解反应 |
收获三:我们知道常见物质之间存在着一定的转化关系。
已知A~G都是初中化学常见的物质,通常情况下,A,C为无色液体,且都是由两种相同元素组成,D、E为气体,它们之间的转化关系如图所示。回答下列问题:

(5)请写出化学式A
(6)物质B在反应①中的作用是
(7)检验气体D的方法是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】“碳捕捉技术”是指通过一定的方法,将工业生产中产生的 分离出来进行储存和利用的工艺和技术。
分离出来进行储存和利用的工艺和技术。
(1)最近有科学家提出“绿色自由”构想:把 含量高的气体吹入饱和
含量高的气体吹入饱和 溶液中,生成
溶液中,生成  ,然后利用
,然后利用 受热易分解的性质,再把
受热易分解的性质,再把  提取出来,经化学反应使之变为甲醇(
提取出来,经化学反应使之变为甲醇(  )和水。“绿色自由”构想的技术流程如下图:
)和水。“绿色自由”构想的技术流程如下图:
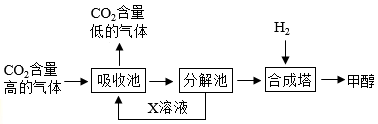
(注:分解池内的反应条件是加热;合成塔内的反应条件为300℃、200 和催化剂)
和催化剂)
①分解池内反应的化学方程式为______ ;②合成塔内反应的化学方程式为 ______ ;③ 溶液可循环利用,溶质是
溶液可循环利用,溶质是 ______ (填化学式)。
(2)实际生产中,经常利用 溶液来“捕捉”
溶液来“捕捉”  ,流程图如下图(部分条件及物质未标出):
,流程图如下图(部分条件及物质未标出):
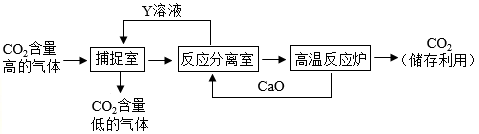
①捕捉室内反应的化学方程式为______ ;②反应分离室中发生反应的化学方程式为 ______ 、 ______ ;③该生产过程中,涉及到的物质属于碱的是 ______ (填化学式)。
 分离出来进行储存和利用的工艺和技术。
分离出来进行储存和利用的工艺和技术。(1)最近有科学家提出“绿色自由”构想:把
 含量高的气体吹入饱和
含量高的气体吹入饱和 溶液中,生成
溶液中,生成  ,然后利用
,然后利用 受热易分解的性质,再把
受热易分解的性质,再把  提取出来,经化学反应使之变为甲醇(
提取出来,经化学反应使之变为甲醇(  )和水。“绿色自由”构想的技术流程如下图:
)和水。“绿色自由”构想的技术流程如下图:
(注:分解池内的反应条件是加热;合成塔内的反应条件为300℃、200
 和催化剂)
和催化剂)①分解池内反应的化学方程式为
 溶液可循环利用,溶质是
溶液可循环利用,溶质是 (2)实际生产中,经常利用
 溶液来“捕捉”
溶液来“捕捉”  ,流程图如下图(部分条件及物质未标出):
,流程图如下图(部分条件及物质未标出):
①捕捉室内反应的化学方程式为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】请回答下列问题。
Ⅰ.高纯硅可用于制备硅半导体材料,其主要生产流程如图所示:
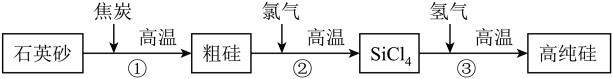
(1)①发生反应的化学方程式为 ,该反应中属于氧化物的是
,该反应中属于氧化物的是___________ (填化学式),一氧化碳在生产生活中的用途是___________ (写一种即可)。
(2)反应的化学方程式为SiCl4+2H2 Si+4HCl ,该反应中氢元素的化合价变化为零价→+1价,硅元素的化合价变化为
Si+4HCl ,该反应中氢元素的化合价变化为零价→+1价,硅元素的化合价变化为___________ 。
Ⅱ.A~I都是初中化学中的常见物质,A是大理石、石灰石、鸡蛋壳的主要成分。C、E为气体且元素组成相同,其中E为有毒气体。D、H为黑色固体,I为红色金属单质。它们的转化关系如图所示,请回答下列有关问题:

(3)写出下列物质的化学式:B________ :D________ :G_______ 。
(4)反应②发生时要___________ (填“放出”或“吸收”)热量。
(5)写出反应①的化学方程式___________ ,该反应属于___________ (填基本反应类型)
(6)写出反应⑤的化学方程式___________ 。
Ⅰ.高纯硅可用于制备硅半导体材料,其主要生产流程如图所示:

(1)①发生反应的化学方程式为
 ,该反应中属于氧化物的是
,该反应中属于氧化物的是(2)反应的化学方程式为SiCl4+2H2
 Si+4HCl ,该反应中氢元素的化合价变化为零价→+1价,硅元素的化合价变化为
Si+4HCl ,该反应中氢元素的化合价变化为零价→+1价,硅元素的化合价变化为Ⅱ.A~I都是初中化学中的常见物质,A是大理石、石灰石、鸡蛋壳的主要成分。C、E为气体且元素组成相同,其中E为有毒气体。D、H为黑色固体,I为红色金属单质。它们的转化关系如图所示,请回答下列有关问题:

(3)写出下列物质的化学式:B
(4)反应②发生时要
(5)写出反应①的化学方程式
(6)写出反应⑤的化学方程式
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】Ⅰ、工业炼铁和轧制钢材的主要流程如下图:
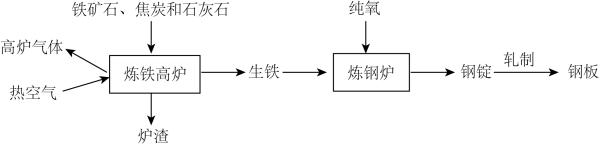
已知生铁的含碳量为2%-4.3%,钢的含碳量为0.03%-2%,铁矿石约含80%的Fe2O3。
(1)高炉炼铁的原理是______ (用化学方程式表示)。
(2)高炉气体含有较高浓度的一氧化碳和氧化铁尘粒,请对高炉气体处理提出一条合理化建议______ 。
(3)炼铁过程中,固体原料从炉顶加入,而热空气从炉底往上通的目的是______ 。
(4)生铁炼钢需要降低生铁中的碳、硫、硅等元素的含量,在工业上选择向炼钢炉通入“纯氧”而不通入“空气”的原因是______ 。
(5)写出一种预防钢铁制品生锈的措施或方法______ 。
Ⅱ、A~E都是初中化学1~6单元常见的物质,它们的组成元素均为非金属元素,且5种物质含有一种相同的元素,已知D是单质,另外四种物质都是化合物。图中“→”表示相连的两种物质能转化(反应条件和部分反应物、生成物已省略)。
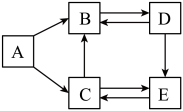
(6)D的化学式为______ 。
(7)C→E反应的化学方程式为______ 。
(8)若A能发生分解反应生成B和C,则A的化学式为______ 。
(9)关于以上图中各物质及相关反应的说法正确的是______ 。
①C和E都是对空气有污染的气体 ②E→C和C→E反应的基本类型可能相同
③E→C的反应中E发生还原反应 ④C→B反应可以用来检验C

已知生铁的含碳量为2%-4.3%,钢的含碳量为0.03%-2%,铁矿石约含80%的Fe2O3。
(1)高炉炼铁的原理是
(2)高炉气体含有较高浓度的一氧化碳和氧化铁尘粒,请对高炉气体处理提出一条合理化建议
(3)炼铁过程中,固体原料从炉顶加入,而热空气从炉底往上通的目的是
(4)生铁炼钢需要降低生铁中的碳、硫、硅等元素的含量,在工业上选择向炼钢炉通入“纯氧”而不通入“空气”的原因是
(5)写出一种预防钢铁制品生锈的措施或方法
Ⅱ、A~E都是初中化学1~6单元常见的物质,它们的组成元素均为非金属元素,且5种物质含有一种相同的元素,已知D是单质,另外四种物质都是化合物。图中“→”表示相连的两种物质能转化(反应条件和部分反应物、生成物已省略)。

(6)D的化学式为
(7)C→E反应的化学方程式为
(8)若A能发生分解反应生成B和C,则A的化学式为
(9)关于以上图中各物质及相关反应的说法正确的是
①C和E都是对空气有污染的气体 ②E→C和C→E反应的基本类型可能相同
③E→C的反应中E发生还原反应 ④C→B反应可以用来检验C
您最近一年使用:0次
【推荐3】低碳行动,我们一直在努力。
【CO2在大气中的作用】大气中,红外辐射可以透过N2和O2,但不能透过CO2.
方面:若没有CO2防止地表热辐射到太空,地球年均气温要降低20℃左右。
另一方面:CO2含量过高使温室效应加剧,温室效应对生态环境影响的一种现象是___________ 。
【空气中CO2增加的原因】CO2主要以下列三种途径产生。
(1)自然界中生物的有氧呼吸:细胞中的葡萄糖(化学式为C6H12O6)在酶的作用下与氧气反应,生成二氧化碳和水,其反应方程式为___________ 。
(2)化石燃料的燃烧:
下表列出了家庭常用化石燃料及其再生产品的相关数据,请回答下列问题。
①相同质量的水煤气和天然气若完全燃烧,产生CO2较少的是________ :理由是_________ 。
②与水煤气相比,天然气除了具有无毒、来源较广的优点,还具有的两个优点是_________ 、_________ 。
(3)工业上生产水泥的过程:水泥生产过程中产生的二氧化碳,主要源于高温煅烧石灰石和煤的燃烧,它们所涉及到的化学反应基本类型有_______ 种。
【CO2的转化】“碳中和”是当今我国环境治理的重大举措。
如图是同学们学过的物质与CO2相关联的示意图,图中A、B、C都含有碳元素。“一”表示两种物质能够发生化学反应,“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已忽略)。
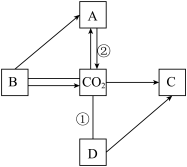
(4)物质B是_________ 。
(5)若反应①有明显现象,该反应化学方程式为_________ 。
(6)写出图中②属于化合反应的化学方程式:_________ 。
【CO2在大气中的作用】大气中,红外辐射可以透过N2和O2,但不能透过CO2.
方面:若没有CO2防止地表热辐射到太空,地球年均气温要降低20℃左右。
另一方面:CO2含量过高使温室效应加剧,温室效应对生态环境影响的一种现象是
【空气中CO2增加的原因】CO2主要以下列三种途径产生。
(1)自然界中生物的有氧呼吸:细胞中的葡萄糖(化学式为C6H12O6)在酶的作用下与氧气反应,生成二氧化碳和水,其反应方程式为
(2)化石燃料的燃烧:
下表列出了家庭常用化石燃料及其再生产品的相关数据,请回答下列问题。
| 名称 | 热值 | 爆炸极限 |
| 水煤气(H2和CO) | 1.9x107J/m3 | 6.9%—69.5% |
| 天然气 | 4.5×107J/m3 | 4.8%--13.5% |
②与水煤气相比,天然气除了具有无毒、来源较广的优点,还具有的两个优点是
(3)工业上生产水泥的过程:水泥生产过程中产生的二氧化碳,主要源于高温煅烧石灰石和煤的燃烧,它们所涉及到的化学反应基本类型有
【CO2的转化】“碳中和”是当今我国环境治理的重大举措。
如图是同学们学过的物质与CO2相关联的示意图,图中A、B、C都含有碳元素。“一”表示两种物质能够发生化学反应,“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已忽略)。

(4)物质B是
(5)若反应①有明显现象,该反应化学方程式为
(6)写出图中②属于化合反应的化学方程式:
您最近一年使用:0次

 与
与 之差表示
之差表示